Zinn(IV)-iodid
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
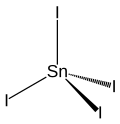 | |||||||||||||||||||
| Keile zur Verdeutlichung der räumlichen Struktur | |||||||||||||||||||
| Raumgruppe | Pa3 (Nr. 205) | ||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Zinn(IV)-iodid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | SnI4 | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 626,328 g·mol−1 | ||||||||||||||||||
| Aggregatzustand | fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | 364,5 °C[2] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Brechungsindex | 2,106[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Zinn(IV)-iodid ist eine anorganische chemische Verbindung des Zinns aus der Gruppe der Iodide.
Gewinnung und Darstellung
Zinn(IV)-iodid kann durch direkte Synthese aus den Elementen oder durch Erhitzen einer Zinn(II)-chlorid-Lösung mit Iod gewonnen werden.[1]
Eigenschaften
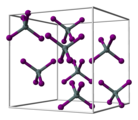
Zinn(IV)-iodid ist ein oranger Feststoff, der in Wasser hydrolysiert.[5] Es besitzt eine kubische Kristallstruktur mit der Raumgruppe Pa3 (Raumgruppen-Nr. 205), dem Gitterparameter a = 1226 pm und acht Formeleinheiten pro Elementarzelle.[6] Dies entspricht einer kubisch-dichtesten Kugelpackung von Iod-Atomen, in der 1/8 aller tetraedrischen Lücken mit Zinn-Atomen besetzt sind. Dies führt zu diskreten tetraedrischen SnI4-Molekülen.[7]
Einzelnachweise
- ↑ a b c d e Moeller, T., Edwards, D. C., Brandt, R. L. and Kleinberg, J.: Tin(IV) Iodide (Stannic Iodide). In: Inorganic Syntheses. 4. Jahrgang, 1953, S. 119–121, doi:10.1002/9780470132357.ch40.(eingeschränkte Vorschau in der Google-Buchsuche)
- ↑ a b c d Datenblatt Tin(IV) iodide (PDF) bei Strem, abgerufen am 25. Dezember 2012.
- ↑ a b c Datenblatt Tin(IV) iodide, anhydrous, powder, 99.999% trace metals basis bei Sigma-Aldrich, abgerufen am 4. Mai 2022 (PDF).
- ↑ D'Ans-Lax, Taschenbuch für Chemiker und Physiker. Bd. 3 (1998) ISBN 3-540-60035-3, S. 740.
- ↑ Hickling, G. G.: Gravimetric analysis: The synthesis of tin iodide. In: J. Chem. Educ. 67. Jahrgang, Nr. 8, 1990, S. 702–703, doi:10.1021/ed067p702.
- ↑ F. Meller and I. Fankuchen: The crystal structure of tin tetraiodide. In: Acta Crystallographica. 8. Jahrgang, 1955, S. 343–344, doi:10.1107/S0365110X55001035.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 970.
Auf dieser Seite verwendete Medien
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globales Harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS) Piktogramm für gesundheitsgefährdende Stoffe.
Photo of a sample of crystalline tin(IV) iodide, SnI4
Struktur von SnI4
Ball-and-stick model of the unit cell of tin tetraiodide, SnI4. X-ray crystallographic data from F. Meller and I. Fankuchen (1955). "The crystal structure of tin tetraiodide". Acta Crystallographica 8: 343-344. DOI:10.1107/S0365110X55001035.