Vertico-SMI
Das Vertico-SMI ist ein Fluoreszenzmikroskop für die dreidimensionale Aufnahme von Zellen im Nanometerbereich (Super Resolution Mikroskopie). Im Unterschied zu vergleichbaren Ansätzen erfolgt die Markierung mit normalen Fluoreszenzfarbstoffen wie GFP, Cy2/3, Fluorescein, Alexa- und Attofarbstoffen, beruhend auf dem sogenannten Blinking-Phänomen. Es basiert auf zwei Mikroskoptechnologien, welche 1996 entwickelt wurden, der Lokalisationsmikroskopie SPDM und der Strukturierten Beleuchtung SMI. Die effektive optische Auflösung dieses optischen Nanoskopes erreicht 5 nm in 2D und 40 nm in 3D und ist dadurch deutlich besser als die physikalische Auflösungsgrenze von 200 nm, postuliert durch das Gesetz von Abbe 1873.[1]
Konfiguration
„SMI“ steht für eine spezielle Art der laseroptischen Beleuchtung (Spatially Modulated Illumination, Räumlich Strukturierte Beleuchtung) und „Vertico“ für die vertikale Anordnung der Mikroskopachse, die es ermöglicht, fixierte Zellen, aber auch lebende Zellen mit einer dreidimensionalen effektiven optischen Auflösung von 40 Nanometer (1 Nanometer = 1 nm = 10−9 m) zu analysieren.
Grundlagen
Das Mikroskop wurde von Christoph Cremer, Professor für Angewandte Optik und Informationsverarbeitung an der Universität Heidelberg / Institut für Molekulare Biologie entwickelt. Es basiert auf einer Kombination von lichtoptischen Techniken der Lokalisationsmikroskopie (SPDM, Spectral Precision Distance Microscopy) und strukturierter Beleuchtung (SMI, Spatially Modulated Illumination). Eine Besonderheit im Unterschied zu fokussierenden Techniken wie der 4Pi-Mikroskopie sind die Weitfeldaufnahmen, bei denen die ganze Probe gleichzeitig beleuchtet und detektiert wird. Dies ermöglicht ganze Zellen schnell nanoskopisch aufzunehmen. Für 3D-Aufnahmen solcher ganzen Zellen mit typischen Bildfeldern der Größe 20 µm × 20 µm werden nur 2 Minuten benötigt.
Die effektive optische Auflösung dieses optischen Nanoskops hat einen Bereich von 5 nm in 2D und 40 nm in 3D erreicht und liegt daher wesentlich unter der physikalischen Grenze von 200 nm, welche durch das Gesetz von Abbe 1873 als die physikalische Grenze, unterhalb der eine lichtmikroskopische Auflösung theoretisch nicht möglich ist, postuliert worden ist.[1]
Spatially Modulated Illumination (SMI)
Spatially Modulated Illumination (SMI) steht für räumlich strukturierte Beleuchtung. Die SMI-Mikroskopie ist ein lichtoptisches Verfahren des sogenannten Point Spread Function-Engineering. Darunter sind Verfahren zu verstehen, die die Punktbild-Funktion (Point Spread Function, PSF) eines Mikroskops in geeigneter Weise modifizieren, um entweder die optische Auflösung zu erhöhen, die Präzision von Distanzmessungen an punktförmigen, d. h., im Vergleich zur Wellenlänge kleinen fluoreszierenden Objekten zu maximieren oder andere Strukturparameter im Nanometerbereich zu extrahieren.
Beim gegenwärtig am Kirchhoff-Institut für Physik der Universität Heidelberg entwickelten SMI-Mikroskop wird dies dadurch erreicht, dass die Anregungsintensität im Objektraum im Gegensatz zu herkömmlichen Weitfeldfluoreszenz-Mikroskopen nicht homogen ist, sondern durch Verwendung zweier gegenläufiger, interferierender Laserstrahlen in axialer Richtung räumlich präzise moduliert wird. Das Prinzip des räumlich modulierten Wellenfeldes wurde 1993 von Bailey et al. entwickelt. Bei dem Heidelberger SMI Mikroskopieansatz wird das Objekt in hochpräzisen Schritten durch das Wellenfeld bewegt oder es wird das Wellenfeld selbst verschoben (Phase). Daraus resultiert eine Erhöhung der axialen Größen- und Distanzauflösung.
SMI kann mit anderen Super Resolution Mikroskopie Technologien, zum Beispiel mit 3D LIMON oder mit LSI-TIRF als Totalreflexion (TIRF) Interferometer mit räumlich strukturierter Beleuchtung, kombiniert werden. In der Kombination mit TIRF können lichtoptische Bilder von autofluoreszierenden (selbst leuchtenden) Strukturen im menschlichen Augengewebe mit bislang unerreichter optischer Auflösung unter Verwendung von drei verschiedenen Anregungswellenlängen (488, 568 und 647 nm) aufgenommen werden. Die optische Auflösung beträgt 100 nm bei Untersuchungen der Makuladegeneration von erkranktem menschlichem Augengewebe.[2]
Spectral Precision Distance Microscopy (SPDM)
SPDM (Spektrale Präzisions-Distanz-Mikroskopie) ist ein lichtoptisches Verfahren der Fluoreszenzmikroskopie, mit welchem an „optisch isolierte“ Teilchen (z. B. einzelne Moleküle) Positions-, Abstands- und Winkelmessungen weit unterhalb der optischen Beugungsbegrenzung möglich sind. „Optisch isoliert“ bedeutet, dass zu einem bestimmten Zeitpunkt nur ein einziges Teilchen/Molekül in einem durch die konventionelle optische Auflösung festgelegten Gebiet (typischerweise ca. 200–250 nm Durchmesser) registriert wird. Dies ist möglich, wenn die in einem solchen Gebiet befindlichen Teilchen/Moleküle unterschiedliche spektrale Markierungen tragen (z. B. verschiedene Farben haben, oder andere nutzbare Unterschiede in der Lichtemission zeigen).
Die mit SPDM mögliche Strukturauflösung kann angegeben werden durch die kleinste messbare Distanz zwischen zwei in ihrer räumlichen Position bestimmten „punktförmigen“ Teilchen unterschiedlicher spektraler Markierung („Topologische Auflösung“). Simulationsrechnungen haben gezeigt, dass unter geeigneten Annahmen über Lokalisationsgenauigkeit, Teilchendichte etc. die „topologische Auflösung“ einer Raumfrequenz entspricht, die einer stark erhöhten optischen Auflösung im Sinne der klassischen Definition äquivalent ist.
Es handelt sich um eine Lokalisationsmikroskopie, wodurch eine effektive optische Auflösung möglich gemacht wird, die um ein Vielfaches besser ist als die konventionelle optische Auflösung (ca. 200–250 nm), gegeben durch die Halbwertsbreite des Hauptmaximums der effektiven Punktbildfunktion. Durch geeignete laseroptische Präzisionsverfahren werden Positionen und Distanzen erheblich kleiner als die Halbwertsbreite der Punktbildfunktion zwischen Zielobjekten verschiedener spektraler Signatur nanometergenau vermessen. Ein wichtiges Einsatzgebiet ist die Genomforschung (Studium der funktionellen Organisation des Genoms). Ein weiteres wesentliches Anwendungsgebiet ist die Membranstrukturforschung.
SPDMphymod „Blinkende Farbstoffe“ statt photoschaltbarer Moleküle
Cremers Arbeitsgruppe fand 2008 heraus, dass die Super Resolution Mikroskopie unter bestimmten photophysikalischen Bedingungen auch für viele „ganz gewöhnliche“ Farbstoffmoleküle wie GFP oder Alexa-Farbstoffe realisiert werden kann. Dadurch können in derselben Spektralfarbe leuchtende Moleküle eingesetzt werden (aber mit verschiedener spektraler Signatur aufgrund von „Blink“-Eigenschaften). Durch die Kombination vieler tausender Einzelaufnahmen derselben Zelle werden mithilfe von laseroptischen Präzisionsmessungen „Lokalisationsbilder“ mit wesentlich verbesserter optischer Auflösung gewonnen.
Dies erweitert die Anwendbarkeit der SPDM-Methode auf zahlreiche Gebiete der biophysikalischen, zellbiologischen und medizinischen Forschung.[3]
- Super Resolution Mikroskopie - Lokalisationsmikroskopie
LIMON: 3D Super Resolution Mikroskopie
LIMON (Light MicrOscopical nanosizing microscopy) wurde 2001 an der Universität Heidelberg entwickelt und kombiniert die beiden Methoden Lokalisationsmikroskopie und Strukturierte Beleuchtung zur 3D Super Resolution Mikroskopie.
Die Vorgehensweise ist folgende: zuerst werden SMI-Aufnahmen gemacht und dann der SPDM-Vorgang durchgeführt. Der SMI-Prozess bestimmt die Mitte der Teilchen und ihre Ausbreitung in Richtung der mikroskopischen Achse. Während die Mitte der Partikel/Moleküle mit einer Genauigkeit von 1–2 nm bestimmt werden kann, kann die Ausbreitung in diesem Punkt bis zu einem axialen Durchmesser von ca. 30–40 nm ermittelt werden. Anschließend wird die laterale Position der einzelnen Partikel/Moleküle mit SPDM mit einer Genauigkeit von wenigen Nanometern bestimmt. Derzeit erreicht SPDM 16 Aufnahmen pro Sekunde (in Abhängigkeit von der Kamera) mit einer effektiven Auflösung von 5 nm in 2D (Objektebene); etwa 2000 solcher Aufnahmen werden mit SMI-Daten kombiniert, um ein dreidimensionales Bild der höchstmöglichen Auflösung zu erreichen (effektive optische 3D Auflösung ca. 40–50 nm).[4]
Durch diese Zweifarben-Kolokalsiations 3D Super Resolution Mikroskopie wurde die räumlichen Anordnung der beiden bei Brustkrebs aktiven Gene Her2/neu und HER3 mit einer Genauigkeit von etwa 25 nm bestimmt, sowie ihre für die Krebsentstehung vermutlich relevante Clusterbildung auf Einzelmolekülebene analysiert.[5]
Auch Biomolekulare Maschinen, hochkomplexe Nanostrukturen, die in den Körperzellen grundlegende Funktionen erfüllen, können mit der 3D Super Resolution Mikroskopie LIMON in ihrer biologisch relevanten Zusammensetzung untersucht werden. Einzelne Proteine oder Nukleinsäuren, die im 3D-Molekülkomplex sogenannter Biomolekularer Maschinen versteckt sind, können durch variable Markierung sichtbar gemacht werden, ohne den Komplex zu zerstören.
Einzelnachweise
- ↑ a b Jürgen Reymann, David Baddeley, Manuel Gunkel, Paul Lemmer, Werner Stadter, Thibaud Jegou, Karsten Rippe, Christoph Cremer, Udo Birk: High-precision structural analysis of subnuclear complexes in fixed and live cells via spatially modulated illumination (SMI) microscopy. In: Chromosome Research. Band 16, Nr. 3, Mai 2008, S. 367–382, doi:10.1007/s10577-008-1238-2, PMID 18461478.
- ↑ G Best, R Amberger, D Baddeley, T Ach, S Dithmar, R Heintzmann, C Cremer: Structured illumination microscopy of autofluorescent aggregations in human tissue. In: Micron, 42, 2011, S. 330–335
- ↑ Manuel Gunkel, Fabian Erdel, Karsten Rippe, Paul Lemmer, Rainer Kaufmann, Christoph Hörmann, Roman Amberger, Christoph Cremer: Dual color localization microscopy of cellular nanostructures. In: Biotechnology Journal. Band 4, Nr. 6, 2009, ISSN 1860-6768, S. 927–938, doi:10.1002/biot.200900005.
- ↑ D Baddeley, C Batram, Y Weiland, C Cremer, UJ. Birk: Nanostructure analysis using Spatially Modulated Illumination microscopy. In: Nature Protocols, 2007, 2:, S. 2640–2646
- ↑ Rainer Kaufmann, Patrick Müller, Georg Hildenbrand, Michael Hausmann, Christoph Cremer: Analysis of Her2/neu membrane protein clusters in different types of breast cancer cells using localization microscopy. In: Journal of Microscopy, 2010, doi:10.1111/j.1365-2818.2010.03436.x.
Weblinks
- „Blinkende Farbstoffe“. Ruperto Carola, Forschungszeitschrift der Universität Heidelberg
- Publikationsliste zur Lichtoptischen Nanoskopie
- Heidelberger Innovationsforum 2009: Schnellstes Lichtmikroskop der Welt zur besten Geschäftsidee gekürt
- Pressemitteilung der Universität Heidelberg
- GFP Superresolution (PDF; 330 kB)
Auf dieser Seite verwendete Medien
Autor/Urheber: Andy Nestl, Lizenz: CC BY-SA 3.0
First description of 50 nm optical resolution of cellular structures in label-free cells:
Interestingly SPDM revealed cellular objects not detectable under conventional light microscopy
Christoph Cremer, emeritus at Heidelberg university [1]
Comprehensive studies published in Micron, 2010: The paper describes for the first time that optical resolution of cellular structures in the lamda/10 range (about 50 nm) can be achieved even in label-free cells using the localization microscopy SPDM (Spectral Precision Distance/Position Determination Microscopy).
Beside a substantial resolution improvement of autofluorescent structures, SPDM revealed cellular objects with are not detectable under conventional fluorescence imaging conditions.
Rainer Kaufmann, Patrick Müller, Michael Hausmann, Christoph Cremer: Imaging label-free intracellular structures by localisation microscopy. Micron (2010), doi:10.1016/j.micron.2010.03.06Autor/Urheber: Andy Nestl, Lizenz: CC BY-SA 3.0
Superresolution Microscopy/ Optical nanoscopy using SPDMphymod as a new localization microscopy technique for standard fluorescent dyes
SPDMphymod image of protein distribution in a human cancer cell. Enlarged inserts above and below: Positions of single fluorescent molecules in Gaussian intensity shape of 5 nm standard deviation. Typical distance measurements in the 15 nm range are highlighted
Fundamental to SPDMphymod are blinking phenomena (flashes of fluorescence), induced by reversible bleaches (metastable dark states). Individual molecules of the same spectral emission color can be detected. Counting individual molecules up to a density of 1000/µm2 – at present, this is possible in an area of up to 5000 µm2.
Christoph Cremer, emeritus at Heidelberg university [1] Basic publications:
Lemmer P, Gunkel M, Baddeley D, Kaufmann R, Urich A, Weiland Y, Reymann J, Müller P, Hausmann M, Cremer C: SPDM – Light Microscopy with Single Molecule Resolution at the Nanoscale. In: Applied Physics B 2008; 93: 1–12
Manuel Gunkel, Fabian Erdel, Karsten Rippe, Paul Lemmer, Rainer Kaufmann, Christoph Hörmann, Roman Amberger and Christoph Cremer: Dual color localization microscopy of cellular nanostructures. In: Biotechnology Journal, 2009, 4, 927-938. ISSN 1860-6768Autor/Urheber: Andy Nestl, Lizenz: CC BY-SA 3.0
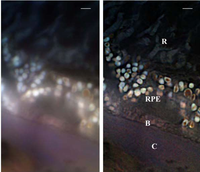
Investigation of AMD, macular degeneration a medical condition which usually affects older adults and results in a loss of vision in the center of the visual field (the macula) because of damage to the retina macular degeneration.
Sections from human eye tissue were analyzed with Structured Illumination Microscopy (SMI) / Optical nanoscopy using a specially designed Super Resolution Microscope setup: LSI-TIRF as a total internal reflection interferometer with laterally structured illumination. This SMI technique allowed to acquire light-optical images of autofluorophore distributions in the tissue with previously unmatched optical resolution. Use of three different excitation wavelengths (488, 568 and 647 nm), enables to gather spectral information about the autofluorescence signal.
Detailed Image description: Overview image. The SMI image (right) shows more details and less out of focus light than the widefield image (left). The Bruch membrane (B) is located between the choroid (C) and the retinal pigment epithelium (RPE). On the top of the image endings of retinal rod cells (R) can be seen. The scale bar is 2�m.
Reference: Best G, Amberger R, Baddeley D, Ach T, Dithmar S, Heintzmann R and Cremer C (2011). Structured illumination microscopy of autofluorescent aggregations in human tissue. Micron, 42, 330-335.Autor/Urheber: Andy Nestl, Lizenz: CC BY-SA 3.0
GFP superresolution, optical nanoscopy ( Christoph Cremer, emeritus at Heidelberg university [1])
View of a nucleus of a bone cancer cell: using normal high resolution fluorescence microscopy, it is not possible to distinguish details of its structure (image on the left). Using the two Color Localization Microscopy 2CLM (image on the right) it is possible to localize 70,000 histone molecules (red: RFP-H2A) and 50,000 chromatin remodeling proteins (green: GPF-Snf2H) in a field of view of 470 µm2 with an optical depth of 600 nm. Common fluorescence markers were used.
2CLM is the only optical nanoscopy method that allows position based co-localization of single molecules at high density in a wide field of view using conventional fluorescent proteins such as GFP, YFP, RFP, or other conventional fluorochromes.
Due to its high optical single molecule resolution, 2CLM allows significantly more precise analyses of potential protein interactions than FRET-(Fluorescence Resonance Energy Transfer) technology, which is at present the preferred method for such investigations. This is of particular significance in studies of biomolecular machines (BMMs) within cells: Single BMMS can be analysed, including the number of molecules of a given type; distances between proteins in these BMMs often are substantially greater than those that can be analyzed by FRET (restricted to a maximum distance of only a few nm).
Possible to use conventional, well established and inexpensive fluorescent dyes, from the GFP group, and its dye variants, to the well-known Alexa and fluorescein dyes. Fundamental to SPDMphymod are blinking phenomena (flashes of fluorescence), induced by reversible bleaches (metastable dark states). Individual molecules of the same spectral emission color can be detected.
Publikation: Manuel Gunkel, Fabian Erdel, Karsten Rippe, Paul Lemmer, Rainer Kaufmann, Christoph Hörmann, Roman Amberger and Christoph Cremer: Dual color localization microscopy of cellular nanostructures. In: Biotechnology Journal, 2009, 4, 927-938. ISSN 1860-6768Autor/Urheber: Andy Nestl, Lizenz: CC BY-SA 3.0
3D Dual Color Super Resolution Microscopy by combining localization microscopy SPDM with spatially modulated illumination SMI / Optical nanoscopy / Christoph Cremer emeritus at Heidelberg university [1], [2]
3D reconstruction of dual color acquistion of Her2/neu and Her 3. A) conventional wide-field fluorescence image of an AG11132 mammary epithelial cells. Her3 is labelled with Alexa488 (green) and Her2/neu with Alexa568 (red). B) magnified image of a small area of A. C) localization microscopy SPDM of the same region of interest as in B. D) and E) show a 3D reconstruction of the protein clusters using the combination of SPDM and SMI microscopy (LIMON technology). Scale bars in D) and E) are 500 nm in each direction.
By combining SPDMphymod with SMI (both invented in Christoph Cremer´s lab in 1996) a 3D dual colour reconstruction of the spatial arrangements of Her2/neu and Her3 clusters was achieved. The positions in all three directions of the protein clusters could be determined with an accuracy of about 25 nm.
Her2/neu and Her3 are tyrosine kinase receptors and their overexpression is related to certain types breast cancer. The paper analyses the Her2 distribution pattern in breast cancer cells and counts the clusters (20 637 clusters with a mean diameter of 67 nm) with a specifically developed clusters finding algorithm for super resolution microscopy. This methods could help for the exploration of the resistance mechanism in Trastuzumab/Herceptin treatment.
Publication: Rainer Kaufmann, Patrick Müller, Georg Hildenbrand, Michael Hausmann & Christoph Cremer [3], [4] : Analysis of Her2/neu membrane protein clusters in different types of breast cancer cells using localization microscopy, Journal of Microscopy 2010, doi: 10.1111/j.1365-2818.2010.03436.x