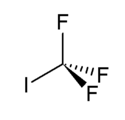
Trifluoriodmethan
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Trifluoriodmethan | |||||||||||||||
| Summenformel | CF3I | |||||||||||||||
| Kurzbeschreibung | farbloses Gas[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 195,88 g·mol−1 | |||||||||||||||
| Aggregatzustand | gasförmig[1] | |||||||||||||||
| Dichte | 2,3608 g·cm−3 (−42 °C)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | −22,5 °C[1] | |||||||||||||||
| Brechungsindex | 1,3790 (−32 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 | −587,8 kJ/mol[4] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Trifluoriodmethan ist eine chemische Verbindung aus der Gruppe der Halogenkohlenwasserstoffe.
Gewinnung und Darstellung
Trifluoriodmethan kann durch Reaktion von Natriumtrifluoracetat oder Silbertrifluoracetat mit Iod gewonnen werden.[5]
Eigenschaften
Trifluoriodmethan ist ein farbloses, nicht brennbares, lichtempfindliches Gas.[1]
Verwendung
Trifluoriodmethan liefert beim Erhitzen und beim Bestrahlen mit UV-Licht freie CF3-Radikale und eignet sich daher zur Synthese zahlreicher Verbindungen des Typus CF3(CF2)n-X sowie organometallischer und organometalloider Verbindungen.[5] Es hat ein Ozonabbaupotenzial von 0,01 bis 0,02.[1]
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu Trifluoriodmethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-500.
- ↑ Eintrag zu Trifluoroiodomethane im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-19.
- ↑ a b Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 222.
Auf dieser Seite verwendete Medien
Created using: ACD/ChemSketch
Globales Harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS) Piktogramm für gesundheitsgefährdende Stoffe.
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for gases under pressure