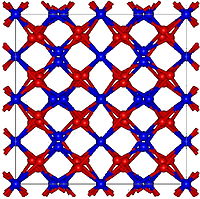
Thallium(III)-oxid
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| _ Tl3+ _ O2− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Thallium(III)-oxid | |||||||||||||||
| Andere Namen | Dithalliumtrioxid | |||||||||||||||
| Verhältnisformel | Tl2O3 | |||||||||||||||
| Kurzbeschreibung | brauner bis schwarzer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 456,76 g·mol−1 | |||||||||||||||
| Aggregatzustand | fest | |||||||||||||||
| Dichte | 10,11 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | 717 °C[1] | |||||||||||||||
| Siedepunkt | 875 °C[2] | |||||||||||||||
| Löslichkeit | nahezu unlöslich in Wasser[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Thallium(III)-oxid (Tl2O3) ist eine anorganische chemische Verbindung aus der Gruppe der Oxide des Thalliums. Es handelt sich hierbei um einen braunen bis schwarzen Feststoff. Wie alle anderen Thalliumverbindungen auch ist Thallium(III)-oxid extrem giftig.
Vorkommen
Thallium(III)-oxid kommt natürlich in Form des sehr seltenen Minerals Avicennit vor.[5]
Gewinnung und Darstellung

Thallium(III)-oxid kann durch Reaktion von Thallium(I)-nitrat mit Kalilauge und Chlor gewonnen werden, wobei dabei das rotbraune Thallium(III)-oxidhydrat mit der ungefähren Zusammensetzung Tl2O3·1,47 H2O entsteht, welches durch Vakuumexsikkation in die wasserfreie Form überführt werden kann.[6]
Wenn reines Thallium der Luft ausgesetzt wird, bildet sich ein dünner Film von Thallium(III)-oxid durch Oxidation.[7]
Eigenschaften
Thallium(III)-oxid ist ein brauner bis schwarzer (je nach Darstellungsbedingungen) Feststoff, welcher in Wasser unlöslich ist. Er besitzt eine Defektstruktur vom Calciumfluorid-Typ[8] (a = 10,543 Å).[1] Über 500 °C und 65 kBar nimmt es eine Kristallstruktur vom Korund-Typ an.[6] Im Gegensatz zum „isoelektronischen“ Blei(IV)-oxid ist Thallium(III)-oxid ein nur mäßiges Oxidationsmittel und zerfällt erst bei hoher Temperatur zu Thallium(I)-oxid und Sauerstoff.
Weblinks
Einzelnachweise
- ↑ a b c d Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 884.
- ↑ a b EPA: Toxicological Review of Thallium and Compounds (PDF; 1,1 MB)
- ↑ a b c Datenblatt Thallium(III) oxide, 99.99% trace metals basis bei Sigma-Aldrich, abgerufen am 1. Dezember 2019 (PDF).
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag thallium compounds, with the exception of those specified elsewhere in this Annex im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Mineralienatlas:Avicennit
- ↑ a b Anthony John Downs: Chemistry of aluminium, gallium, indium, and thallium, S. 286; ISBN 978-0-7514-0103-5
- ↑ Thallium: Unique Applications and Risks - Element 81 Explained. Abgerufen am 1. Juni 2024.
- ↑ Peter Paetzold; Chemie, S. 205; ISBN 978-3-11-020268-7
Auf dieser Seite verwendete Medien
(c) Materialscientist in der Wikipedia auf Englisch, CC BY-SA 3.0
Room-temperature (cubic) structure of Tl2O3 (or Mn2O3) viewed along a cubic axis. Red atoms are oxygens
Autor/Urheber: Dschwen, Lizenz: CC BY 2.5
Heavily corroded thallium metal rod. Length ca. 5cm. Image taken by User:Dschwen on January 5th 2006.
Globales Harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS) Piktogramm für gesundheitsgefährdende Stoffe.
Global harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS): Piktogramm für giftige / toxische Chemikalien
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances