Thallium(I)-oxid
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
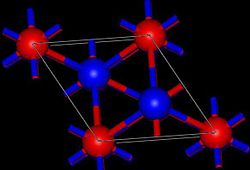
| _ Tl+ _ O2− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Thallium(I)-oxid | |||||||||||||||
| Andere Namen | Dithalliummonoxid | |||||||||||||||
| Verhältnisformel | Tl2O | |||||||||||||||
| Kurzbeschreibung | schwarzer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 424,77 g·mol−1 | |||||||||||||||
| Aggregatzustand | fest[1] | |||||||||||||||
| Dichte | 9,52 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | 1080 °C[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Thallium(I)-oxid ist eine anorganische chemische Verbindung des Thalliums aus der Gruppe der Oxide.
Gewinnung und Darstellung
Thallium(I)-oxid kann durch Erhitzung von Thallium(I)-hydroxid auf über 100 °C oder Thallium(III)-oxid auf über 700 °C in Abwesenheit von Luft dargestellt werden.[5]
Eigenschaften
Thallium(I)-oxid ist ein sehr hygroskopischer schwarzer Feststoff, der leicht löslich in Wasser unter Bildung von Thallium(I)-hydroxid ist.[1] Er besitzt eine Kristallstruktur, die als dreifache polytype Form vom Anti-Cadmium(II)-iodid-Typ aufzufassen ist.[6] Es ist eine trigonale Kristallstruktur mit der Raumgruppe R3m (Raumgruppen-Nr. 166).[1]
Einzelnachweise
- ↑ a b c d e f Jean D’Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. Springer, 1997, ISBN 3-540-60035-3, S. 776 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ David R. Lide: CRC Handbook of Chemistry and Physics. CRC Press, 2012, ISBN 1-4398-8049-2, S. 4–94 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Eintrag zu Thalliumverbindungen, anorganisch, löslich in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. November 2013. (JavaScript erforderlich)
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag Thalliumverbindungen mit Ausnahme der namentlich in diesem Anhang bezeichneten im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 14. November 2022. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Cameron Jones, Andreas Stasch: The Chemistry of the Group 13 Metals in the +1 Oxidation State. In: Simon Aldridge, Anthony J. Downs (Hrsg.): The Group 13 Metals Aluminium, Gallium, Indium and Thallium: Chemical Patterns and Peculiarities. John Wiley & Sons, 2011, ISBN 0-470-97668-3, S. 285–341, hier S. 325 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ H. Sabrowsky: Zur Darstellung und Kristallstruktur von Tl2O. In: Zeitschrift für anorganische und allgemeine Chemie. Bd. 381, Nr. 3, 1971, S. 266–279, doi:10.1002/zaac.19713810305
Auf dieser Seite verwendete Medien
Global harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS): Piktogramm für giftige / toxische Chemikalien
Globales Harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS) Piktogramm für gesundheitsgefährdende Stoffe.
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances
(c) Materialscientist, CC BY-SA 3.0
Room-temperature structure of Tl2O viewed along the high-symmetry c axis. Red atoms are oxygens