Stickstoff
| Eigenschaften | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemein | ||||||||||||||||
| Name, Symbol, Ordnungszahl | Stickstoff, N, 7 | |||||||||||||||
| Elementkategorie | Nichtmetalle | |||||||||||||||
| Gruppe, Periode, Block | 15, 2, p | |||||||||||||||
| Aussehen | Farbloses Gas | |||||||||||||||
| CAS-Nummer | ||||||||||||||||
| EG-Nummer | 231-783-9 | |||||||||||||||
| ECHA-InfoCard | 100.028.895 | |||||||||||||||
| ATC-Code | V03AN04 | |||||||||||||||
| Massenanteil an der Erdhülle | 0,03 % (17. Rang)[1] | |||||||||||||||
| Atomar[2] | ||||||||||||||||
| Atommasse | 14,0067 (14,00643 – 14,00728)[3][4] u | |||||||||||||||
| Atomradius (berechnet) | 65 (56) pm | |||||||||||||||
| Kovalenter Radius | 71 pm | |||||||||||||||
| Van-der-Waals-Radius | 155 pm | |||||||||||||||
| Elektronenkonfiguration | [He] 2s2 2p3 | |||||||||||||||
| 1. Ionisierungsenergie | 14.53413(4) eV[5] ≈ 1402.33 kJ/mol[6] | |||||||||||||||
| 2. Ionisierungsenergie | 29.60125(9) eV[5] ≈ 2856.09 kJ/mol[6] | |||||||||||||||
| 3. Ionisierungsenergie | 47.4453(25) eV[5] ≈ 4577.77 kJ/mol[6] | |||||||||||||||
| 4. Ionisierungsenergie | 77.4735(4) eV[5] ≈ 7475.05 kJ/mol[6] | |||||||||||||||
| 5. Ionisierungsenergie | 97.8901(4) eV[5] ≈ 9444.96 kJ/mol[6] | |||||||||||||||
| Physikalisch[2] | ||||||||||||||||
| Aggregatzustand | gasförmig (N2) | |||||||||||||||
| Modifikationen | 1 | |||||||||||||||
| Kristallstruktur | hexagonal | |||||||||||||||
| Dichte | 1,250 kg/m3[7] bei 273,15 K | |||||||||||||||
| Magnetismus | diamagnetisch (χm = −6,7 · 10−9)[8] | |||||||||||||||
| Schmelzpunkt | 63,05 K (−210,1 °C) | |||||||||||||||
| Siedepunkt | 77,15 K[9] (−196 °C) | |||||||||||||||
| Verdampfungsenthalpie | 5,58 kJ·mol−1[9] | |||||||||||||||
| Schmelzenthalpie | 0,36 kJ·mol−1 | |||||||||||||||
| Schallgeschwindigkeit | 333,6 m·s−1 bei 298,15 K | |||||||||||||||
| Spezifische Wärmekapazität | 1040 J·kg−1·K−1 bei 298 K | |||||||||||||||
| Wärmeleitfähigkeit | 0,02583 W·m−1·K−1 | |||||||||||||||
| Chemisch[2] | ||||||||||||||||
| Oxidationszustände | −3, −2, −1, ±0, +1, +2, +3, +4, +5 | |||||||||||||||
| Elektronegativität | 3,04 (Pauling-Skala) | |||||||||||||||
| Isotope | ||||||||||||||||
| Weitere Isotope siehe Liste der Isotope | ||||||||||||||||
| NMR-Eigenschaften | ||||||||||||||||
| ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Stickstoff (lateinisch Nitrogenium) ist ein chemisches Element mit der Ordnungszahl 7 und dem Symbol N. Im Periodensystem steht es in der fünften Hauptgruppe bzw. der 15. IUPAC-Gruppe oder Stickstoffgruppe sowie der zweiten Periode. Das Symbol N leitet sich von der lateinischen Bezeichnung nitrogenium ab (von altgriechisch νίτρονnítron „Laugensalz“ und -gen, meist als „Salpeterbildner“ übersetzt). Die deutsche Bezeichnung Stickstoff erinnert daran, dass molekularer Stickstoff Flammen durch Verdrängen von Sauerstoff löscht („erstickt“) und dass in reinem Stickstoff Lebewesen ersticken, weil Sauerstoff fehlt. Ältere Bezeichnungen sind Azot oder Azotum, von denen sich weiterhin der Name einiger Stickstoffverbindungen ableitet, Stickgas und Zoogenium.
Elementar tritt Stickstoff in der Regel nur in Form zweiatomiger Moleküle auf (molekularer Stickstoff, auch Distickstoff, Summenformel N2) und ist mit 78 % der Hauptbestandteil der Luft. In der Erdkruste kommt anorganisch gebundener Stickstoff selten vor; von Bedeutung ist er nur in Salpetervorkommen.
Im Laufe der Evolution hat sich ein Stickstoffkreislauf der Ökosysteme ausgebildet: Als Bestandteil von Proteinen und vielen anderen Naturstoffen ist Stickstoff essentiell für Lebewesen, die ihn in einem energieintensiven Prozess (Stickstofffixierung) organisch binden und bioverfügbar machen. Dies geschieht zum Beispiel enzymatisch an einem Eisen-Schwefel-Cluster, welcher ein Kofaktor des Enzyms Nitrogenase ist.
Geschichte

Natürlich vorkommende chemische Verbindungen des Stickstoffs, wie Nitrate und Ammoniumsalze, wurden schon in der Antike und von den Alchimisten verwendet. Beide Verbindungstypen kann man neben ihrem Vorkommen als Mineralien auch aus Exkrementen herstellen. So stellten die Ägypter beispielsweise Ammoniumchlorid (Salmiak) aus Kamelmist her und Salpeter wurde lange Zeit aus dem Boden von Ställen gewonnen. Carl Wilhelm Scheele wies 1771 Stickstoff als Bestandteil der Luft nach – er bezeichnete ihn als „verdorbene Luft“ – und wurde im Jahr 1772 von Daniel Rutherford bestätigt.[10] Antoine de Lavoisier gab dem Gas den Namen azôte (von altgriechisch ἄζωτοςázōtos „das Leben nicht unterstützend, lebensfeindlich“, also „erstickender, das Leben nicht unterhaltender Stoff“).[11] Jean-Antoine Chaptal führte den Namen nitrogène 1790 ein (von lateinisch nitrogenium), nachdem man erkannt hatte, dass der Salpeter und die Salpetersäure Stickstoff-Verbindungen sind.[12] Daher stammt die übliche Übersetzung „Salpeterbildner“ (nitrogenium ist abgeleitet von altgriechisch νίτρονnítron „Laugensalz“, das in der Antike verschiedene Salze im modernen Sinn bezeichnete – vergleiche die anfänglichen Ausführungen zur Geschichte des Natriums –, und -gen, gemeinsam „[Laugen-]Salzbildner“).[11] Reiner Ammoniak wurde erstmals im Jahr 1774 von Joseph Priestley dargestellt.[13] Dass Luft Sauerstoff und Stickstoff in einem konstanten Verhältnis von etwa 1:4 enthält hatte Henry Cavendish 1783[14] erkannt.
Die Bedeutung von Stickstoff in der Biologie wurde zu diesem Zeitpunkt nur unzureichend erkannt. 1786 wies Claude Louis Berthollet Stickstoff als wesentlichen Bestandteil tierischer Substanzen nach. In seinem grundlegenden Werk Traité élémentaire de chimie gab Antoine Lavoisier 1789 eine Übersicht über die damals bekannten Pflanzenstoffe. Auffällig ist dabei die geringe Beachtung stickstoffhaltiger Substanzen, was die damalige Auffassung widerspiegelt, dass solche Verbindungen vor allem in Tieren vorkommen. Teilweise wurde ihr Vorkommen sogar als Unterscheidungsmerkmal zwischen tierischen und pflanzlichen Stoffen angesehen. Im gleichen Jahr versuchte Antoine François de Fourcroy, tierische Stoffe nach ihrem Stickstoffgehalt zu klassifizieren. Dabei hob er insbesondere die Eiweißstoffe (matières albumineuses) hervor. Obwohl es ihm zugleich gelang, eiweißähnliche Substanzen auch in Pflanzen nachzuweisen, blieb die Vorstellung eines grundsätzlichen Unterschieds zwischen tierischer und pflanzlicher Materie zunächst bestehen. In diesem Zusammenhang sprach man sogar von „animalischer Materie“ in Pflanzen. Erst allmählich setzte sich im Verlauf des späten 18. und frühen 19. Jahrhunderts die Erkenntnis durch, dass Pflanzen allgemein ebenfalls Stickstoff enthalten. Gleichzeitig wurden spezifische pflanzliche Stickstoffverbindungen entdeckt, darunter das Chlorophyll, dessen Untersuchung ebenfalls auf Berthollet zurückgeht, sowie das Morphin, das 1804 von Friedrich Sertürner isoliert wurde. Trotz dieser Fortschritte dauerte es noch mehr als ein halbes Jahrhundert, bis die grundlegende Bedeutung stickstoffhaltiger Verbindungen vollständig erkannt wurde. Erst in der Mitte des 19. Jahrhunderts wurde klar, dass eiweißartige Stoffe und damit Stickstoff selbst unverzichtbare Bestandteile der Zellen sind.[15][16]
So gelang Friedrich Wöhler 1828 mit der Synthese der schon 1729 von Herman Boerhaave aus tierischem Urin isolierten Stickstoffverbindung Harnstoff aus Ammoniumcyanat der Beweis, dass eine organische Verbindung aus anorganischen Stoffen hergestellt werden kann. Dies widerlegte die bis dahin verbreitete Vorstellung einer besonderen „Lebenskraft“ in der organischen Chemie.[17][18]
Jean-Baptiste Boussingault bewies ab 1836 durch die weltweit ersten Feldversuche mit exakter Messung der Pflanzen- und Bodenzusammensetzung die essenzielle Rolle der Stickstoffaufnahme über den Boden sowie die Sonderstellung der Leguminosen bei der Stickstofffixierung aus der Luft und schuf damit die experimentelle Basis für die moderne Düngung.[19]
Nachdem Justus von Liebig 1840 in seiner Schrift Die organische Chemie in ihrer Anwendung auf Agricultur und Physiologie zunächst die (irrtümliche) Auffassung vertrat, Pflanzen könnten ihren Stickstoffbedarf rein aus der Atmosphäre decken, widerlegten John Bennet Lawes und Joseph Henry Gilbert dies ab 1843 und auch Boussingault bis 1860 durch Feldversuche. Erst 1862 in der 7. Auflage seines Hauptwerks revidierte Liebig seine Position und erkannte die Notwendigkeit der Stickstoffzufuhr über den Boden an, was die Nachfrage nach stickstoffhaltigem Dünger massiv steigerte.[20][21][22][23][24] 1888 beobachteten Hermann Hellriegel und Hermann Wilfarth an der landwirtschaftlichen Versuchsstation in Bernburg die Bildung von Wurzelknöllchen nach Infektion mit Bakterien und maßen die gleichzeitige Reduktion von Stickstoff aus der Luft zu Ammoniak, der an die Pflanze abgegeben wird. Martinus Willem Beijerinck konnte noch im gleichen Jahr in Delft nach Kenntnisnahme der Hellriegel’schen Versuche das erste Bakterium Bacillus radicicola isolieren, das die Knöllchenbildung verursacht.[25] Zwischen 1889 und 1895 klärte Sergei Nikolajewitsch Winogradski zentrale mikrobiologische Prozesse des Stickstoffkreislaufs auf, bei denen er auch weitere nitrifizierende Bakterien identifizierte und isolierte.[26][25]
Ab der Mitte des 19. Jahrhunderts spielte Stickstoff auch eine zentrale Rolle in der Entwicklung moderner Explosivstoffe. So gelang 1846 Christian Friedrich Schönbein und auch Rudolf Christian Böttger die Herstellung von Schießbaumwolle durch Nitrierung von Cellulose, womit erstmals ein hochenergetischer, stickstoffreicher Sprengstoff verfügbar wurde. Bereits 1847 synthetisierte Ascanio Sobrero Nitroglycerin, dessen technische Nutzbarkeit Alfred Nobel ab 1867 mit der Erfindung des Dynamits erschloss. Ab etwa 1902 folgte mit der industriellen Einführung von Trinitrotoluol (TNT) ein weiterer Meilenstein der Stickstoffchemie, der die militärische und zivile Sprengstofftechnik nachhaltig prägte.[27][28]
Bis zum Beginn des 20. Jahrhunderts war natürlicher Salpeter die einzige großtechnisch verfügbare Quelle von Stickstoffverbindungen.[29] Bereits 1860 führten Louis Joseph Frederic Margueritte und Alfred Lalouel Sourdeval erste technische Versuche zur Bindung von Luftstickstoff durch, indem sie Baryt in Gegenwart von Kohle zu Bariumcyanid umsetzten, das sich mit Wasserdampf zu Ammoniak zersetzen ließ.[30] Einen wichtigen Zwischenschritt bildete die Entdeckung der elektrischen Carbidherstellung die 1892 Thomas Willson in den USA mit der ersten großtechnischen Darstellung von Calciumcarbid im elektrischen Ofen gelang, während Henri Moissan im selben Jahr die wissenschaftliche Untersuchung dieses Prozesses veröffentlichte.[31] Bereits 1895 entwickelte Hamilton Castner in den USA ein frühes Cyanamid‑Verfahren, das Calciumcarbid zur Bildung von Calciumcyanamid nutzte und damit ein unmittelbarer Vorläufer des späteren Frank-Caro-Verfahrens war. Eine indirekte Rolle spielte ab 1889 das von Ludwig Mond entwickelte Mond-Verfahren, das durch die Erzeugung nahezu schwefelfreier Kohlenmonoxid‑Ströme zur Weiterentwicklung der industriellen Gaschemie beitrug und damit wichtige Voraussetzungen für spätere Synthesegas‑basierte Verfahren der Stickstoffchemie schuf.[32] Auf dieser Grundlage entwickelten Adolph Frank und Nikodem Caro ab 1898 das Frank-Caro-Verfahren zur Herstellung von Kalkstickstoff, mit dem Luftstickstoff erstmals im industriellen Maßstab in Form von Calciumcyanamid chemisch fixiert werden konnte. Ab 1903 wurde mit dem Birkeland-Eyde-Verfahren (nach Kristian Birkeland und Sam Eyde) ein weiteres Verfahren zur industriellen Stickstofffixierung eingeführt, bei dem Luftstickstoff in einem elektrischen Lichtbogen zu Stickoxiden oxidiert wurde, die anschließend durch Lösung in Wasser zu Salpetersäure umgesetzt wurden. Diese frühen Verfahren wurden jedoch bald durch das ab 1909 technisch realisierte Haber-Bosch-Verfahren (nach Fritz Haber und Carl Bosch) zur Synthese von Ammoniak aus Stickstoff und Wasserstoff verdrängt. Die großtechnische Umsetzung von Ammoniak zu Salpetersäure erfolgte anschließend über das von Wilhelm Ostwald entwickelte katalytische Ostwaldverfahren, das ab 1902 patentiert und ab 1905–1908 industriell etabliert wurde.[33][34]
Seit dem 20. Jahrhundert hat die technische und ökologische Bedeutung des Stickstoffs stark zugenommen. Mit der weltweiten Einführung des Haber‑Bosch‑Verfahrens ab 1913 stieg die Produktion synthetischer Stickstoffdünger kontinuierlich an und wurde zu einem zentralen Faktor der globalen Landwirtschaft und der sogenannten „Grünen Revolution“.[35][36] Gleichzeitig rückten ab den 1970er Jahren die ökologischen Folgen des zunehmenden Eintrags reaktiver Stickstoffverbindungen in den Vordergrund, darunter Eutrophierung, Nitratbelastung des Grundwassers, Versauerung von Böden sowie die Emission des klimawirksamen Gases Distickstoffmonoxid.[37][38] Auch Stickoxide (NOx) aus Verbrennungsprozessen wurden zu einem bedeutenden Luftschadstoff, was zur Entwicklung von Abgasreinigungssystemen wie Dreiwegekatalysatoren und SCR‑Verfahren führte.[39]
In der Erdsystemforschung gilt Stickstoff seit Beginn des 21. Jahrhunderts als eine der am stärksten überschrittenen planetaren Belastungsgrenzen, da der anthropogene Eintrag reaktiver Stickstoffverbindungen inzwischen die natürlichen Fixierungsprozesse übertrifft.[40][41] Parallel dazu wurden neue mikrobiologische Prozesse des Stickstoffkreislaufs entdeckt, darunter die anaerobe Ammoniumoxidation (Anammox, 1995)[42] und die vollständige Ammoniakoxidation durch einzelne Mikroorganismen (Comammox, 2015),[43] die das Verständnis des globalen Stickstoffkreislaufs wesentlich erweitert haben.
Im Zuge der Energiewende gewinnt Ammoniak als potenzieller Wasserstoffträger und CO2‑freier Energieträger seit den 2020er Jahren erneut an Bedeutung.[44] Moderne industrielle Entwicklungen umfassen zudem optimierte Verfahren der Ammoniak‑ und Salpetersäureproduktion sowie neue katalytische Technologien zur Reduktion von Stickoxiden.[45][46]
Vorkommen
Stickstoff in der Luft
Die Lufthülle der Erde besteht zu 78,08 Vol-% (75,53 % Gewichtsanteil) aus molekularem Stickstoff (Distickstoff N2).[47] Sie enthält damit heute etwa 3,8·1018 kg Stickstoff.[48] Nach der Entstehung der Erde war die Konzentration von Stickstoff in der Erdatmosphäre anfangs sehr gering. Die inerte Verbindung sammelte sich jedoch im Verlauf der Entwicklung der Erdatmosphäre aus vulkanischen Aktivitäten an, da andere Verbindungen wie Methan und Wasser sich zersetzen, gebunden wurden beziehungsweise kondensierten oder wie Wasserstoff in den Weltraum entwichen.[49][50][51][52]
Stickstoff als Mineral
In der Natur wurde erstmals kristalliner Stickstoff als Einschluss in Diamant in den Flusssedimenten des Rio São Luís nahe Juína in Brasilien entdeckt. Das in orthorhombischer Struktur kristallisierende Allotrop von Stickstoff (auch δN) wurde von seinen Erstbeschreibern Oliver Tschauner, Oded Navon und Christian Schmidt als Deltanitrogen bezeichnet und von der International Mineralogical Association (IMA) unter der Eingangs-Nr. 2019-067b als eigenständige Mineralart anerkannt.[53][54]
Da Deltanitrogen erst 2019 als Mineral anerkannt wurde, ist es weder in der zuletzt 2009 aktualisierten 9. Auflage der Mineralsystematik nach Hugo Strunz noch in der zuletzt 2018 überarbeiteten Lapis-Systematik nach Stefan Weiß verzeichnet. Auch die vorwiegend im englischen Sprachraum gebräuchliche Systematik der Minerale nach Dana kennt den Deltanitrogen noch nicht.
Die von der Mineraldatenbank „Mindat.org“ weitergeführte Strunz-Klassifikation in der 9. Auflage (auch Strunz-mindat) ordnet Deltanitrogen in die Klasse der „Elemente“ und dort in die Abteilung der „Halbmetalle (Metalloide) und Nichtmetalle“ (englisch Metalloids and Nonmetals; vergleiche auch gleichnamige Abteilung der Strunz-Klassifikation). Eine weitere Eingruppierung in eine bestimmte Unterabteilung bzw. Stroffgruppe fand bisher nicht statt (Stand 2024).[55]
Neben dieser Form kommt Stickstoff auch als Bestandteil einiger Minerale vor. Darin liegt es meist in Form des Ammonium-Ions vor (wie zum Beispiel in Salmiak oder Buddingtonit), das anstelle des ähnlich großen Kaliums in Glimmer oder Tonminerale eingebaut wird. Auch als Nitrid (wie in Roaldit) oder Nitrat (wie in Nitronatrit) ist Stickstoff in Mineralen vorhanden.[56][57]
Stickstoff in der Erde
Der Anteil von Stickstoff in der Erdkruste (Atmo-, Hydro- und Lithosphäre bis zu 16 km Tiefe) beträgt etwa 0,03 %. Es steht damit in der Häufigkeitsliste an 18. Stelle.[48] Die im Vergleich zur Atmosphäre enorme Gesamtmasse der Erde bedeutet, dass sie große Mengen an Stickstoff binden kann und ein Großteil des Stickstoffs im Inneren der Erde gespeichert sind. Aktuelle Schätzungen des Anteils geben zwischen 57 und 61 % für den Erdmantel, 9–14 % für die kontinentale Kruste und 27–30 % für die Atmosphäre an, wobei einige Studien stark abweichende Daten nahelegen.[58][59]
Gleichwohl des geringen Anteils von Stickstoff in der Erdkruste sind stickstoffhaltige Gesteine und Minerale zwar selten, aber weltweit verbreitet. Der Stickstoff in diesen stammt ursprünglich aus organisch gebundenem Stickstoff, der mit Sedimenten assoziiert ist, oder aus Thermalwasser, das eine Mischung aus sedimentären, mantelbezogenen und meteorischen Stickstoffquellen darstellt. Die Stickstoffkonzentrationen in Gesteinen reicht dabei von Konzentrationen (<200 mg N·kg−1) in Graniten bis hin zu ökologisch bedeutsamen Konzentrationen von über 1000 mg N·kg−1 in einigen Sediment- und Metasedimentgesteinen. Auch in ariden und semiariden Regionen angesammelte Nitratablagerungen stellen ein Reservoir für Stickstoff im Boden dar.[57]
In der Ackerkrume (A-Horizont) liegen meist mehr als 95 % des Gesamtstickstoffs als organisch gebundener Stickstoff in lebender Wurzelmasse, abgestorbener Pflanzenmasse, Humusstoffen und Bodenlebewesen vor. Der Rest von weniger als 5 % ist anorganischer Stickstoff in Form von Ammonium oder Nitrat und in sehr geringer Menge in Form von Nitrit. Dieser mineralische Stickstoffgehalt wird im Frühjahr vor der Düngung mit der Nmin-Methode bestimmt. Der Gesamtstickstoffgehalt der Böden ist stark von deren Kohlenstoffgehalt abhängig. Er wird durch Klima, Vegetation, Bodenart, Geländegestalt und Maßnahmen des Landwirts, wie Bodenbearbeitung, beeinflusst.[60]
Stickstoff im Weltall
Stickstoff ist nach der Anzahl der Atome das 6. häufigste Element im Sonnensystem[61]. Im Gegensatz zur Erdatmosphäre und der Atmosphäre des Saturnmondes Titan, dessen Stratosphäre 98,4 % Stickstoff[62] enthält, macht es in der Photosphäre der Sonne nur einen geringen Anteil von etwa 0,09 bis 0,11 % der Gesamtmasse aus.[63][64]
Stickstoff entsteht im Weltall vor allem durch den CNO-Zyklus in Sternen.[65] Vor allem Sterne großer Massen und Wolf-Rayet-Sterne Sterne erzeugen große Mengen davon, die dann bei Supernova-Explosionen den Stickstoff im Weltraum verteilen.[66][67]
Gewinnung und Darstellung
Primär wird Stickstoff heute durch die fraktionierte Destillation verflüssigter Luft in Luftzerlegungsanlagen nach dem Linde-Verfahren mit einer Reinheit von bis zu 99,99999 % gewonnen.[68] Stickstoff mit Verunreinigungen unter 1 ppb erfordert zusätzliche Reinigungsschritte. Für das Entfernen des verbliebenen Sauerstoffs existiert eine biologische Methode unter Verwendung von Reiskeimlingen.

Stickstoff mit einem Reinheitsgrad von ca. 99 % wird wesentlich kostengünstiger durch mehrstufige Adsorption/Desorption an Zeolithen erhalten. Eine weitere Methode zur dezentralen Gewinnung von Stickstoff ist das Membranverfahren. Hierbei wird Druckluft mit einem Druck von 5 bis 13 bar durch eine Kunststoffmembran gepresst. Die Diffusionsgeschwindigkeit von Stickstoff und Argon durch diese Membran ist deutlich langsamer als jene von Sauerstoff, Wasser und Kohlendioxid, dadurch wird der Gasstrom auf der Innenseite der Membran mit Stickstoff angereichert. Durch Anpassung der Durchströmgeschwindigkeit kann die Reinheit des Stickstoffs gesteuert werden (bis 99,995 % bei Kleinstmengen, 99 % bei industriellen Maßstäben.)[68]
Eine etwas altertümliche Methode ist das Binden des Luftsauerstoffs unter Erhitzen an Kohle und das anschließende Auswaschen des entstandenen Kohlenstoffdioxids mit einer Kaliumcarbonatlösung oder mit Wasser unter Druck. Bei begrenztem Luftzutritt verbrennt die Kohle nur zu Kohlenmonoxid, wobei das so gebildete Gemisch von Stickstoff und Kohlenmonoxid als Generatorgas bezeichnet wird.[69] Der Luftsauerstoff kann auch durch das Überleiten der Luft über glühendes Kupfer[69] oder durch eine alkalische Pyrogallol-[70] bzw. Natriumdithionitlösung entfernt werden. Da die Luft außer Stickstoff und Sauerstoff noch eine geringe Menge an Edelgasen enthält, erhält man aus ihr keinen reinen Stickstoff, sondern ein edelgashaltiges Gemisch.[69]
Im Labor gewinnt man reinen Stickstoff zweckmäßigerweise aus Stickstoffverbindungen. So zum Beispiel durch Erhitzen einer wässrigen Ammoniumnitritlösung oder einer Lösung des Gemisches Ammoniumchlorid/Natriumnitrit auf etwa 70 °C dargestellt werden:[71]
Alternativ ist eine Thermolyse von Natriumazid möglich, die zur Herstellung von spektroskopisch reinem Stickstoff verwendet wird.[71]
Eine weiterhin geeignete Verbindung ist Ammoniak, das durch Einwirkung eines Oxidationsmittels Stickstoff entwickelt. So bildet dieses sich beim Eintropfen einer konzentrierter Ammoniaklösung in einen wässerigen Chlorkalkbrei (CaCl2O + CaCl2 + O) oder durch Reaktion mit Salpetriger Säure.[69]
Gefährlich ist die Darstellung von Stickstoff durch Einleiten von Chlor in wässeriges Ammoniak, da sich bei einem Überschuss von Chlor explosives Stickstofftrichlorid bildet.[72]
Eigenschaften
Physikalische Eigenschaften


| Oxidationszustände von Stickstoff[73] | |
|---|---|
| −3 | NH3, NaNH2, Li3N, HCN, Methylamin |
| −2 | N2H4 |
| −1 | N2H2, Hydroxylamin |
| 0 | N2 |
| +3 | HNO2, NaNO2, Nitromethan |
| +5 | HNO3, NaNO3 |
Molekularer Stickstoff ist ein farb-, geruch- und geschmackloses Gas, welches bei tiefen Temperaturen (−196 °C) zu einer farblosen Flüssigkeit mit einer Dichte von 0,8076 g·cm3 kondensiert. Stickstoff ist in Wasser wenig löslich (23,2 ml Stickstoff in 1 l Wasser bei 0 °C)[69][74] und nicht brennbar. Es ist in Metallschmelzen löslich; so lassen sich beispielsweise 4 % Stickstoff in Eisenschmelzen lösen, was zum Beispiel bei Nitrierstahl genutzt wird.[75] Der kritische Punkt liegt bei: Temperatur 126,19 K (−146,95 °C), Druck 33,9 bar, Dichte 0,314 g/cm3. Der Tripelpunkt liegt bei einer Temperatur von 63,15 K (−210 °C) und einem von Druck 0,125 bar.[76] Der Schmelzpunkt des farblosen festen Stickstoffs liegt bei −209,99 °C. Es liegt in Form einer hexagonal-dichtesten Kugelpackung von N2-Molekülen vor. Unterhalb von −237,54 °C existiert noch eine Form mit kubisch-dichtester Packung. Bei einer Temperatur von −253 °C beträgt die Dichte des festen Stickstoffs 1,0265 g·cm3.[69]
In einer Gasentladungs-Spektralröhre werden bei einem Restdruck von ca. 5–10 mbar die Molekülorbitale des Stickstoffs beim Betrieb mit 1,8 kV Hochspannung, 18 mA Stromstärke und einer Frequenz von 35 kHz zum Leuchten angeregt. Bei der Rekombination der ionisierten Gasmoleküle wird hierbei das charakteristische Farbspektrum abgestrahlt.[77] Dieser Prozess ist mit einem charakteristischen gelben Nachleuchten verbunden, das bei geeigneten Versuchsbedingungen noch bis zu 6 Stunden nach Ausschalten der elektrischen Entladung anhält.[69]
Chemische Eigenschaften
Stickstoff ist das einzige Element der Stickstoffgruppe, das mit sich selbst (p-p)π-Bindungen bildet.[78] Der molekulare Distickstoff N2 ist durch die im Stickstoffmolekül vorhandene stabile Dreifachbindung mit einem Atomabstand von 109,76 pm[69] und der damit verbundenen hohen Bindungsdissoziationsenergie von 945,33 kJ/mol[79] sehr reaktionsträge. Die Erklärung hierfür ist, dass bei der aus einer σ-Bindung und zwei senkrecht zueinander stehenden π-Bindungen bestehende Dreifachbindung die p-Orbitale, die an der Bildung der beiden π-Bindungen beteiligt sind, bei den kleinen Stickstoff-Atomen stark überlappen.[80] Deswegen braucht es in der Regel einen hohen Energieaufwand, um diese Verbindung zu trennen und Stickstoff an andere Elemente zu binden. Hoch ist auch die erforderliche Aktivierungsenergie, die gegebenenfalls durch geeignete Katalysatoren verringert werden kann.[69] Im Gegensatz dazu bildet Stickstoff nur sehr schwache Einfachbindungen. Als mittlere Bindungsenthalpie einer Stickstoff/Stickstoff-Einfachbindung lässt sich ein Wert von 158 kJ/mol angeben.[80]
Stickstoff kann Oxidationszahlen von −3 bis +5 annehmen und zeigt dadurch ein sehr vielseitiges chemisches Verhalten. Der große Unterschied zwischen den Bindungsenergien der N/N-Einfachbindung und der N/N-Dreifachbindung trägt dazu bei, dass in der Stickstoffchemie sehr häufig N2-Moleküle gebildet werden. Die Bildung von Ketten mit N/N-Einfachbindungen findet dagegen so gut wie gar nicht statt. Damit verhält sich Stickstoff vollkommen anders als das Nachbarelement Kohlenstoff, dessen Neigung zur Bildung von C/C-Einfachbindungen ein wesentliches Merkmal der darauf aufbauenden organischen Chemie ist.[80]
Mit einer Elektronegativität von etwa 3,0 besitzt Stickstoff eine relativ hohe Fähigkeit, Elektronen anzuziehen. Deshalb bildet es bevorzugt kovalente Bindungen, besonders mit Nichtmetallen wie Wasserstoff, Sauerstoff oder Kohlenstoff.[81] In der 2s2p3 Elektronenkonfiguration führt die Bildung von drei Kovalenzen zur Oktett-Komplettierung.[82] Beispiele hierfür sind:
- Ammoniak
- Amine
- Hydrazin
- Hydroxylamin
Alle diese Verbindungen haben eine trigonale pyramidale Struktur und ein freies Elektronenpaar. Über dieses freie Elektronenpaar können sie als Nukleophile und als Basen reagieren.[83]
Mit Erdalkalimetallen reagiert Stickstoff relativ leicht und vollständig, dabei mit Lithium sogar bei Raumtemperatur. Auch mit vielen anderen Metallen wie Aluminium, Titan, Vanadium und Chrom reagiert es bei starker Hitze zu Nitriden. Mit Wasserstoff reagiert es unter diesen Bedingungen zu Ammoniak und mit Sauerstoff zu Stickoxiden.[69]
Chemische Reaktionen
Reaktionen des Stickstoffs umfassen insbesondere Prozesse, bei denen Stickstoff in chemische Verbindungen eingebaut wird. Dazu zählen die Nitrierung, bei der eine Nitrogruppe in organische Verbindungen eingeführt wird, sowie die Aminierung, bei der Aminogruppen in Moleküle eingebracht werden. Weitere wichtige Reaktionen sind die Bildung von Ammoniak aus Stickstoff und Wasserstoff, die Umsetzung mit Metallen zu Nitriden sowie die Stickstofffixierung, bei der molekularer Stickstoff in reaktive Verbindungen überführt wird.
Der Begriff Azotierung wird uneinheitlich verwendet und bezeichnet allgemein die Einführung von Stickstoff in eine Verbindung. In der technischen Chemie wird darunter häufig die Umsetzung von Calciumcarbid mit Stickstoff zu Calciumcyanamid (Kalkstickstoff) verstanden, welche ein typisches Beispiel für eine Azotierung darstellt:
Davon zu unterscheiden ist die Diazotierung, bei der primäre aromatische Amine mit salpetriger Säure zu Diazoniumsalzen umgesetzt werden.
Allotrope
Neben dem beschriebenen Distickstoff N2 bildet Stickstoff mehrere Allotrope, die sich nach der Anzahl Stickstoffatome.
Polymerer Stickstoff
In einer Veröffentlichung im August 2004 gaben Forscher vom Max-Planck-Institut für Chemie in Mainz bekannt, dass sie unter Drücken von über 110 GPa bei einer Temperatur von über 2000 K eine neue farblose kristalline Form, sogenannter „polymerer Stickstoff“ mit Einfachbindungen erzeugt haben. Diese Modifikation besitzt eine einzigartige kubische Struktur, die sogenannte „cubic gauche“-Struktur.[69]
Durch die hohe Instabilität sind die Einsatzmöglichkeiten begrenzt, man könnte sich polymeren Stickstoff aber zum Beispiel als Sprengstoff oder Energiespeicher vorstellen. Polystickstoff wäre dann mit Abstand der stärkste nicht-nukleare Sprengstoff.[84]
Eine weitere, dem schwarzen Phosphor analoge polymere und als Schwarzer Stickstoff bezeichnete Form des Stickstoffs wurde 2020 beschrieben. Die Struktur enthält zweidimensionale Schichten, in denen die Stickstoffatome über ein einheitliches Zickzack-Muster vernetzt sind. Diese 2D-Schichten ähneln in ihren elektronischen Eigenschaften dem Graphen, so dass das Material für viele technische Anwendungen interessant sein könnte. Die Herstellung erfolgte durch Lasererhitzung von Stickstoff bei einem Druck von 140 GPa in einer Diamantzelle.[85][86]
Hexastickstoff N6
Ein internationales Forschungsteam berichtete 2025 in Nature erstmals über die Synthese von molekularem Hexanitrogen (N6), einem neuen metastabilen Stickstoff-Allotrop. Durch die Reaktion von Chlor oder Brom mit Silberazid (oder Natriumazid) bei Raumtemperatur über die Zwischenstufe Chlorazid und anschließender Stabilisierung in Argon-Matrizen bei 10 Kelvin gelang die Isolierung und Charakterisierung der Verbindung. Bei Raumtemperatur beträgt die Halbwertszeit der Verbindung nur 35,7 Millisekunden.

Spektroskopische Analysen und Berechnungen bestätigten die Struktur. N6 setzt bei Zersetzung ausschließlich Stickstoff frei. Es wurde eine sehr hohe Zersetzungsenthalpie von −774,9 kJ·mol−1 bzw. −9220 kJ·kg−1 abgeschätzt, etwa doppelt so hoch wie die bekannter Sprengstoffe wie TNT oder HMX.[87] Damit ist Hexastickstoff der stärkste nichtnukleare Sprengstoff.[88]

Die Autoren schlagen die Verbindung als möglichen Kandidaten für zukünftige Energiespeichermaterialien vor. Mit Blick auf die eher teure Herstellung, die geringe Temperaturstabilität bei der Handhabung und der schwer beherrschbaren Energiefreisetzung bei der Zersetzung besteht noch ein erheblicher Forschungsbedarf.[89]
Atomarer Stickstoff
Bei Einwirkung elektrischer Glimmentladungen unter vermindertem Druck spalten sich Stickstoffmoleküle teilweise unter Bildung von chemisch sehr reaktiven Stickstoffatomen, was zuerst 1913 von John William Strutt beobachtet wurde. Diese Form bildet mit zahlreichen Metallen (wie zum Beispiel Quecksilber, Zink, Cadmium, Natrium und Magnesium) schon bei Raumtemperatur Nitride, ebenso mit Nichtmetallen wie Phosphor und Schwefel.[69][90]
Weitere Allotrope
Daneben sind mit Tristickstoff N3, Tetrastickstoff N4 (nur im Mikrosekundenbereich existierende Spezies) und Oktastickstoff N8 (nur bei hohem Druck nachgewiesen) weitere allotrope Formen bekannt.[69][91] Weitere Formen wie Bipentazol N10 wurden bisher nur theoretisch vorausgesagt.[92]
Isotope
Es sind insgesamt 17 Isotope zwischen 9N und 25N sowie weitere Isomere des Stickstoffs bekannt. Von diesen sind zwei, die Isotope 14N und 15N, stabil und kommen in der Natur vor. Das Isotop mit dem größeren Anteil an der natürlichen Isotopenzusammensetzung ist 14N mit 99,636 %, 15N hat einen Anteil von 0,364 %.[93] Die langlebigsten instabilen Isotope sind 13N, das mit einer Halbwertszeit von 9,965 Minuten durch β+-Zerfall in 13C übergeht, und 16N, das mit einer Halbwertszeit von 7,13 Sekunden durch β−-Zerfall zu 16O zerfällt. Alle anderen Isotope haben nur kurze Halbwertszeiten von Sekunden oder Millisekunden.[94]
Das 15N-Isotop wurde 1929 von Stefan Meiring Naudé entdeckt[95] und schon wenige Jahre später von A. G. Norman und Chester Hamlin Werkman (1943) in ersten biologischen Feldversuchen eingesetzt.[96] Auch heute noch wird dieses Isotop in ähnlicher Weise für biochemische Untersuchungen des Stickstoffstoffwechsels im Ackerboden oder in Pflanzen, aber auch bei der Umsetzung von Proteinen als Indikator eingesetzt. Der Anteil von 15N am Stickstoff der Atmosphäre beträgt 0,3663 %.[97]
Anreichern kann man 15N wie andere Isotope gasförmiger Stoffe zum Beispiel durch Thermodiffusionstrennung.[98]
Verwendung
Stickstoffverbindungen
Stickstoffverbindungen finden mannigfaltige Anwendungen im Bereich der organischen Chemie und dienen als Düngemittel. Unter diesen ist Ammoniak die technisch bedeutendste, da sie Stickstoff als funktionelle Einheit synthetisch verfügbar macht und so als Ausgangsstoff vieler Stickstoffverbindungen dient.[99]
Viele Sprengstoffe sind Stickstoffverbindungen. Es handelt sich dabei um Nitroverbindungen oder Salpetersäureester. Bei ausreichend vielen Nitrogruppen im Molekül, z. B. bei Pikrinsäure, können die Sauerstoffatome der Nitrogruppen bei Anregung durch Schlag oder Temperaturerhöhung mit den Kohlen- oder Wasserstoffatomen im selben Molekül exotherm reagieren. Somit wird aus dem Feststoff in sehr kurzer Zeit ein Gas hoher Temperatur, das sich mit großer Gewalt ausdehnt. Sprengstoffe befinden sich also in einem metastabilen Zustand. Bei wenigen Nitrogruppen erfolgt lediglich eine schnelle und unvollständige Verbrennung, z. B. bei Nitrocellulose (u. a. Zelluloid).
Seit Beginn des 20. Jahrhunderts kann Luftstickstoff technisch fixiert werden und öffnete damit den Weg in eine umfangreiche Nutzung von Stickstoffverbindungen. Die großtechnische Kalkstickstoff-Synthese begann um 1901, die der Salpetersäure nach dem Birkeland-Eyde-Verfahren um 1905 und die des Ammoniaks (Haber-Bosch-Verfahren) ab 1908.[12]
Stickstoffgas
Die Eigenschaft von Stickstoff, unter moderaten Temperaturen chemisch weitgehend inert zu sein (chemisch nicht zu reagieren), wird vielfältig genutzt. So dient er zur Inertisierung brennbarer Gasgemische und Stäube durch Absenkung der Sauerstoffkonzentration unter die für eine Zündung erforderliche Grenze.[100]
Ein Beispiel ist die Füllung von Flugzeugreifen großer Flugzeuge mit Stickstoff. Das Vermeiden von Sauerstoff (etwa zu 21 % in Luft enthalten) bei etwa 10 bar Druck verhindert, dass Flugzeugreifen unter der großen Hitzeentwicklung (durch Reibung und Walken) bei Landung oder beim Startlauf und insbesondere beim Startabbruch von innen in Brand geraten können oder ein Reifenbrand durch entweichendes Füllgas weiter angefacht wird.[101] Ein vernachlässigbarer günstiger Nebeneffekt ist, dass Stickstoff etwa 2,5 % leichter als Luft ist.
Stickstoff wird auch als Schutzgas beim Schweißen oder der Herstellung von Halbleitern, als Glühlampen-Füllgas, sowie als Treibgas und Packgas eingesetzt.[100][102][103]
Weiterhin ist es als Gas zum Aufschäumen von Sahne und ähnlichem als Lebensmittelzusatzstoff E 941[104] zugelassen. (Siehe Sahnespender) Da Stickstoff im Gegensatz zu CO2 den pH-Wert nicht reduziert, also nicht säuernd wirkt, können auch Milchmix- und Kaffeegetränke ohne sauren Geschmack geschäumt werden.[105] Auch in Getränkezapfanlagen, wenn auf Grund von baulichen Umständen (langer Leitungsweg, großer Höhenunterschied) ein hoher Zapfdruck notwendig ist, wird Stickstoff hier zusammen mit Kohlenstoffdioxid als Mischgas verwendet.[106][107] Da sich Stickstoff nicht im Getränk löst, kann auch bei höheren Drücken ohne zu viel Schaumbildung bzw. Aufcarbonisierung gezapft werden.[108] Stickstoff hat bei gleichem erhöhten Druck eine geringere Löslichkeit in – stets wasserbasierten – Getränken als Kohlenstoffdioxid. Durch Entspannen beim Zapfen werden dadurch kleinere Schaumbläschen erreicht.[109]

In Gasentladungsröhren diente früher Stickstoff zur Erzeugung von goldgelben Licht.[110] Heute sind sie nur noch selten für didaktische Zwecke im Einsatz.[111] Eine Spezialanwendung sind Gasmoleküllaser im UV-Bereich, die als laseraktives Medium reinen Stickstoff verwenden.[112]
Der US-amerikanische Bundesstaat Oklahoma hat im April 2015 Stickstoffgas zur Exekution der Todesstrafe durch Ersticken gesetzlich zugelassen.[113]
Auch in Alabama und Mississippi ist es zugelassen.[114] Im Januar 2024 wurde auf diese Weise erstmals ein Mensch in Alabama hingerichtet. Im Gegensatz zu Behauptungen der Behörden, dies sei „vielleicht die humanste Hinrichtungsmethode“, berichteten Zeugen von einem mehrere Minuten andauernden, qualvollen Todeskampf.[115] Siehe auch Stickstoffhypoxie.

In den Handel kommt Stickstoffgas für industrielle und andere Anwendungen (zum Beispiel in der Medizin und dem Tauchen) in Gasflaschen (Bomben) unter einem Druck von 200-300 bar. Diese müssen in Europa seit 2006 mit einer schwarzen Flaschenschulter für Stickstoff gekennzeichnet sein.[69][116]
Flüssigstickstoff

Aufgrund des niedrigen Siedepunkts wird flüssiger Stickstoff als Kältemedium in der Kryotechnik eingesetzt. Der Stickstoff entzieht dabei dem Kühlgut seine Verdampfungsenthalpie und hält dieses solange kalt, bis er verdampft ist. Gegenüber flüssigem Sauerstoff, der bei −183 °C (90 K) siedet, ist der Siedepunkt von flüssigem Stickstoff um weitere 13 K niedriger, er siedet bei −196 °C (77 K) und bringt Luftsauerstoff und andere Gase zur Kondensation, die auf diese Weise getrennt werden können.
Flüssiger Stickstoff (Dichte 0,8085 kg/L bei −195,8 °C)[12] wird unter anderem dazu verwendet, bei Hochtemperatursupraleitern den supraleitenden Zustand zu erzeugen. Er wird auch zur Lagerung biologischer und medizinischer Proben, Eizellen und Sperma, sowie zum Schockfrieren von biologischem Material verwendet und in der Kryochirurgie zum Beispiel zur Behandlung von Warzen eingesetzt.[117] Ein Beispiel ist auch die Kühlung von Infrarot-Fotoempfängern, um deren thermisches Rauschen zu verringern oder überhaupt erst einen halbleitenden Zustand in ihnen herbeizuführen. Auch die Kühlung von Hochtemperatursupraleitern wird es eingesetzt.[118]
Ein weiterer Einsatzgebiet ist die Lebensmittelindustrie (Schockfrosten und Schälen von Lebensmitteln) und spezielle Arten der Gastronomie (Molekularküche).[119]
Im Tiefbau dient er der Bodenvereisung.[117] Im Bereich der Werkstofftechnik benutzt man Flüssigstickstoff, um Restaustenit in bestimmten gehärteten Stählen zu beseitigen oder die Werkstoffe durch „Tiefkühlen“ künstlich zu altern. Flüssiger Stickstoff wird auch eingesetzt, um zum Beispiel Getriebewellen so weit zu schrumpfen, dass aufgesetzte Zahnräder durch Presspassung auf der Welle halten. Beim Recycling werden Autoreifen oder bei Kabeln der Isolierstoff durch Kühlen mit flüssigem Stickstoff spröde und kann vom Metall (Aluminium bzw. Kupfer) abgeschlagen oder zerkleinert werden.[117]
Bei der (in Deutschland nicht zugelassenen) „Stickstoffbestattung“ (Promession) wird der Leichnam in einem Bad aus flüssigem Stickstoff eingefroren und anschließend zu einem Pulver zermahlen.
Stickstoffverbraucher bekommen Stickstoff oft statt in Druckgasflaschen als Flüssigstickstoff in Thermobehältern ähnlich einer Thermosflasche bereitgestellt. Diese Behälter bezeichnet man als Dewargefäß. Der Stickstoff wird dazu flüssig aus ebenfalls doppelwandigen Tankfahrzeugen abgefüllt.
Sicherheitshinweise
Obwohl Luft zu über 78 % aus Stickstoff besteht und Stickstoff ein Inertgas und somit ungiftig ist, müssen bei der Handhabung von gasförmigem Stickstoff in größeren Mengen Sicherheitsmaßnahmen getroffen werden – beispielsweise wenn aufgrund der Menge an Stickstoff die Gefahr besteht, dass Personen Arbeitsbereiche wie Maschinenräume betreten, welche aus Brandschutzgründen mit Stickstoffgas gefüllt sind, und durch Verdrängung kein oder nur eine ungenügende Menge an Sauerstoff für die Atmung vorhanden ist. Betritt eine Person einen solchen Bereich, kommt es zu einer heimtückischen, da durch die betroffene Person nicht bewusst wahrnehmbaren, normobaren Hypoxie durch Stickstoff, welche nach einigen Sekunden zu leichten Bewusstseinsstörungen gefolgt von Bewusstlosigkeit und nach wenigen Minuten zum Tod durch Erstickung führt. So kam es beispielsweise im Vorfeld der ersten Mission des Space Shuttle im März 1981 zum Tod zweier Techniker, welche einen aus Brandschutzgründen mit Stickstoff gefüllten Bereich in der Mobile Launcher Platform betreten hatten.[120]
Der Grund für diese Gefahr liegt darin, dass der menschliche Körper über keine hinreichend schnelle Sensorik im Glomus caroticum zur Erkennung der Unterversorgung mit Sauerstoff verfügt. Das Gefühl von Erstickung tritt bei einem Anstieg des Kohlendioxidgehalts im Blut auf, gefolgt von heftigem Atemreflex und Panik. Kann hingegen das Kohlendioxid in einer reinen Stickstoffatmosphäre problemlos abgeatmet werden, was in größeren mit Stickstoff gefüllten Räumen der Fall ist, kommt es zu keinem wahrnehmbaren Erstickungsgefühl und die Unterversorgung mit Sauerstoff führt zur vom Betroffenen nicht bewusst wahrnehmbaren Hypoxie.[121]
Daher müssen in Bereichen, in denen mit größeren Mengen Stickstoff hantiert wird und die potentielle Gefahr einer Erstickung beispielsweise bei Fehlfunktionen besteht, neben der nötigen Belüftung auch spezielle Warneinrichtungen vorhanden sein, die einen Sauerstoffmangel optisch oder akustisch anzeigen. Zusätzlich kann das Tragen einer persönlichen Schutzausrüstung nötig sein, welche das Unterschreiten des Sauerstoffgehalts unter einen Grenzwert rechtzeitig anzeigt.
Biologische Bedeutung und Stickstoffkreislauf
Schon im 19. Jahrhundert erkannte man, dass ein großer Teil der pflanzlichen Materie Stickstoff enthält und er ein wichtiges Bauelement aller Lebewesen ist. Er ist das wesentliche Element der Proteine und Proteide und der DNS. Stickstoff ist daher auch Baustein aller Enzyme, die den pflanzlichen, tierischen und menschlichen Stoffwechsel steuern. Stickstoff ist für das Leben auf der Erde unentbehrlich.
Stickstoffkreislauf
Der Stickstoffkreislauf beschreibt die Nutzbarmachung von Stickstoff aus der Luft für Pflanzen und Tiere und dessen Wiederabgabe in die Atmosphäre.

Lediglich eine kleine Anzahl von Mikroorganismen kann elementaren Stickstoff nutzen, ihn in ihre Körpersubstanz einbauen oder auch an Pflanzen abgeben. Pflanzen können, soweit bekannt, den gasförmigen Stickstoff der Luft nicht unmittelbar nutzen. Die Überführung in eine Form, die von den Pflanzen verwertbar ist, geschieht durch:
- Knöllchenbakterien: Diese Bakterien dringen in die Wurzeln der sogenannten Leguminosen ein. Sie ernähren sich von den Assimilaten der Pflanze. Im Tausch dafür liefern sie der Wirtspflanze Ammonium. Dieses wurde durch ein spezielles Enzym, der Nitrogenase, unter hohem Energieaufwand aus dem Luftstickstoff reduziert. Diese Lebensgemeinschaft ist eine Symbiose. Sie ermöglicht den Leguminosen die Besiedelung auch schlechter Standorte, weshalb der Mensch diese Pflanzen insbesondere im ökologischen Landbau zur Anreicherung des Bodens mit Stickstoff nutzt. Hier stellen Leguminosen die Hauptstickstoffquelle dar.
- Freilebende Mikroorganismen: Die nichtsymbiotische Stickstoffbindung beruht auf der Fähigkeit einiger freilebender Mikroorganismen (zum Beispiel Azotobacter und Cyanobakterien), Luftstickstoff zum Aufbau von körpereigenen Proteinen zu verwenden. Bei ackerbaulicher Nutzung wird die Größenordnung der Bindung von atmosphärischem Stickstoff durch freilebende Mikroorganismen mit 5–15 kg/ha und Jahr angenommen.
- Elektrische Entladung bei Gewittern: In niederschlagsreichen Gebieten können jährlich 20–25 kg N pro ha durch Regen dem Boden zugeführt werden. Das geschieht bei elektrischen Entladungen, wenn sich Sauerstoff und Stickstoff zu Stickstoffoxiden verbinden. Letztendlich reagieren diese Oxide mit dem Regenwasser zu Salpetersäure und im Boden können Nitrate entstehen.
- Ammoniaksynthese: Die Chemiker Fritz Haber und Carl Bosch haben zu Anfang des 20. Jahrhunderts ein Verfahren entwickelt, mit dem aus Luftstickstoff und Wasserstoff Ammoniak hergestellt werden kann. Die durch das Haber-Bosch-Verfahren möglich gewordene Nutzung des Stickstoff der Atmosphäre hat zur wesentlichen Ertragssteigerung landwirtschaftlicher Produktionen beigetragen. Die Ernährungssicherung konnte damit wesentlich verbessert werden. Die Pflanze baut aus dem aufgenommenen Ammoniak pflanzliche Proteine auf, die Mensch und Tier als Nahrung und zum Aufbau der eigenen Körperproteine dient. Im menschlichen und tierischen Organismus werden die Proteine zum großen Teil wieder abgebaut und mit dem Kot und Harn ausgeschieden. Zum heutigen Zeitpunkt wurde im Schnitt bereits jedes dritte Stickstoffatom in der Biosphäre einmal von der Düngemittelindustrie verarbeitet.[122]
- Autoabgase: Durch die Verbrennung fossiler Energieträger (Benzin, Diesel) werden durch den Autoverkehr Stickstoffverbindungen freigesetzt. Bei dem Verbrennungsvorgang entstehen Stickoxide (NOx, vor allem Stickstoffdioxid NO2, aber auch Stickstoffmonoxid NO und andere NOx-Verbindungen). In der Vergangenheit wurden diese direkt in die Umgebung entlassen. Heutzutage besitzen Autos Katalysatoren, welche diese Verbindungen reduzieren: NOx wird im Katalysator zu Ammoniak reduziert. Dieses wird im Beisein von Wasser in Ammonium umgewandelt (Ammoniak/Ammonium-Gleichgewicht in angesäuerter Lösung: NH3 + H3O+ ⇔ NH4+ + H2O). Sowohl die oxidierten als auch die reduzierten Stickstoffverbindungen werden über die Luft verfrachtet und tragen zu einem beträchtlichen Teil zur Eutrophierung benachbarter Ökosysteme bei.
Stickstoff in Pflanzen
Aufgaben in der Pflanze
Stickstoff wird in die Photosyntheseprodukte eingebaut, um unter anderem Eiweiße herzustellen, und fördert so das Wachstum. Eine wichtige Bedeutung kommt dem Stickstoff als essentieller Bestandteil der Desoxyribonukleinsäure und des Chlorophylls zu. Je nach Art liegt der Anteil der Trockensubstanz bei 2–6 %, oder bei durchschnittlich 1,5 %.[123] Die Aufnahme des Stickstoffs erfolgt meist in Form von Ammonium- oder Nitratsalzen.
Mangelsymptome
- kümmerlicher Wuchs
- blassgrüne Farbe der Blätter. Ältere werden chlorotisch und fallen vorzeitig ab.
- zu frühes Blühen (Notblüte)
- Vergilbungen
Überschusssymptome
- Mastiger Wuchs
- Blätter dunkelgrün
- Blüte verzögert
- Pflanze frost- und krankheitsanfällig
- Blattgewebe wirkt schwammig und weich
Nachweis
Stickstoff, der in organisch gebundener Form vorliegt, kann qualitativ mittels Lassaignescher Probe und quantitativ mittels der Stickstoffbestimmung nach Will-Varrentrapp, der Kjeldahlschen Stickstoffbestimmung, über ein Azotometer oder die Elementaranalyse erfasst werden. Für anorganisch gebundenen Stickstoff werden als Nachweisreaktion die Kreuzprobe für Ammoniumionen oder die Ringprobe für Nitrationen durchgeführt. Zur Durchführung der Ringprobe wird die Probelösung (schwefelsauer, schwermetallfrei) mit frischer Eisen(II)-sulfat-Lösung versetzt und mit konzentrierter Schwefelsäure unterschichtet. An der Grenzfläche zwischen beiden Flüssigkeiten werden die Nitrationen zu Stickstoffmonoxid (NO) reduziert. Dieses Radikal bildet in wässriger Lösung mit weiteren Eisenionen einen braunen Komplex, der als „Ring“ an der Phasengrenze im Reagenzglas sichtbar wird:
Schritt 1:
sowie Schritt 2:
Verbindungen
Stickstoff kommt in seinen Verbindungen in lückenloser Folge in den Oxidationsstufen −3 bis +5 vor, wobei die negativen Wertigkeiten in Verbindungen mit elektropositiven Elementen (zum Beispiel Wasserstoff) und die positiven Wertigkeiten in Verbindungen mit elektronegativen Elementen (zum Beispiel Sauerstoff) auftreten.[69]
Ammoniak
Ammoniak ist ein stark stechend riechendes, farbloses, wasserlösliches und giftiges Gas, das zu Tränen reizt und erstickend wirkt. Es ist der Grundstoff zur Herstellung anderer Stickstoffverbindungen, zum Beispiel Harnstoff, Ammoniumsalze wie Ammoniumnitrat und Ammoniumchlorid, Metallamide, Säureamide und Imide. Die Herstellung von Ammoniak erfolgt fast ausschließlich mit dem Haber-Bosch-Verfahren.
Nitride
Stickstoff bildet mit anderen Elementen verschiedene Arten von Nitriden:
- Kovalente Nitride wie Dischwefeldinitrid, Tetraschwefeltetranitrid, Siliciumnitrid und Bornitrid
- Metallische Nitride wie Titannitrid und Chromnitrid
- Salzartige Nitride wie Lithiumnitrid und Magnesiumnitrid

Titannitrid hat eine Natriumchlorid-Kristallstruktur. Es dient für Beschichtungen, die die Lebensdauer von Produkten, zum Beispiel Werkzeugen, verlängern. Diese goldfarbenen Schichten sind üblicherweise sehr dünn.
Siliciumnitrid tritt in drei Modifikationen (α-Si3N4, β-Si3N4 und γ-Si3N4) auf, die sich in ihrer Kristallstruktur unterscheiden. Es wird in der Halbleitertechnik und für Messspitzen von Rasterkraftmikroskopen verwendet.
Stickoxide
Bei Oxidationsprozessen, zum Beispiel bei der Verbrennung von Benzin, Erdöl und Kohle entstehen Stickoxide. Stickstoffquelle kann die Luft oder der Brennstoff sein. Einige Stickoxide, zum Beispiel Stickstoffdioxid, Stickstoffmonoxid und Distickstofftetroxid, sind giftig, ätzend und gesundheitsschädlich. Stickstoffdioxid und Distickstofftetroxid sind teilweise für den sauren Regen verantwortlich. Distickstoffmonoxid (Lachgas) wird als Narkosemittel eingesetzt. Es schädigt die Ozonschicht und ist ein sehr starkes Treibhausgas.[124]
Halogenide
Stickstofftrifluorid ist ein starkes Oxidationsmittel.[125] Es wird zur Herstellung von Halbleitern, Flachbildschirmen und Solarzellen verwendet. Iodstickstoff (Stickstofftriiodid) ist eine sehr instabile Verbindung, die hochexplosiv ist und bei Reibung, Schlag oder Erschütterung stark exotherm reagiert.[126]
Säuren und deren Salze
Salpetersäure ist eine starke Säure, die unter anderem zur Herstellung von Düngemitteln, Farbstoffen und Sprengstoffen verwendet wird. Die Salze der Salpetersäure sind die Nitrate. Ammoniumnitrat, Natriumnitrat, Kaliumnitrat und Calciumnitrat sind wichtige Düngemittel.
Salpetrige Säure ist eine mittelstarke, instabile Säure, die bei Erwärmung in einer Disproportionierungsreaktion zu Salpetersäure, Stickstoffmonoxid und Wasser zerfällt:[127]
Die Salze der Salpetrigen Säure sind die Nitrite. Natriumnitrit und Kaliumnitrit werden als Konservierungsmittel eingesetzt.[128]
Hyposalpetrige Säure ist eine schwache, instabile Säure, die bereits bei Zimmertemperatur zu Distickstoffmonoxid und Wasser zerfällt:[127]
Stickstoffwasserstoffsäure ist eine instabile, hochexplosive, die Schleimhäute reizende, stechend riechende Flüssigkeit. Die Salze der Stickstoffwasserstoffsäure heißen Azide. Bleiazid wird als Initialsprengstoff verwendet.[129]
Weitere anorganische Verbindungen
Cyanwasserstoff (Blausäure) ist eine farblose bis leicht gelbliche, brennbare, sehr flüchtige und wasserlösliche Flüssigkeit. Cyanwasserstoff und seine Salze, die Cyanide, zum Beispiel Kaliumcyanid und Natriumcyanid, sind hochgiftig. Ähnliches gilt für Hydrazin, das als Raketen- und Satellitentreibstoff und in Brennstoffzellen eingesetzt wird.
Weitere stickstoffhaltige Säuren sind Cyansäure, Isocyansäure und Knallsäure.
Organische Verbindungen

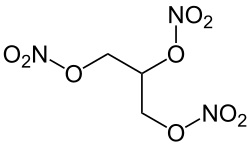
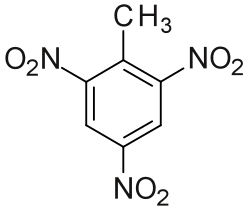

Stickstoff ist in zahlreichen organischen Verbindungen enthalten, zum Beispiel
- Organische Aminoverbindungen
- Amine wie Spermin
- Aminosäuren, Peptide und Proteine
- Azoverbindungen
- Nitroverbindungen und Salpetersäureester
- Nitromethan
- Sprengstoffe wie Nitroglycerin, Trinitrotoluol (TNT) und Octanitrocuban
- Stickstoffhaltige Heterocyclen wie Pyridin oder Indigo
Sonstiges
In den Niederlanden gibt es in dem seit dem 10. Januar 2022 amtierenden Kabinett Rutte IV erstmals einen Minister für Natur und Stickstoff (er ist Minister ohne Geschäftsbereich).
Literatur
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 651–743.
- Norman N. Greenwood, A. Earnshaw: Chemie der Elemente. 1. Auflage. VCH Verlagsgesellschaft, Weinheim 1988, ISBN 3-527-26169-9, S. 518–607.
- Harry H. Binder: Lexikon der chemischen Elemente – das Periodensystem in Fakten, Zahlen und Daten. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
Weblinks
- Literatur von und über Stickstoff im Katalog der Deutschen Nationalbibliothek
Einzelnachweise
- ↑ Harry H. Binder: Lexikon der chemischen Elemente. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
- ↑ Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Stickstoff) entnommen.
- ↑ Angegeben ist der von der IUPAC empfohlene Standardwert; da die Isotopenzusammensetzung dieses Elements örtlich schwanken kann, ergibt sich für die mittlere Atommasse der in Klammern angegebene Massenbereich. Siehe: Michael E. Wieser, Tyler B. Coplen: Atomic weights of the elements 2009 (IUPAC Technical Report). In: Pure and Applied Chemistry. 2010, S. 1, doi:10.1351/PAC-REP-10-09-14.
- ↑ IUPAC, Standard Atomic Weights Revised 2013.
- ↑ a b c d e Eintrag zu nitrogen in Kramida, A., Ralchenko, Yu., Reader, J. und NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1). Hrsg.: National Institute of Standards and Technology, Gaithersburg, MD. doi:10.18434/T4W30F (physics.nist.gov/asd). Abgerufen am 11. Juni 2020.
- ↑ a b c d e Eintrag zu nitrogen bei WebElements, www.webelements.com, abgerufen am 11. Juni 2020.
- ↑ a b c Eintrag zu Stickstoff in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. Januar 2026. (JavaScript erforderlich)
- ↑ Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics. CRC (Chemical Rubber Publishing Company), Boca Raton 1990, ISBN 0-8493-0470-9, S. E-129 bis E-145. Werte dort sind auf g/mol bezogen und in cgs-Einheiten angegeben. Der hier angegebene Wert ist der daraus berechnete maßeinheitslose SI-Wert.
- ↑ a b Yiming Zhang, Julian R. G. Evans, Shoufeng Yang: Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks. In: Journal of Chemical & Engineering Data. 56, 2011, S. 328–337, doi:10.1021/je1011086.
- ↑ Ernst von Meyer: Geschichte der Chemie. DOGMA Verlag, 2013, ISBN 978-3-95580-588-3, S. 117 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b A. F. Holleman, Wiberg Nils: Lehrbuch der anorganischen Chemie. De Gruyter, 2019, ISBN 978-3-11-083817-6, S. 539 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c Eintrag zu Stickstoff. In: Römpp Online. Georg Thieme Verlag, abgerufen am 5. Juli 2021.
- ↑ Hans Peter Latscha, Martin Mutz: Chemie der Elemente. Springer Berlin Heidelberg, 2011, ISBN 978-3-642-16915-1, S. 103 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Paul Diepgen, Heinz Goerke: Aschoff/Diepgen/Goerke: Kurze Übersichtstabelle zur Geschichte der Medizin. 7., neubearbeitete Auflage. Springer, Berlin/Göttingen/Heidelberg 1960, S. 29.
- ↑ W. Ruhland: Handbuch der Pflanzenphysiologie, Band VIII: Der Stickstoffumsatz / Nitrogen Metabolism. Springer Berlin Heidelberg, 1958, ISBN 978-3-642-94733-9, S. 1 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Claude Louis Berthollet, “Précis d’observations sur l’analyse animale comparée à analyse végétale” in Observations et mémoires sur la physique, sur l’histoire naturelle et sur les arts et métiers, Vol. 28, (Paris, 1786), S. 272–75
- ↑ Dieter Holzner, Karsten Holzner: Chemie für Technische Assistenten in der Medizin und in der Biologie. Wiley, 2018, ISBN 978-3-527-34283-9, S. 237 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Enzyklopädie Medizingeschichte. De Gruyter, ISBN 978-3-11-097694-6, S. 535 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Richard P. Aulie: Boussingault and the Nitrogen Cycle. In: Proceedings of the American Philosophical Society. Band 114, Nr. 6, 1970, S. 435–479, JSTOR:986146.
- ↑ Sven Schubert: Pflanzenernährung. utb GmbH, 2017, ISBN 978-3-8252-4509-2, S. 14 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Liebig, J.: Die organische Chemie in ihrer Anwendung auf Agricultur und Physiologie. Vieweg, Braunschweig 1840 (1. Aufl.) u. 1862 (7. Aufl.).
- ↑ John Bennet Lawes, Joseph Henry Gilbert, Evan Pugh: On the sources of the nitrogen of vegetation; with special reference to the question whether plants assimilate free or uncombined nitrogen. In: Proceedings of the Royal Society of London. Nr. 10, 1860, S. 544–557, doi:10.1098/rspl.1859.0109.
- ↑ Wolfgang Böhm: Biographisches Handbuch zur Geschichte des Pflanzenbaus. De Gruyter, 2014, ISBN 978-3-11-096710-4, S. 189 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Ludwig Darmstaedter, René Du Bois-Reymond, Carl Schaefer: Handbuch zur Geschichte der Naturwissenschaften und der Technik. Springer Berlin Heidelberg, 2013, ISBN 978-3-662-43152-8, S. 595 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Gerhart Drews: Bakterien – ihre Entdeckung und Bedeutung für Natur und Mensch. Springer Berlin Heidelberg, 2015, ISBN 978-3-662-45327-8, S. 90 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Elias König: Jäger des Unsichtbaren. FlipFlop, 2025, ISBN 978-3-695-35124-4 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Beat Kneubuehl: Ballistik. Springer Berlin Heidelberg, 2018, ISBN 978-3-662-58300-5, S. 59 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Siegfried Julius von Romocki: Geschichte der Explosivstoffe. DOGMA Verlag, 2013, ISBN 978-3-95580-637-8, S. 171 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Hugh S. Gorman: The Story of N. Rutgers University Press, 2013, ISBN 978-0-8135-5439-6, S. 4 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Adriano Zecchina, Salvatore Califano: The Development of Catalysis: A History of Key Processes and Personas in Catalytic Science and Technology. 1. Auflage. Wiley, 2017, ISBN 978-1-119-18126-2, S. 30, doi:10.1002/9781119181286.
- ↑ Commercial Process for Producing Calcium Carbide and Acetylene. In: acs.org. American Chemical Society, abgerufen am 19. April 2026.
- ↑ Anthony S. Travis: The Synthetic Nitrogen Industry in World War I. Springer International Publishing, 2015, ISBN 978-3-319-19357-1, S. 153 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Bruno Waeser: Die Luftstickstoff-Industrie. Springer Berlin Heidelberg, 2013, ISBN 978-3-662-28970-9, S. 3 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Edmund Oskar von Lippmann: Zeittafeln zur Geschichte der Organischen Chemie. Springer Berlin Heidelberg, 2013, ISBN 978-3-662-24666-5, S. 8 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Vaclav Smil: Enriching the Earth: Fritz Haber, Carl Bosch, and the Transformation of World Food Production. The MIT Press, 2000, ISBN 978-0-262-28385-4, doi:10.7551/mitpress/2767.001.0001.
- ↑ Vaclav Smil: Detonator of the population explosion. In: Nature. Band 400, Nr. 6743, 1999, S. 415–415, doi:10.1038/22672.
- ↑ JAMES N. GALLOWAY, JOHN D. ABER, JAN WILLEM ERISMAN, SYBIL P. SEITZINGER, ROBERT W. HOWARTH, ELLIS B. COWLING, B. JACK COSBY: The Nitrogen Cascade. In: BioScience. Band 53, Nr. 4, 2003, S. 341, doi:10.1641/0006-3568(2003)053[0341:TNC]2.0.CO;2.
- ↑ IPCC: Climate Change 2021 – The Physical Science Basis. Cambridge University Press, 2021.
- ↑ Bosch, H.; Janssen, F.: Catalytic Reduction of Nitrogen Oxides. In: Catalysis Today 2, 1988.
- ↑ Johan Rockström, Will Steffen, Kevin Noone, Åsa Persson, F. Stuart Chapin, Eric F. Lambin, Timothy M. Lenton, Marten Scheffer, Carl Folke, Hans Joachim Schellnhuber, Björn Nykvist, Cynthia A. de Wit, Terry Hughes, Sander van der Leeuw, Henning Rodhe, Sverker Sörlin, Peter K. Snyder, Robert Costanza, Uno Svedin, Malin Falkenmark, Louise Karlberg, Robert W. Corell, Victoria J. Fabry, James Hansen, Brian Walker, Diana Liverman, Katherine Richardson, Paul Crutzen, Jonathan A. Foley: A safe operating space for humanity. In: Nature. Band 461, Nr. 7263, 2009, S. 472–475, doi:10.1038/461472a.
- ↑ Steffen, W. et al.: Planetary boundaries: Guiding human development on a changing planet. In: Science 347, 2015, doi:10.1126/science.1259855.
- ↑ A Mulder: Anaerobic ammonium oxidation discovered in a denitrifying fluidized bed reactor. In: FEMS Microbiology Ecology. Band 16, Nr. 3, 1995, S. 177–183, doi:10.1016/0168-6496(94)00081-7.
- ↑ Holger Daims, Elena V. Lebedeva, Petra Pjevac, Ping Han, Craig Herbold, Mads Albertsen, Nico Jehmlich, Marton Palatinszky, Julia Vierheilig, Alexandr Bulaev, Rasmus H. Kirkegaard, Martin von Bergen, Thomas Rattei, Bernd Bendinger, Per H. Nielsen, Michael Wagner: Complete nitrification by Nitrospira bacteria. In: Nature. Band 528, Nr. 7583, 2015, S. 504–509, doi:10.1038/nature16461, PMID 26610024.
- ↑ A Valera-Medina, H Xiao, M Owen-Jones, W. I. F. David, P. J. Bowen: Ammonia for power. In: Progress in Energy and Combustion Science. Band 69, 2018, S. 63–102, doi:10.1016/j.pecs.2018.07.001.
- ↑ Ullmann's encyclopedia of industrial chemistry. Vol. 23: Nitric acid, nitrous acid, and nitrogen oxides to Nuclear technology. 6., completely rev. Auflage. Wiley-VCH-Verl, Weinheim 2003, ISBN 978-3-527-32943-4.
- ↑ Kevin Rouwenhorst: Low-emission Ammonia Production and Utilization. Royal Society of Chemistry, 2026, ISBN 978-1-83767-875-4.
- ↑ Peter W. Atkins, Julio de Paula: Kurzlehrbuch Physikalische Chemie. Wiley-VCH Verlag GmbH & Company KGaA, 2019, ISBN 978-3-527-82036-8, S. 13 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Hans Mohr: Stickstoff in der Biosphäre. Springer, Berlin, Heidelberg 1990, ISBN 978-3-662-06547-1, S. 8, doi:10.1007/978-3-662-06547-1_2.
- ↑ Informationsdienst Wissenschaft e. V.: Wie der Stickstoff auf die Erde kam, abgerufen am 12. April 2026.
- ↑ Astrodicticum Simplex: Sternengeschichten Folge 552: Der Stickstoff der Erdatmosphäre – Astrodicticum Simplex, abgerufen am 12. April 2026.
- ↑ John Grotzinger, Thomas Jordan: Press/Siever Allgemeine Geologie. Springer Spektrum, ISBN 978-3-662-48342-8, S. 222 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Yuan Li: The origin and evolution of Earth's nitrogen. In: National Science Review. Band 11, Nr. 6, 2024, S. nwae201, doi:10.1093/nsr/nwae201, PMID 38966072.
- ↑ Ritsuro Miyawaki, Frédéric Hatert, Marco Pasero, Stuart J. Mills: IMA Commission on New Minerals, Nomenclature and Classification (CNMNC) – Newsletter 69. In: Mineralogical Magazine. Band 86, 2022, S. 988–992, doi:10.1180/mgm.2022.115 (englisch, cambridge.org [PDF; 112 kB; abgerufen am 3. September 2024]).
- ↑ Malcolm Back, Cristian Biagioni, William D. Birch, Michel Blondieau, Hans-Peter Boja und andere: The New IMA List of Minerals – A Work in Progress – Updated: July 2024. (PDF; 3,6 MB) In: cnmnc.units.it. IMA/CNMNC, Marco Pasero, Juli 2024, abgerufen am 3. September 2024 (englisch).
- ↑ Classification of Deltanitrogen. In: mindat.org. Hudson Institute of Mineralogy, abgerufen am 3. September 2024 (englisch, siehe auch Anker „Strunz-Mindat“).
- ↑ Gregor Markl: Minerale und Gesteine. Springer Berlin Heidelberg, 2014, ISBN 978-3-662-44628-7, S. 519 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b JoAnn M. Holloway, Randy A. Dahlgren: Nitrogen in rock: Occurrences and biogeochemical implications. In: Global Biogeochemical Cycles. Band 16, Nr. 4, 2002, doi:10.1029/2002GB001862.
- ↑ Ralf Halama, Gray E. Bebout, Fernando Bea: Nitrogen loss and isotopic fractionation during granulite-facies metamorphism in the lower crust (Ivrea Zone, NW Italy). In: Chemical Geology. Band 584, 2021, S. 120475, doi:10.1016/j.chemgeo.2021.120475.
- ↑ Takahiro Yoshioka, Michael Wiedenbeck, Svyatoslav Shcheka, Hans Keppler: Nitrogen solubility in the deep mantle and the origin of Earth's primordial nitrogen budget. In: Earth and Planetary Science Letters. Band 488, 2018, S. 134–143, doi:10.1016/j.epsl.2018.02.021.
- ↑ Markus Bernhardt-Römermann, Jörg Ewald: Einst zu wenig, heute zuviel: Stickstoff in Waldlebensgemeinschaften. In: Gefahrstoffe – Reinhaltung der Luft. 66 (6), 2006, S. 261–266, Abstract.
- ↑ K. Lodders, M. Bergemann, H. Palme: Solar System Elemental Abundances from the Solar Photosphere and CI-Chondrites. In: Space Science Reviews. Band 221, Nr. 2, 2025, doi:10.1007/s11214-025-01146-w.
- ↑ Véronique Vuitton: Composition of Titan's Atmosphere. 2021, S. 217–230, doi:10.1016/B978-0-08-102908-4.00064-3.
- ↑ E. Maiorca, E. Caffau, P. Bonifacio, M. Busso, R. Faraggiana, M. Steffen, H.-G. Ludwig, I. Kamp: The Solar Photospheric Nitrogen Abundance: Determination with 3D and 1D Model Atmospheres. In: Publications of the Astronomical Society of Australia. Band 26, Nr. 3, 2009, S. 345–350, doi:10.1071/AS08056.
- ↑ K. Lodders, M. Bergemann, H. Palme: Solar System Elemental Abundances from the Solar Photosphere and CI-Chondrites. In: Space Science Reviews. Band 221, Nr. 2, 2025, S. 23, doi:10.1007/s11214-025-01146-w.
- ↑ Linda K. Glover: Die große National-Geographic-Enzyklopädie Weltall. National Geographic Deutschland, 2005, ISBN 978-3-937606-26-2, S. 54 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Cristina Chiappini, Francesca Matteucci, Silvia K. Ballero: The origin of nitrogen: the implications of very metal poor stars. In: Proceedings of the International Astronomical Union. Band 1, S228, 2005, S. 329–330, doi:10.1017/S1743921305005910.
- ↑ Arpita Roy, Ralph S Sutherland, Mark R Krumholz, Alexander Heger, Michael A Dopita: Helium and nitrogen enrichment in massive main-sequence stars: mechanisms and implications for the origin of WNL stars. In: Monthly Notices of the Royal Astronomical Society. Band 494, Nr. 3, 2020, S. 3861–3879, doi:10.1093/mnras/staa781.
- ↑ a b Hermann Sicius: Pnictogene: Elemente der fünften Hauptgruppe. Springer Fachmedien Wiesbaden, 2015, ISBN 978-3-658-10804-5, S. 11 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c d e f g h i j k l m n o Arnold F. Holleman, Nils Wiberg: Holleman/Wiberg - Anorganische Chemie, Band 1, Grundlagen und Hauptgruppenelemente. De Gruyter, ISBN 978-3-11-049585-0, S. 740 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Auskunftsbuch für die chemische Industrie. Halbband 2. De Gruyter, ISBN 978-3-11-266842-9, S. 1376 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b G. Brauer (Hrsg.): Handbook of Preparative Inorganic Chemistry. 2. Auflage. vol. 1, Academic Press, 1963, S. 457–460.
- ↑ H. Blücher: Auskunftsbuch für die chemische Industrie. Halbband 2. De Gruyter, 1923, ISBN 978-3-11-266842-9, S. 1376 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ LibreTexts: Oxidation States of Nitrogen
- ↑ Eintrag zu Stickstoff in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Dezember 2019. (JavaScript erforderlich)
- ↑ Encyclopedia of Inorganic and Bioinorganic Chemistry. 2. Auflage. Wiley, 2012, ISBN 978-1-119-95143-8, S. 3, doi:10.1002/9781119951438.eibc0147.
- ↑ Roland Span, Eric W. Lemmon, Richard T Jacobsen, Wolfgang Wagner, Akimichi Yokozeki: A Reference Equation of State for the Thermodynamic Properties of Nitrogen for Temperatures from 63.151 to 1000 K and Pressures to 2200 MPa. In: Journal of Physical and Chemical Reference Data. Band 29, Nr. 6, November 2000, S. 1361–1433, doi:10.1063/1.1349047.
- ↑ Bild einer Stickstoff-Spektralröhre ( vom 5. März 2016 im Internet Archive).
- ↑ E. Riedel, C. Janiak: Anorganische Chemie. 8. Auflage. de Gruyter, 2011, ISBN 978-3-11-022566-2, S. 464.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 653.
- ↑ a b c Michael Binnewies, Maik Finze, Manfred Jäckel, Peer Schmidt, Helge Willner, Geoff Rayner-Canham: Allgemeine und Anorganische Chemie. W.H. Freeman, 2016, ISBN 978-3-662-45067-3, S. 550 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Erwin Riedel, Hans-Jürgen Meyer: Allgemeine und Anorganische Chemie. De Gruyter, 2013, ISBN 978-3-11-027013-6, S. 268 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Ralf Steudel: Chemie der Nichtmetalle. De Gruyter, 2021, ISBN 978-3-11-241938-0, S. 335 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Lexikon der Chemie: Stickstoff, abgerufen am 28. April 2026.
- ↑ Pressemitteilung der Max-Planck-Gesellschaft vom 3. August 2004.
- ↑ Dominique Laniel, Bjoern Winkler, Timofey Fedotenko, Anna Pakhomova, Stella Chariton, Victor Milman, Vitali Prakapenka, Leonid Dubrovinsky, Natalia Dubrovinskaia: High-Pressure Polymeric Nitrogen Allotrope with the Black Phosphorus Structure in Phys. Rev. Lett. 124 (2020) 216001, doi:10.1103/PhysRevLett.124.216001.
- ↑ Neues Hochdruckmaterial entdeckt – Schwarzer Stickstoff folgt Goldener Regel der Chemie, Laborpraxis-Online, abgerufen am 2. Juni 2020.
- ↑ Weiyu Qian, Artur Mardyukov, Peter R. Schreiner: Preparation of a neutral nitrogen allotrope hexanitrogen C2h-N6. In: Nature. Band 642, Nr. 8067, Juni 2025, S. 356–360, doi:10.1038/s41586-025-09032-9.
- ↑ N6 ist der stärkste nichtnukleare Sprengstoff. Am 3. August auf n-tv.de
- ↑ Ideal als Raketentreibstoff. Forscher stellen energiereichste Substanz der Welt her am 25. Juni 2025 auf n-tv.de
- ↑ Robert John Strutt: An active modification of nitrogen, produced by the electric discharge. In: Proceedings of the Royal Society of London. Series A, Containing Papers of a Mathematical and Physical Character. Band 88, Nr. 605, 1913, S. 539–549, doi:10.1098/rspa.1913.0049.
- ↑ Sakun Duwal, Young-Jay Ryu, Minseob Kim, Choong-Shik Yoo, Sora Bang, Kyungtae Kim, Nam Hwi Hur: Transformation of hydrazinium azide to molecular N8 at 40 GPa. In: The Journal of Chemical Physics. Band 148, Nr. 13, 2018, doi:10.1063/1.5021976.
- ↑ Bipentazole (N10): A Low-Energy Molecular Nitrogen Allotrope with High Intrinsic Stability, Sergey V. Bondarchuk The Journal of Physical Chemistry Letters 2020 11 (14), 5544-5548, doi:10.1021/acs.jpclett.0c01542.
- ↑ National Nuclear Data Center, Brookhaven National Laboratory: Nudat 2. Abgerufen am 9. Januar 2019.
- ↑ G. Audi, F. G. Kondev, Meng Wang, W.J. Huang, S. Naimi: The NUBASE2016 evaluation of nuclear properties. In: Chinese Physics C. 41, 2017, S. 030001, doi:10.1088/1674-1137/41/3/030001 (Volltext).
- ↑ S. M. Naudé: An Isotope of Nitrogen, Mass 15. In: Physical Review. Band 34, Nr. 11, 1929, S. 1498–1499, doi:10.1103/PhysRev.34.1498.
- ↑ A. G. Norman, C. H. Werkman: The Use of the Nitrogen Isotope N15 in Determining Nitrogen Recovery from Plant Materials Decomposing in Soil 1. In: Agronomy Journal. Band 35, Nr. 12, 1943, S. 1023–1025, doi:10.2134/agronj1943.00021962003500120004x.
- ↑ David W. Emerich, Hari B. Krishnan: Nitrogen Fixation in Crop Production. American Society of Agronomy, 2009, S. 131 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Alexander E. Brodsky: Isotopenchemie. De Gruyter, 1961, ISBN 978-3-11-270869-9, S. 386 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Martin Bertau, Armin Müller, Peter Fröhlich, Michael Katzberg, Karl Heinz Büchel, Hans-Heinrich Moretto, Dietmar Werner: Industrielle Anorganische Chemie. Wiley-VCH, 2013, ISBN 978-3-527-64958-7, S. 32 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Arno Behr, Manfred Baerns, Axel Brehm, Jürgen Gmehling, Kai-Olaf Hinrichsen, Hanns Hofmann, Michael Kleiber, Norbert Kockmann, Ulfert Onken, Regina Palkovits, Dieter Vogt, Albert Renken: Technische Chemie. Wiley, 2023, ISBN 978-3-527-34574-8, S. 837 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Handbuch der Luftfahrzeugtechnik. Carl Hanser Verlag GmbH & Company KG, ISBN 978-3-446-43604-6, S. 777 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Detlef Gronwald, Martin Wolf: Lehrorientierte Einführung in die Elektrotechnik. Vieweg&Teubner Verlag, 2013, ISBN 978-3-322-83826-1, S. 161 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Prof. Dr. Ibrahim Elmadfa, Prof. Dr. Erich Muskat, Doris Fritzsche: E-Nummern & Zusatzstoffe. GR%C3%84FE UND UNZER Verlag GmbH, 2016, ISBN 978-3-8338-5293-0, S. 89 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Zusatzstoff-Zulassungsverordnung: Anlage 3 (zu § 5 Abs. 1 und § 7) Allgemein zugelassene Zusatzstoffe.
- ↑ Der ORF – Cremig und süffig wie Guinness vom 18. Juli 2016, abgerufen am 12. Dezember 2018.
- ↑ Johannes Tippmann, Thomas Becker: Analyse der Geschichte der Schankanlagentechnik und ihre Auswirkungen auf den heutigen Stand der Technik. In: Chemie Ingenieur Technik. Band 88, Nr. 12, 2016, S. 1891–1903, doi:10.1002/cite.201600034.
- ↑ Air Liquide: Schankgas: optimale Gasmischung für Gastro Ausschanktechnik, abgerufen am 2. Mai 2026.
- ↑ Dr.-Ing. Günter Bleisch, Prof. Dr. Horst-Christian Langowski, Prof. Dr.-Ing. Jens-Peter Majschak: Lexikon Verpackungstechnik. Behr's Verlag DE, 2014, ISBN 978-3-95468-166-2, S. 513 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Pneumatech: Wie Brauereien mit Stickstoff und Generatoren vor Ort erfolgreich sind, abgerufen am 2. Mai 2026.
- ↑ A. P. Iwanow: Elektrische Lichtquellen. De Gruyter, 1955, ISBN 978-3-11-270889-7, S. 281 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Handbuch der experimentellen Schulphysik. Aulis Verlag Deubner, S. 67 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Dieter Sautter, Hans Weinerth: Lexikon Elektronik und Mikroelektronik. Springer Berlin Heidelberg, ISBN 978-3-642-58006-2, S. 1009 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ by States Fell in 2015, Report says. The New York Times Dec. 16, 2015 (abgerufen am 16. Dezember 2015)
- ↑ czl/AP: Todesstrafe in den USA: Oberstes Gericht in Alabama erlaubt Hinrichtung mit Stickstoff. In: Der Spiegel. 3. November 2023, abgerufen am 3. November 2023.
- ↑ Ed Pilkington: Alabama executes Kenneth Smith using untested method of nitrogen gas. In: The Guardian, 26. Januar 2024, abgerufen am 26. Januar 2024 (englisch).
- ↑ Linde Gas Deutschland: Farbkennzeichnung bei Gasflaschen, abgerufen am 19. April 2026.
- ↑ a b c Helmuth Hausen, H. Linde: Tieftemperaturtechnik. Springer Berlin Heidelberg, 2013, ISBN 978-3-662-10553-5, S. 1 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Ron Legarski: Nitrogen. SolveForce, 2024 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Fabiola Pesce, Lucia Parafati, Biagio Fallico, Rosa Palmeri: Use of Liquid Nitrogen in Food Products: A Review. In: Food Frontiers. Band 6, Nr. 4, 2025, S. 1617–1644, doi:10.1002/fft2.70035.
- ↑ Space Shuttle Columbia Fast Facts. 28. Januar 2018, abgerufen am 20. Juli 2018.
- ↑ Cryogenic materials - The risks posed by using them. University of Bath, Department of Biology & Biochemistry, 6. Februar 2007, archiviert vom am 6. Februar 2007; abgerufen am 20. Juli 2018.
- ↑ Manfred Schloesser: Mikroorganismen- die größten Chemiker. Max-Planck-Institut für marine Mikrobiologie, Pressemitteilung vom 3. Februar 2010 beim Informationsdienst Wissenschaft (idw-online.de), abgerufen am 23. Dezember 2014.
- ↑ Lincoln Taiz, Eduardo Zeiger: Physiologie der Pflanzen. Spektrum, Akad. Verlag, Heidelberg/Berlin 2000, ISBN 3-8274-0537-8.
- ↑ Bedrohte Ozonschicht: Lachgas ist größeres Problem als FCKW. In: Spiegel Online. 28. August 2009, abgerufen am 13. April 2015.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 695.
- ↑ Eintrag zu Iodstickstoff. In: Römpp Online. Georg Thieme Verlag, abgerufen am 15. Juli 2014.
- ↑ a b A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9.
- ↑ Verordnung (EG) Nr. 1333/2008 in der konsolidierten Fassung vom 31. Oktober 2022
- ↑ Eintrag zu Bleiazid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
Auf dieser Seite verwendete Medien
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for gases under pressure
Carl Wilhelm Scheele (1742-1786)
Autor/Urheber: GRASYS, Lizenz: CC BY-SA 3.0
Flux distribution inside the fiber
Autor/Urheber: Stiftland-Gymnasium Tirschenreuth, Lizenz: CC0
Spektrum einer Stickstoff-Gasentladung durch ein Rowland-Gitter aufgenommen.
Lewisformel des Stickstoffmoleküls
Hexanitrogen - synthesis
Hexanitrogen - decomposition
Autor/Urheber: Alchemist-hp (talk) (www.pse-mendelejew.de), Lizenz: FAL
Spektralröhre = Gasentladungsröhre gefüllt mit Stickstoff N2. Betrieb mit: 1,8kV, 18mA, 35kHz. Länge ≈20cm.
Autor/Urheber: Pbsouthwood, Lizenz: CC BY-SA 4.0
IMCA Nitrogen gas cylinder shoulder colour code
Autor/Urheber: David Monniaux, Lizenz: CC BY-SA 3.0
Bei Zimmertemperatur kochender, flüssiger Stickstoff
Autor/Urheber:
- Cicle_del_nitrogen_ca.svg: Johann Dréo (User:Nojhan), traduction de Joanjoc d'après Image:Cycle azote fr.svg.
- derivative work: Burkhard (talk)
Stickstoffzyklus
Autor/Urheber: Peter Binter Original uploader was Binter at de.wikipedia, Lizenz: CC BY 3.0
Titanium nitride coated drill, 70 mm, Photographed by Peter Robert Binter, 25.06.2005
Chemische Strukturformel von Nitroglycerin
















