Siloxane
| Siloxane |
 Disiloxan |
 Hexamethyldisiloxan, |
 Octamethyltrisiloxan, |
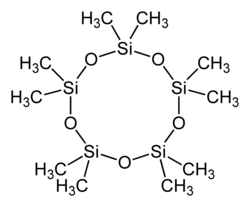 Decamethylcyclopentasiloxan, |
Siloxane sind chemische Verbindungen mit der allgemeinen Formel R3Si–[O–SiR2]n–O–SiR3, wobei R Wasserstoffatome oder Alkylgruppen sein können.[1] Im Gegensatz zu den Silanen sind die Siliciumatome nicht untereinander, sondern durch genau ein Sauerstoffatom mit ihrem benachbarten Siliciumatom verknüpft: Si–O–Si. Siloxane mit R = CH3 heißen Polydimethylsiloxane. Oligomere oder polymere Organosiloxane (Siloxane mit R ≠ H) heißen Silikone.[2] Sie besitzen lange Si–O-Hauptketten und sind je nach molarer Masse und -vernetzung zähflüssig oder dauerelastisch. Sind sie flüssig, heißen sie auch Silikonöle.
Verwendung
Siloxane, meist als Polydimethylsiloxane, finden unter anderem in Reinigungsmitteln, Kosmetika, Deodoranten, Seifen und Waschmitteln Verwendung. Im Bereich der Bauwerksabdichtung werden die hydrophoben Eigenschaften[3] genutzt. In der Industrie finden Siloxane (Silikonöle) als Entschäumer Anwendung, aber auch bei der Gefriertrocknung als Kälteträger.
Besondere Bekanntheit und Bedeutung haben höhermolekulare Siloxane, die sogenannten Silikone.
Industrielle Herstellung
Siloxane können auf verschiedene Art und Weisen hergestellt werden. Die Autoren des Werkes Winnacker-Küchler: Chemische Technik führen als wichtigste Herstellungsweisen folgende Methoden an:[4]
- kontinuierliche Hydrolyse von Dimethyldichlorsilan unter Abspaltung von Chlorwasserstoff
- kontinuierliche Reaktion von Dimethyldichlorsilan mit Methan unter Abspaltung von Chlormethan
- durch Reaktion von chlorierten Silanen mit Alkoxiden unter Abspaltung von Wasser und einer chlororganischen Verbindung
Siloxane in Klär- und Deponiegas
Siloxane können in geringen Konzentrationen (im Bereich 10 mg Silicium pro Normkubikmeter) in Klär- oder Deponiegas vorhanden sein. Bei Klärgas erfolgt der Siloxaneintrag durch Siedlungs- oder Industrieabwässer. Auf Deponien geht man eher von einer Zersetzung silikonhaltiger Abfälle in flüchtige Siloxane aus.
Siloxane werden bei der Verbrennung von Klär- und Deponiegas zum Problem, da aus dem Rohgas (z. B. im BHKW) festes Siliciumdioxid (Sand) entsteht, das zum Verschleiß der bewegten Teile der Anlagen führt. Weiß-graue Ablagerungen setzten sich auf Maschinenteile ab und werden über das Öl an alle beweglichen Teile der Maschine transportiert, wo sie zu Abrieb führen. Betroffene Teile sind v. a. Ventile, Zylinderköpfe, Turbinenschaufeln, Rohrleitungen.
Vor der Verbrennung in Gasmotoren werden Siloxane heute in der Regel durch Adsorption an Aktivkohle, Absorption oder Tieftemperaturkühlung (typischerweise bei Temperaturen unter −25 °C) zumindest teilweise entfernt. Neben diesen Techniken gibt es prinzipiell noch weitere Methoden der Siloxanabscheidung, darunter Adsorption mittels Silikagel, Aluminiumoxid oder katalytischen Materialien, Biofilter und Gaspermeation.[5] Ein typischer Grenzwert der meisten Gasmotorenhersteller für Silicium beträgt 5 mg Silicium pro Normkubikmeter Methan.
Aktivkohleadsorption
Aktivkohle verringert die Siloxankonzentrationen im Rohgas recht vollständig. Werte unter 0,1 mg Silicium pro Normkubikmeter sind typisch.[6] Ebenso werden auch die meisten anderen flüchtigen Kohlenwasserstoffe wie BTEX entfernt (was nicht unbedingt erforderlich ist). In der Tat führt die Anwendung von Aktivkohle bei Deponiegas zu einer relativ schnellen Erschöpfung der Beladungskapazität, da nicht nur Siloxane, sondern auch eine Vielzahl an flüchtigen Kohlenwasserstoffen adsorbiert. Deshalb wird der Aktivkohleadsorption oft ein Trocknungsschritt (z. B. Kondensation bei 5 °C) vorgeschaltet, welcher die relative Feuchte nach Wiederaufheizung des Gases verringert und einen Großteil der hydrophilen Spurenstoffe im Rohgas vorab entfernen soll. Eine Regeneration der Aktivkohle erfolgt in der Regel nicht, die verbrauchte Aktivkohle wird mit einer frischen Charge ersetzt. Hauptkostenpunkt einer Aktivkohle-basierten Siloxanreinigung ist v. a. der notwendige Austausch der Aktivkohle.[7][6] Es werden jedoch auch kommerzielle Adsorptionssysteme angeboten, die das Adsorptionsmittel regenerieren.
Absorption
Eine breite Auswahl verschiedener Waschflüssigkeiten wurde untersucht, um Siloxane entweder physikalisch oder chemisch aus dem Rohgasstrom zu absorbieren.[8] Chemische Absorption (also die Zerstörung des Siloxanmoleküls) erfolgt prinzipiell bei niedrigen oder hohen pH-Werten. Da basische Waschflüssigkeiten in Verbindung mit dem Kohlenstoffdioxid im Biogas zur Karbonatbildung führen, kommen jedoch nur Säuren als Absorptionsmittel in Frage. Neben der Stärke der Säure ist auch eine erhöhte Temperatur für die Siloxanabsorption förderlich. Der Umgang mit heißen Säuren ist möglich, stellt jedoch eine gewisse Sicherheitsherausforderung dar. Physikalische Siloxanabsorption wurde vor allem mit Wasser, organischen Lösemitteln und Mineralöl getestet. Siloxane sind i. d. R. hydrophob, so dass Wasseradsorption (pH 7) keine nennenswerte Abreicherung bewirkt.[9] Die Verwendung des sauren Sumpfwassers des Absorbers als Waschflüssigkeit kann jedoch sinnvoll sein. Erfahrungen mit der Verwendung von Mineralöl zeigen eine relativ geringe Reinigungsleistung[10] und ergaben Probleme mit in den Gasmotor eingetragenem Öldampf.[6]
Tieftemperaturkühlung
Die Effektivität der Reinigungsleistung der Tieftemperaturkühlung hängt von der Kühltemperatur ab. Je höher die Siloxanbelastung im Rohgas, desto besser ist die relative Siliciumabscheidung bei der gewählten Kühltemperatur. Vor allem das leicht flüchtige Hexamethyldisiloxan (L2), welches in höheren Konzentrationen besonders in Deponiegasen vorhanden ist, lässt sich jedoch selbst bei Temperaturen um −40 °C nicht signifikant auskondensieren. Klärgas hingegen enthält wesentlich höhere Anteile von D4 und D5. Um die Gesamtsiliciumkonzentration zu verringern, ist Tieftemperaturkühlung bei Klärgas deshalb effektiver als bei Deponiegas. Mit der Temperaturabsenkung verbunden ist auch ein Kondensieren vieler weiterer Stoffe (v. a. Wasser). Da das dabei anfallende saure Kondensat mit dem Rohgas kontaktiert wird, ist auch von einer gewissen Absorption der Siloxane in das Kondensat auszugehen.
Nebenwirkungen von Siloxanen
Abwasser: Bei der Membranfiltration sind Siloxane unerwünscht, da sie sich in die Poren der Membran einlagern und zu Fouling führen, welches durch Rückspülen und Einsatz von Chemikalien nur bedingt zu entfernen ist.[11]
Elektromechanische Kontakte (Schalter, Taster, Relais), die unter erhöhter Belastung stehen, können durch Siloxane verglasen. Dabei werden durch den Lichtbogen die Moleküle der Siloxane oberhalb von 1000 °C so zerlegt, dass SiO2 entsteht und den Kontakt isoliert. Bei dieser Art des Versagens spielt auch die Kontamination der Umgebung eine Rolle, da beispielsweise in Silikonölen gebundene Siloxane Wanderungsgeschwindigkeiten von 30…50 mm je 1000 h erreichen.[12], wobei die Beweglichkeit mit längeren Molekülen abnimmt. Daher können Reinigungs- und Pflegemittel, die Siloxane enthalten, auf nahegelegene Kontakte indirekt einwirken und ein Versagen bewirken.
Benennung
Die MDTQ-Notation ist etabliert:[13]
- M-Gruppe: (CH3)3SiO0.5
- D-Gruppe: (CH3)2SiO
- T-Gruppe: (CH3)SiO1.5
- Q-Gruppe: SiO2
| Cyclische Siloxane | Lineare Siloxane |
|---|---|
| D3: Hexamethylcyclotrisiloxan | MM oder L2: Hexamethyldisiloxan |
| D4: Octamethylcyclotetrasiloxan | MDM oder L3: Octamethyltrisiloxan |
| D5: Decamethylcyclopentasiloxan | MD2M oder L4: Decamethyltetrasiloxan |
| D6: Dodecamethylcyclohexasiloxan | MDnM oder PDMS: Polydimethylsiloxan |
Nur einfach methylierte Einheiten werden mit einem hochgestellten „H“ gekennzeichnet. So steht beispielsweise DH4 für Tetramethylcyclotetrasiloxan[14], MDHM für Bis(trimethylsiloxy)methylsilan[15] und M3TH für Tris(trimethylsiloxy)silan[16].[17][18]
Literatur
- Christoph Rücker, Klaus Kümmerer: Environmental Chemistry of Organosiloxanes. In: Chemical Reviews. 115(1), 2015, S. 466–524, doi:10.1021/cr500319v.
- Tarsilla Gerthsen: Chemie für den Maschinenbau 2. Universitätsverlag Karlsruhe, Karlsruhe 2008, ISBN 978-3-86644-080-7, 6 Polysiloxane SI., unter der CC BY-NC-ND 2.0 DE Lizenz erschienen, Download beim Verlag
Weblinks
Einzelnachweise
- ↑ Eintrag zu siloxanes. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.S05671.
- ↑ Eintrag zu silicones. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.S05670.
- ↑ Jürgen Weber; Volker Hafkesbrink (Hrsg.): Bauwerksabdichtung in der Altbausanierung - Verfahren und juristische Betrachtungsweise. 4. Auflage. Springer Fachmedien, Wiesbaden 2016, ISBN 978-3-658-07843-0, 10.2 "Injektionsstoffe und ihre Wirkungsweise", Abschnitt "Siloxane – Siliconmikroemulsionen".
- ↑ W. Kaiser, R. Riedle: Silikone. In: H. Harnisch, R. Steiner, K. Winnacker (Hrsg.): Winnacker-Küchler: Chemische Technologie, Organische Technologie I, I, 4. Auflage, Bd. 6. Carl Hanser Verlag, München 1982, S. 830–834
- ↑ M. Ajhar, M. Travesset, S. Yüce, T. Melin: Siloxane removal from landfill and digester gas – A technology overview. In: Bioresource Technology, 101, 2010, S. 2913–2923
- ↑ a b c D. Rossol, K.-G. Schmelz, R. Hohmann: Siloxane im Faulgas. In: KA – Abwasser Abfall 8,8 2003.
- ↑ E.P. Wheless, Jeffrey: Siloxanes in Landfill and Digester Gas Update SWANA. 27th Landfill Gas Conference, March 22–25 2004.
- ↑ M. Schweigkofler, R. Niessner: Removal of siloxanes in biogases. In: Journal of Haradous Materials, 83, 2001, s. 183–196.
- ↑ S. Rasi, J. Lantela, A. Veijanen, J. Rintala: Landfill gas upgrading with countercurrent water wash. In: Waste Management 28, 2008, S. 1528–1534.
- ↑ P. Martin, E. Ellersdorfer, A. Zemann: Auswirkungen flüchtiger Siloxane in Abwasser und Klärgas auf Verbrennungsmotoren. In: Korrespondenz Abwasser, 43, 5, 1996
- ↑ S. Wilhelm: Wasseraufbereitung Chemie und chemische Verfahrenstechnik. 7. Auflage. Springer Verlag, 2003, ISBN 978-3-540-25163-7, S. 126/127.
- ↑ Eduard Vinaricky (Hrsg.): Elektrische Kontakte, Werkstoffe und Anwendungen - Grundlagen, Technologien, Prüfverfahren. 3. Auflage. Springer-Verlag, Berlin Heidelberg 2016, ISBN 978-3-642-45426-4, 4.4 "Einfluss siliziumhaltiger Substanzen".
- ↑ Randal Myron Hill: Silicone surfactants. Marcel Dekker, New York 1999, ISBN 0-585-12871-5, S. 8.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Tetramethylcyclotetrasiloxan: CAS-Nr.: 2370-88-9, EG-Nr.: 219-137-4, ECHA-InfoCard: 100.017.399, GESTIS: 112389, PubChem: 75404, Wikidata: Q72507557.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Bis(trimethylsiloxy)methylsilan: CAS-Nr.: 1873-88-7, EG-Nr.: 217-496-1, ECHA-InfoCard: 100.015.906, GESTIS: 111122, PubChem: 74640, ChemSpider: 67215, Wikidata: Q27288310.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Tris(trimethylsiloxy)silan: CAS-Nr.: 1873-89-8, EG-Nr.: 217-497-7, ECHA-InfoCard: 100.015.907, PubChem: 6365044, Wikidata: Q83042181.
- ↑ M. Cypryk: 4.17 – Polymerization of Cyclic Siloxanes, Silanes, and Related Monomers. In: Polymer Science: A Comprehensive Reference. Elsevier, Amsterdam 2012, ISBN 978-0-08-087862-1, S. 451–476, doi:10.1016/b978-0-444-53349-4.00112-6.
- ↑ Mengchen Liao: The Role of Hydrosilanes in the Preparation of Silicones. 2021 (handle.net [abgerufen am 22. November 2022]).
Auf dieser Seite verwendete Medien
Chemical structure of disiloxane
Structural formula of the decamethylcyclopentasiloxane molecule, cyclo-(Me2SiO)5, i.e. C5H30O5Si5.
Structure from CRC Handbook, 88th edition.Octamethyltrisiloxan
Hexamethyldisiloxan



