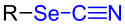Selenocyanate
| Selenocyanate |
Selenocyanat-Anion |
Organisches Selenocyanat, R = Organyl-Rest (z. B. Alkyl-Rest, Aryl-Rest etc.). Die Selenocyanat-Gruppe ist blau markiert. |
Als Selenocyanate werden die anorganischen Salze und die organischen Ester der unbeständigen Selenocyansäure (HSeCN)[S 1] bezeichnet. In den anorganischen Salzen ist das Proton der Selenocyansäure durch ein Alkali-, Erdalkali- oder anderes Kation ersetzt. In den organischen Estern ist das freie Proton der Selenocyansäure (HSeCN) durch einen Alkyl-, Aryl-, Alkylaryl oder einen anderen organischen Rest ersetzt.[1] Das Selenocyanat-Ion (NCSe−) kann als Ligand in Komplexen sowohl über das Stickstoff-Atom als auch über das Selen-Atom an das Zentralatom (Metallatom) koordinieren. In seinem chemischen Verhalten ähnelt es den Halogeniden und wird daher zur Gruppe der Pseudohalogenide gezählt.[2]
Synthese
Kaliumselenocyanat wird aus Kaliumcyanid und grauem Selenpulver durch eine Insertionsreaktion hergestellt. Analog wird Natriumselenocyanat[S 2] aus Natriumcyanid gewonnen. Alkylselenocyanate lassen sich aus Alkylbromiden oder Alkylchloriden durch Umsetzung mit Kaliumselenocyanat in alkoholischer Lösung darstellen. Aromatische Selenocyanate kann man aus Diazoniumsalzen durch Umsetzung mit Kaliumselenocyanat synthetisieren.[1]
Einzelnachweise
- ↑ a b Heinrich Rheinboldt in Houben-Weyl Methoden der Organischen Chemie, herausgegeben von Eugen Müller, Otto Bayer, Hans Meerwein und Karl Ziegler, Band 9, Schwefel-, Selen und Tellur-Verbindungen, Thieme Verlag, Stuttgart, 1955, dort 937–951.
- ↑ N. N. Greenwood und A. Earnshaw: Chemie der Elemente, VCH Verlag, Weinheim/Bergstrasse, Seiten 381–383, ISBN 3-527-26169-9.
Anmerkungen
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Selenocyansäure: CAS-Nr.: 13103-11-2, PubChem: 3014712, ChemSpider: 2283027, Wikidata: Q27110268.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Natriumselenocyanat: CAS-Nr.: 4768-87-0, EG-Nr.: 805-321-7, ECHA-InfoCard: 100.232.090, PubChem: 13927398, ChemSpider: 11517772, Wikidata: Q18235367.
Auf dieser Seite verwendete Medien
Organisches Selenocyanat
Selenocyanat-Anion