Schwarzes Roussin’sches Ammoniumsalz
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
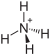  | |||||||
| Allgemeines | |||||||
| Name | Schwarzes Roussin’sches Ammoniumsalz | ||||||
| Andere Namen | Ammonium-heptanitrosyltri-μ3-thiotetraferrat | ||||||
| Summenformel | NH4[Fe4S3(NO)7] | ||||||
| Kurzbeschreibung | schwarzer Feststoff[1] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 565,71 g·mol−1 | ||||||
| Aggregatzustand | fest[1] | ||||||
| Dichte | 2,384 g·cm−3 (Monohydrat)[2] | ||||||
| Schmelzpunkt | >80 °C[1] | ||||||
| Löslichkeit | löslich in Wasser[1] | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Schwarzes Roussin’sches Ammoniumsalz (nach dem französischen Chemiker François-Zacharie Roussin) ist ein Komplexsalz mit der Formel NH4[Fe4S3(NO)7]. Es wird als Metallnitrosyl-Verbindung klassifiziert. Es besteht aus dem Ammoniumkation und dem [Fe4S3(NO)7]−-Anion. Die Geometrie des Anionenclusters ist ein unvollständiger Würfel. Die Punktgruppensymmetrie des Anions ist C3v. Mit dem Anion existieren auch noch andere Salze wie das Schwarze Roussin'sche Natriumsalz[4] oder das Schwarze Roussin'sche Eisensalz.
Gewinnung und Darstellung
Schwarzes Roussin’sches Salz wird durch Durchleiten von Stickstoffmonoxid durch eine Suspension von Eisen(II)-sulfid in verdünnter Alkalisulfidlösung erzeugt.[5] Es kann auch aus dem Roten Roussin'schen Salz[6] unter mild saurer Bedingungen gebildet werden. Diese Reaktion ist umkehrbar, und Rotes Roussin'sches Salz wird durch Alkalisieren der Reaktionslösung zurückgebildet.
Eigenschaften
Das Anion ist strukturell verwandt mit dem Eisen-Schwefel-Cluster, der in verschiedenen Enzymen, etwa der Nitrogenase, vorkommt.
Das Monohydrat NH4[Fe4S3(NO)7] × H2O kristallisiert als schwarzer Feststoff im triklinen Kristallsystem in der Raumgruppe P1 (Raumgruppen-Nr. 2) mit den Gitterparametern a = 944 pm, b = 994 pm, c = 566 pm, α = 117,2°, β = 101,3° und γ = 101,1° sowie zwei Formeleinheiten pro Elementarzelle.[2]
Verwendung
Schwarzes Roussin’sches Ammoniumsalz ist ein Stickstoffmonoxid-Spender. Das durch Schwarzes Roussin’sches Salz eingeschleuste Stickstoffmonoxid hat sich für einige Melanome und Tumorzellen als toxisch erwiesen. Schwarzes Roussin'sches Salz wirkt außerdem antibakteriell (desinfizierend), was z. B. in der Lebensmittelindustrie ausgenutzt wird.[7]
Literatur
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
Einzelnachweise
- ↑ a b c d Jane E. Macintyre: Dictionary of Inorganic Compounds. CRC Press, 1992, ISBN 978-0-412-30120-9, S. 3292 (google.de).
- ↑ a b L. L. Martin, G. D. Fallon, B. Wu: Ammonium heptanitrosyltrithiotetraferrate monohydrate. In: Acta Crystallographica Section E: Structure Reports Online. Band 60, Nr. 3, 2004, S. i37–i39, doi:10.1107/S1600536804002338.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Schwarzes Roussin'sches Natriumsalz: CAS-Nummer: 12518-87-5, Wikidata: Q2254194.
- ↑ Eintrag zu Roussinsche Salze. In: Römpp Online. Georg Thieme Verlag, abgerufen am 15. Juni 2014.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Rotes Roussin'sches Kaliumsalz: CAS-Nummer: 58204-17-4, PubChem: 162850, Wikidata: Q7371347.
- ↑ Agnieszka Janczyk, Agnieszka Wolnicka-Glubisz, Antonina Chmura, Martyna Elas, Zenon Matuszak, Grazyna Stochel, Krystyna Urbanska: NO-dependent phototoxicity of Roussin’s black salt against cancer cells. In: Nitric Oxide. Band 10, Nr. 1, 2004, S. 42–50, doi:10.1016/j.niox.2004.01.009.
Auf dieser Seite verwendete Medien
Anion des Heptanitrosyltrithiotetraferrats

