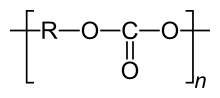
Polycarbonate
| Strukturformel | |||
|---|---|---|---|
 | |||
| Allgemeines | |||
| Name | Polycarbonate | ||
| Andere Namen |
| ||
| CAS-Nummer | 25037-45-0 | ||
| Monomer | Kohlensäureester | ||
| Summenformel der Wiederholeinheit | C16H14O3 | ||
| Molare Masse der Wiederholeinheit | 254,17 g·mol−1 | ||
| Art des Polymers | Thermoplast | ||
| Eigenschaften | |||
| Aggregatzustand | fest | ||
| Dichte | ca. 1,20 g·cm−3[1] | ||
| Glastemperatur | ca. 148 °C[1] | ||
| Härte | R122 (Rockwell, ISO 2039)[1] | ||
| Schlagzähigkeit | 60 kJ m−2 (Kerbschlagzähigkeit Charpy, ISO 179/eA)[1] | ||
| Elastizitätsmodul | 2400 MPa[1] | ||
| Wasseraufnahme | 0,12 (23 °C/59 % r.F./24 h)[1] | ||
| Bruchdehnung | 120 %[1] | ||
| Wärmeformbeständigkeit | 125 °C (HDT A, ISO 75)[1] | ||
| Wärmeleitfähigkeit | 0,20 W m−1 K−1[1] | ||
| Thermischer Ausdehnungskoeffizient | 65·10−6 K−1 (DIN 53328)[2] | ||
| Sicherheitshinweise | |||
| |||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||
Polycarbonate (Kurzzeichen PC) sind thermoplastische Kunststoffe. Sie sind formal Polyester der Kohlensäure. Polycarbonate können durch Polykondensation von Phosgen mit Diolen oder durch ringöffnende Polymerisation von cyclischen Carbonaten hergestellt werden. Praktische Bedeutung haben sie zur Synthese aromatischer Bishydroxyverbindungen, wie beispielsweise Bisphenol A, woraus das sogenannte Bisphenol A-Polycarbonat als wichtigster Vertreter der Polycarbonate synthetisiert wird. Als Alternative zu Phosgen kann auch eine Umesterung mit Kohlensäurediestern stattfinden.[4] Der Recycling-Code für Polycarbonate ist 07 (Andere Kunststoffe).
Geschichte
Obwohl bereits 1898 Alfred Einhorn aromatische Polycarbonate entdeckte, wurde das erste industriell relevante Polycarbonat erst 1953 von Hermann Schnell bei der Bayer AG entwickelt.[1] Dieses basierte auf 2,2-Bis(4-hydroxyphenyl)propan (Bisphenol A). Bayer begann 1958 mit der großtechnischen Produktion unter dem Handelsnamen Makrolon. Später wurde diese Markenbezeichnung von Bayer auch auf andere Polycarbonate ausgedehnt. 1973 folgte General Electric mit der großtechnischen Produktion unter dem Handelsnamen Lexan (heute gehört sie dem Hersteller SABIC).[1]
Synthese
Die weitestverbreiteten Polycarbonate sind jene, welche Bisphenol A als Dihydroxykomponente und Phosgen verwenden.
Die Herstellung geschieht über Grenzflächenkondensation. Die wässrige Phase besteht aus Natronlauge, in der sich Bisphenol A als Natriumsalz löst. In die organische Phase aus beispielsweise Dichlormethan wird das gasförmige Phosgen eingeleitet. Als Katalysatoren wirken tertiäre Amine; die Reaktion setzt bereits bei Raumtemperatur ein. Chlorwasserstoff wird unmittelbar mit der Natronlauge zu Natriumchlorid umgesetzt.[5]
Alternativ können Polycarbonate über Umesterung mit Diphenylcarbonat hergestellt werden. Bei dieser Schmelzkondensation verläuft die Reaktion unter Schutzgas bei niedrigem Druck, das Reaktionsprodukt Phenol wird durch den Unterdruck aus der Reaktionsmasse entfernt:[5]
Die Reaktion wird bei 180 bis 220 °C begonnen, als Katalysatoren dienen Basen. Bei bis zu 300 °C und Unterdruck wird die Polykondensation abgeschlossen.
Varianten
Anstatt Bisphenol A werden auch folgende Hydroxyverbindungen eingesetzt:

Bisphenol S
Dihydroxydiphenylsulfid
1,1,1-Tris(4-hydroxyphenyl)-ethan
(THPE)
Tetramethylbisphenol A
1,1-Bis(4-hydroxyphenyl)-
3,3,5-trimethylcyclohexan
(BPTMC)
Durch Verwendung von Gemischen obiger Komponenten können Eigenschaften des entstehenden Polycarbonats z. T. stufenlos variiert werden. Cokondensate aus Bisphenol A und BPTMC führen zu hochtransparenten, wärmeformbeständigen Kunststoffen. THPE erlaubt den Einbau von Kettenverzweigungen, die die Strukturviskosität bei der Verarbeitung des Materials (beispielsweise bei der Extrusion) positiv beeinflussen. Dihydroxydiphenylsulfid führt zu einem hohen Brechungsindex des Kunststoffs, was für die Herstellung von optischen Linsen vorteilhaft ist.
Eine andere Syntheseroute kommt beim Duroplast Polyallyldiglycolcarbonat zum Einsatz, dort ist bereits das Monomer ein Carbonat, und wird radikalisch polymerisiert.
Eigenschaften
Polycarbonate weisen in der Regel einen Kristallitanteil von weniger als 5 % auf und gelten daher als amorph. Sie zeichnen sich durch hohe Festigkeit, Schlagzähigkeit, Steifigkeit und Härte aus. Außerdem sind Polycarbonate gute Isolatoren gegen elektrische Spannung.[4]
Polycarbonate sind entflammbar, die Flamme erlischt jedoch nach Entfernen der Zündquelle. Polycarbonat erfüllt die Anforderungen der Baustoffklasse B2 nach DIN 4102. In Schichtdicken zwischen 1 und 6 mm ist es im Falle von Innenanwendungen in die Baustoffklasse B1, „schwer entflammbar“ eingestuft. Auch die Anforderungen an das Brandverhalten von PC-Fahrzeugscheiben gemäß Zulassungsrichtlinien wie TA29 (national), ECE43 oder ANSI Z26.1 (USA) werden erfüllt.
Der wasserklare Kunststoff zeichnet sich durch Glas-ähnliche Licht-Transmissionsgrade (88 % bei 3 mm Dicke nach DIN 5036-1) und Brechungsindizes (1,59 nach ISO 489-A) aus.
Polycarbonat ist empfindlich gegenüber UV-Licht im Wellenlängen-Bereich um 340 nm. Bestrahlung mit Licht dieser Wellenlänge, u. a. durch Einsatz unter freiem Himmel, führt ohne Schutzbeschichtung zu Brüchen und Umlagerungen im Polymermolekül, die das Material mit der Zeit verspröden und vergilben lassen.
Die maximale Gebrauchstemperatur liegt bei 125 °C, kurzzeitig bis zu 135 °C. Die Glasübergangstemperatur ist 148 °C. Wie alle amorphen Kunststoffe hat Polycarbonat keinen Schmelzpunkt.
Chemikalienbeständigkeit
Polycarbonate haben eine Beständigkeit gegenüber[1][4]:
- Wasser,
- Alkoholen (mit der Ausnahme von Methanol),
- Fetten,
- Ölen,
- Glycol,
- verdünnte Säuren,
- verdünnte Basen,
- vielen Mineralsäuren und
- wässrigen Lösungen von neutralen Salzen und Oxidationsmitteln.
Keine Beständigkeit haben sie gegen[1][4]:
- Benzol,
- Toluol,
- Xylol,
- chlorierte Kohlenwasserstoffen,
- Methanol,
- starke Säuren,
- starke Laugen,
- alkalische wässrige Lösungen,
- Amine und
- Ammoniak.
Außerdem führt das längere Wirken von heißem Wasser zur Hydrolyse.[1]
Zu den spannungsrissauslösenden Medien für Polycarbonat zählen[1]:
- Aceton,
- Ether,
- Anilin,
- Ester,
- Kaliumhydroxid,
- Ketone,
- Kohlenwasserstoffe,
- Methanol,
- Natriumhydroxid,
- chlorhaltige Quellmittel,
- Terpentin und
- Tetrachlorkohlenstoff.
Anwendungen

Polycarbonate sind transparent und farblos. Sie können jedoch eingefärbt werden.
Polycarbonat ist verhältnismäßig teuer. Es wird daher fast nur dort eingesetzt, wo andere Kunststoffe zu weich, zu zerbrechlich, zu kratzempfindlich, zu wenig formstabil oder nicht transparent genug sind. Darüber hinaus wird Polycarbonat als transparenter Kunststoff wie auch Polymethylmethacrylat (PMMA) oder Styrol-Acrylnitril (SAN) häufig als Glas-Alternative eingesetzt. Im Vergleich zum spröden Glas ist Polycarbonat leichter und deutlich schlagfester. Außerdem besteht bei moderaten Aufprallenergien bzw. Geschwindigkeiten keine Gefahr durch Splitterbildung.
Die Anwendbarkeit als transparente Glas-Alternative kann durch die geringere Abriebbeständigkeit des Polycarbonats eingeschränkt sein. Im Taber-Test nach ASTM D1044 (DIN 52347 bzw. ISO 15082 für Kunststoff-Verglasung) erreicht der Kunststoff nach 100 Zyklen lediglich ∆Haze-Werte um 30 %, d. h., er trübt durch Kontakt mit abrasiven Medien wie z. B. Flugsand deutlich ein. Dieses Manko kann durch Beschichtungen, etwa auf Basis von Polysiloxanen, Polyepoxiden oder Polyurethanacrylaten, ausgeglichen werden. Bereits Polysiloxan-Lackschichten von 5 bis 8 µm Dicke können Polycarbonat-Halbzeuge oder -Werkstücke mit einer glasähnlich-harten Oberfläche (∆Haze nach 100 Zyklen < 4 %) ausstatten.
Mittels geeigneter Lacke lässt sich auch die Chemikalien- und UV-Beständigkeit des Werkstoffs deutlich erhöhen.[6] Spezialisierte Beschichtungen können Polycarbonate darüber hinaus mit selbstreinigenden oder wasserabweisenden Oberflächen ausstatten. Auch die Ableitung statischer Elektrizität ist möglich, die Polycarbonat-Scheiben den Einsatz etwa als Maschinenabdeckung in explosionsgeschützten Bereichen erlauben.
Im Verbund mit transparenten thermoplastischen Polyurethanen (TPU) lassen sich aus Polycarbonat leichte, UV-beständige Verbundsicherheits-Verscheibungen fertigen, die auch im Blick auf das wichtige Head Injury Criterion (HIC) nach DIN 52310 gut abschneiden. Der von der TA29 bzw. ECE 43 (Richtlinie für Fahrzeugverscheibungen) geforderte Grenzwert HIC < 1000 wird von diesen Verbundsicherheitsscheiben unterschritten.
Polycarbonate werden unter anderem eingesetzt zur Herstellung von:
- CDs, DVDs und Blu-ray Discs
- Brillengläsern und optischen Linsen
- Abschlussscheiben (Streuscheiben) von Autoscheinwerfern
- Fenstern von Strahlflugzeugen
- Koffern
- einbruchhemmender Verglasung
- Unterwassergehäusen für Kameras
- Hinterseitenabdeckungen von Mobiltelefonen (meist Smartphones) und Tabletcomputern
- Verscheibungen von Wintergärten und Gewächshäusern
- Verkleidungen avantgardistischer Bauwerke[7]
- Solarmodule
- Schutzhelmen und Visieren
- Campinggeschirr
- wegen guter Biokompatibilität bei einer Vielzahl medizinischer Einmalprodukte
- Mikrofasern mit dem elektrostatischen Sprühverfahren[8]
Der Weltverbrauch an Polycarbonat lag im Jahr 2009 bei etwa 3 Millionen Tonnen, was etwa einem Wert von 6 Mrd. € entsprach.[9]
Verarbeitung
Polycarbonate lassen sich mit allen für Thermoplaste üblichen Verfahren verarbeiten. Beim Spritzgießen wird wegen der hohen Viskosität der Schmelze ein hoher Spritzdruck benötigt. Die Verarbeitungstemperaturen liegen zwischen 280 und 320 °C und beim Extrudieren zwischen 240 und 280 °C. Vor der Verarbeitung muss allerdings die Restfeuchte durch Trocknung (4 bis 24 Stunden bei 120 °C) auf unter 0,01 Prozent gebracht werden. Die Verarbeitungsschwindung von Polycarbonat liegt bei 0,6 bis 0,8 Prozent. Polycarbonat weist so gut wie keine Nachschwindung auf. Es lässt sich mit Lösungsmitteln wie beispielsweise Dichlormethan und Reaktionsharzklebstoffen kleben und ist ultraschall- und hochfrequenzschweißbar.
Sicherheitshinweise
Amerikanischen und japanischen Untersuchungen zufolge kann aus bestimmten Polycarbonaten, für deren Herstellung das Monomer Bisphenol A verwendet wurde, dieses bei Erhitzung wieder freigesetzt werden. Bisphenol A steht im Verdacht, erhebliche gesundheitliche Schädigungen hervorrufen zu können.[10] In der EU ist deshalb der Einsatz von Polycarbonat, das Bisphenol A enthält, beispielsweise als Material für Babyflaschen, verboten.[11][12] Die seither verwendeten Ersatzstoffe Bisphenol S, Bisphenol F und Bisphenol HPF haben laut des Ausschusses für Risikobewertung (RAC) der Europäischen Chemikalienagentur (ECHA) jedoch die gleichen gesundheitsschädigenden Nebenwirkungen wie BPA.[13][14]
Recycling

Der Recycling-Code für Polycarbonate ist 07.
Trivia
Die 180 Fenster des Brüsseler Atomiums bestehen seit der Restaurierung im Jahr 2006 aus beschichtetem Polycarbonat.
Das Dach des Olympiastadions Athen besteht aus rund 25.000 Quadratmetern Polycarbonat-Platten, die in einem Unternehmen in Geesthacht (bei Hamburg) zuvor mit einer UV-beständigen Lackschicht versehen wurden.

Als Klassiker des deutschen Designs gilt der Füllfederhalter Lamy 2000 der von Gerd A. Müller gestaltet wurde. Für einen Füller war die Wahl des Werkstoffes Makrolon ungewöhnlich.
Die Bundeswehr verwendete ab 1965 Ferngläser des Typs Fero-D 12 der Marke Steiner-Optik. Diese Ferngläser hatten ein Gehäuse aus Makrolon und waren aus diesem Grund deutlich leichter als die Ferngläser mit einem Metallkorpus.[15]
Der Lamborghini Gallardo Superleggera hat u. a. ein Rückfenster und eine Motorraumabdeckung aus abriebfest beschichtetem, UV-beständigem Polycarbonat. Die Bauteile entstehen durch Warmumformung und CNC-Fräsen von Polycarbonat-Halbzeugen. Grund für die Material-Wahl war unter anderem das im Vergleich zu Glas geringere Gewicht des Werkstoffs. Dies spart Gewicht (und damit Treibstoff) und verlagert den Schwerpunkt des Wagens etwas nach unten (je tiefer der Schwerpunkt eines Fahrzeugs, desto besser liegt es auf der Straße). Bei zivilen Automobilen ist laut Autoverscheibungs-Norm ECE R43 hinter der B-Säule eine maximale Trübungszunahme (ΔHaze) von 10 % nach 500 Zyklen des Taber-Tests zulässig. Diese Werte werden von Polysiloxan-beschichtetem Polycarbonat gut erreicht.
Der Grevenbroicher Künstler Matthias Hintz fertigt Skulpturen aus Polycarbonat. Dazu fügt er bis zu 20.000 CDs mit einem Heißluftfön zusammen.[16]
Weblinks
- Material Archiv: Polycarbonat (PC) – Umfangreiche Materialinformationen und Bilder
Einzelnachweise
- ↑ a b c d e f g h i j k l m n o Hans Domininghaus (Hrsg.): Die Kunststoffe und ihre Eigenschaften. 8. Auflage, Springer-Verlag Heidelberg 2012, S. 714ff.
- ↑ TECHNISCHES DATENBLATT PC – Polycarbonat. Archiviert vom am 14. September 2022; abgerufen am 14. September 2022.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b c d Eintrag zu Polycarbonate. In: Römpp Online. Georg Thieme Verlag, abgerufen am 12. Juni 2014.
- ↑ a b Wolfgang Kaiser: Kunststoffchemie für Ingenieure. 3. Auflage. Carl Hanser, München 2011, S. 331 ff.
- ↑ Korinna Brammer et al.: (Glas)klare Sache. In: Kunststoffe, Heft 8/2006, S. 84–87.
- ↑ De Zeen: Polycarbonate. Abgerufen am 27. März 2020.
- ↑ Walter Loy: Chemiefasern für technische Textilprodukte. 2., grundlegende überarbeitet und erweiterte Auflage. Deutscher Fachverlag, Frankfurt am Main 2008, ISBN 978-3-86641-197-5, S. 258.
- ↑ Dietrich Braun: Kleine Geschichte der Kunststoffe, 2. Auflage. Carl Hanser Verlag, München 2017, ISBN 978-3-446-44832-2, S. 290.
- ↑ Polycarbonate Plastics and Bisphenol A Release ( vom 19. Mai 2016 im Internet Archive).
- ↑ EU-Koordination Deutscher Naturschutzring (DNR):EU-weites Verbot für Bisphenol A in Babyflaschen ab Juni 2011. ( vom 1. September 2011 im Internet Archive) Meldung vom 26. November 2010.
- ↑ Europäische Kommission: Bisphenol A: EU-Verbot von Säuglingsflaschen tritt morgen in Kraft. Pressemitteilung vom 31. Mai 2011.
- ↑ All news - ECHA. Abgerufen am 15. Januar 2025 (deutsch).
- ↑ CHEM Trust: Von BPA bis BPZ - eine toxische Buchstabensuppe? In: Lobbyregister des Deutschen Bundestags. Abgerufen am 15. Januar 2025.
- ↑ Hans T. Seeger: Militärische Ferngläser und Fernrohre in Heer, Luftwaffe und Marine. Hamburg, 1996, ISBN 3000004572. Zitiert nach Review: Zeiss Dienstglas 8x30 vs. Hensoldt DF 8x30 vs. Steiner Fero-D 12 , abgerufen am 27. August 2011
- ↑ Stefan Albus: Polycarbonat – der Marmor von morgen? In: K-Zeitung, Heft 16/2012, S. 25–26.
Auf dieser Seite verwendete Medien
Struktur des Bisphenol S
Polycarbonatsynthese aus Bisphenol A und Phosgen
Autor/Urheber: Roland.chem, Lizenz: CC0
Synthese von Polycarbonaten mit Diphenylcarbonat
Autor/Urheber: Luis Fernández García, Lizenz: CC BY-SA 2.1 es
Interference colors. Iridiscente reflections on a compact disc.
Plastic recycle logo: Other
(c) Photo: Andrew Linnett/MOD, OGL v1.0
The new Steiner Military 8×30 R binoculars,which replace the Avimo General Purpose Binocular L12A1 7x42 first issued to the Army in 1979.
Lightweight and ergonomic Steiner Military 8×30 R binoculars. Designed to be easier to hold, the new models are 50% lighter than the previous issue, but still offer increased magnification to give better situational awareness.
- Organization: MOD
- Object Name: DES-2014-006-0353
- Keywords: Army, Equipment, Viewing Aid, Binoculars, Camouflage
- Country: England
Autor/Urheber: Vincent Ignace, Lizenz: CC BY-SA 3.0
Lamy 2000 fountain pen with cap off. The black plastic used in the cap and pen body is Polycarbonate branded as Makrolon by Bayer.
Autor/Urheber: Roland.chem, Lizenz: CC0
1,1-Bis(4-Hydroxyphenyl)-3,3,5-trimethylcyclohexan
Autor/Urheber: Roland.chem, Lizenz: CC0
Tetramethylbisphenol A, 2,2-bis-(4-Hydroxy-3,5-dimethylphenyl)propan



















