Polydnaviriformidae
| Polydnaviridae | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Polydnaviridae | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Taxonomische Merkmale | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Polydnaviridae | ||||||||||||
| Links | ||||||||||||
|
Die Polydnaviriformidae (früher Polydnaviridae, Polydnaviren) sind eine Familie behüllter Viriformer, d. h. virusartiger Partikel mit doppelsträngigem, segmentierten DNA-Genom, welche in das Genom von einigen Schlupfwespen integriert sind und als viraler Vektor zur Beeinflussung der Wirte der Schlupfwespenlarven dienen. Die Familie enthält zwei Gattungen mit geringer Homologie zueinander, Ichnoviriform (früher Ichnovirus, Ichnoviren) mit einfacher Lipiddoppelschicht und Bracoviriform (früher Bracovirus, Bracoviren) mit doppelter Lipiddoppelschicht in ihrer jeweiligen Virushülle. Erstere kommen in Ichneumonidae vor, während letztere in Braconidae auftreten.
Struktur
Während Ichnoviriforme im Transmissionselektronenmikroskop eine eiförmige Gestalt besitzen (Ascoviridae-ähnliche Morphologie), sind Bracoviriforme stabförmig (Baculoviridae-ähnlich).[2] Die Entstehung der Polydnaviren wird auf zwischen 64 und 100 Millionen Jahre vor unserer Zeitrechnung datiert und wird heute ausschließlich auf die Nachkommenschaft übertragen (vertikale Infektion).[3][4][5] Das virale Genom ist in das Genom der Schlupfwespe integriert, während die Virionen der Polydnaviren nur in den Calyxzellen der Ovarien gebildet werden und gemeinsam mit den Wespeneiern in die parasitierte Raupe injiziert werden.[6] Das Virion enthält mehrere Kopien viraler dsDNA in segmentierter, ringförmiger und superspiralisierter Form mit Längen zwischen 2 Kbp und 31 Kbp.[7] Je nach Spezies kommen ein bis mehrere Kapside pro Virion vor, also innerhalb einer Virushülle.[7] Bracoviren verlassen die Calyxzellen durch Lyse, während Ichnoviren die Calyxzellen durch Knospung verlassen.[7]
Parasitismus und Symbiose

Polydnaviriforme sind Teil einer einzigartigen Wirts-Pathogen-Beziehung zwischen parasitoiden Schlupfwespen, den parasitierten Raupen (meist Lepidoptera) und dem symbiotischen Virus der Schlupfwespe. Die Raupen sind Wirte der parasitoiden Schlupfwespenlarven, während die Schlupfwespen symbiontische Wirte für die Polydnaviren sind. Gleichzeitig sind Polydnaviren Pathogene für die Raupen,[8] was den symbiotischen Nutzen für die Schlupfwespen darstellt. Die Virionen der Polydnaviren werden nur in den Calyxzellen der Ovarien gebildet und gemeinsam mit den Wespeneiern in die parasitierte Raupe injiziert.[9] Das Virion enthält nicht alle notwendigen Gene für eine Replikation, dafür aber verschiedene, aus dem Genom der Schlupfwespe abgeleitete Virulenzfaktoren, darunter verkürzte Versionen mit Homologie zu Genen der Raupe, die deren Funktion hemmen.[10] Das Virus moduliert das Immunsystem, den Stoffwechsel und das Verhalten der parasitierten Raupe, ohne darin repliziert zu werden. Polydnaviren und Schlupfwespen haben somit einen symbiotischen Mutualismus, denn das Virus dient als Vektor für den transienten Gentransfer, während die Wespen nur in ihren Eierstöcken für dessen Vermehrung sorgen.
Hemmung der Abwehrreaktionen
Die Modulation der Immunreaktion auf die injizierten Eier in den parasitierten Wirten verhindert die üblicherweise eintretende Abwehrreaktion. Diese besteht aus einer Verkapselung der Eier mit den Hämatozyten des Mixocoels, die anschließend durch weitere Hämatozyten über die Phenoloxidase mit Melanin die Sauerstoffversorgung des Fremdkörpers mindert, wodurch die Entwicklung eines Pathogens verlangsamt oder beendet wird. Polydnaviren können darüber hinaus unter anderem durch Hemmung von NF-κB in Hämatozyten diese inaktivieren oder zerstören, was diese Abwehr schwächt.[11] Das Polydnavirus von Cotesia rubecula codiert das Protein CrV1, welches Aktin-Filamente in Hämatozyten depolymerisiert, wodurch deren Beweglichkeit und Stabilität eingeschränkt wird.[12] Das Bracovirus des Microplitis demolitor (MdBV) induziert die Apoptose in Hämatozyten durch PTP-H2, wodurch weniger Abwehr erfolgt und mehr flüssige Nahrung zur Verfügung steht.[12] Weiterhin wird die Phagozytose und Adhäsion der Hämatozyten durch das Gen GLC1.8 gemindert, was die Abwehr weiter mindert.[13] Durch Egf1.0 wird die Phenoloxidase inhibiert, was die Melaninbildung im Zuge der Immunabwehr unterbindet.[14]
Das Protein Ankyris hemmt die Wirkung antiviraler Peptide.[15] In manchen Ichnoviren hemmt Vankyrin die Induktion der Apoptose.[16][17] Das virale Innexin-verwandte Protein Vinnexin verändert die Kommunikation zwischen den Zellen der Raupe an den Gap Junctions.[18] Darüber hinaus induzieren Polydnaviren im Wirt eine Hyperglycämie, was das Nahrungsangebot für die Schlupfwespenlarven verbessert.[19]
Weiterhin führen Polydnaviriforme zu Verhaltensänderungen in den parasitierten Raupen, welche nach einer Infektion das Wandern und die Verpuppung unterlassen,[19] um die aus ihr geschlüpften und sich verpuppenden Schlupfwespenlarven vor Fraßfeinden oder anderen Parasitoiden zu beschützen, bis die eigenen Energiereserven aufgebraucht sind und die Raupe verstirbt.[20] Polydnaviren sind der erste bekannte Fall eines Gentransfervektors, der von Parasitoiden neben der Modulation des Immunsystems und des Stoffwechsels zu Verhaltensänderungen im Wirt genutzt wird. Weiterhin ist es der erste bekannte Fall, dass Wirte bis zur Selbstaufgabe die Nachkommen ihrer Parasiten oder Parasitoiden außerhalb ihres Körpers beschützen.
Virus-like particles
Manche Polydnaviroforme produzieren nur Virus-like particles (VLP) ohne enthaltene Nukleinsäuren, die an sich schon die Immunreaktion dämpfen, z. B. bei Venturia canescens (Ichneumonoidea) und Leptopilina sp. (Figitidaea). Die VLP des V. canescens (VcVLP1, VcVLP2, VcNEP …) werden in Calyxzellen produziert, um in den Eileiter entlassen zu werden. Da die DNA-Sequenzen der VLP-Proteine größere Ähnlichkeiten mit Hymenoptera-Proteinen als mit viralen Proteinen aufweist, ist ein nichtviraler Ursprung vermutet worden.[21]
Die Wespe Leptopilina heterotoma sezerniert VLP, welche die Lamellozyten penetrieren können.[22]
Vorkommen
Polydnaviriforme kommen in verschiedenen Unterfamilien der Schlupfwespen vor, darunter
- Bracoviriform bei:
- Ichnoviriform bei:
Systematik
Interne Systematik
Mit Stand Mitte April 2024 sind vom International Committee on Taxonomy of Viruses (ICTV) besteht die Familie Polydnaviridae aus den beiden folgenden Gattungen:[25][26]
Familie Polydnaviriformidae (früher Polydnaviridae)
- Gattung Bracoviriform (früher Bracovirus, BV, Bracoviren)[27]
- Gattung Ichnoviriform (früher Ichnovirus, IV, Ichnoviren)[28]
Externe Systematik
Nukleinsäureanalysen legen eine sehr lange Verbindung der Viren mit den Wespen nahe (mehr als 70 Millionen Jahre).
Bezüglich der Co-Evolution der Wespen und der Viren wurden zwei gegensätzliche Vorschläge unterbreitet.
- Der erste Vorschlag geht von der Annahme aus, dass das Virus von Wespengenen abstammt. Viele parasitoide Wespen, die keine Polydnaviriforme verwenden, injizieren Proteine mit viele gleichwertige Funktionen haben, d. h. die Immunantwort des Wirts auf das Parasitenei unterdrücken und deshalb englisch Virus-like particles (VLPs) genannt werden (siehe unten). In diesem Modell haben die braconiden und ichneumoniden Wespen Gene für diese Funktionen in die Viren verpackt – was im Wesentlichen zu einem Gentransfersystem führt, bei dem die Raupe selbst die immunsuppressiven Faktoren produziert. In diesem Szenario wurden die Strukturproteine der Viren (Kapside) wahrscheinlich von vorhandenen Viren „entlehnt“.
- Der alternative Vorschlag nimmt an, dass Wespenvorfahren eine vorteilhafte Symbiose mit einem vorhandenen Virus entwickelten, die schließlich zur Integration des Virus in das Genom der Wespe führte. Die für die Virusreplikation und die Kapside verantwortlichen Gene waren dann unnötig und irgendwann nicht mehr im Virus-Genom enthalten.
Diese zweite Hypothese wird durch die unterschiedlichen Morphologien zwischen IV und BV gestützt, was auf unterschiedliche Abkunft der beiden Gattungen schließen lässt. Die IV weisen bemerkenswerte Ähnlichkeiten mit Ascoviren auf und haben sich vermutlich aus diesen entwickelt,[29] während sich die BV möglicherweise vor etwa 100 Millionen Jahren aus den Nudiviridae entwickelt haben.[30][31] Die Polydnaviridae (d. h. die Gruppe der Bracoviren) scheinen nach Koonin et al. (2015 und 2019) zusammen mit den Nimaviridae, Hytrosaviridae, Baculoviridae und den Nudiviridae eine noch unbenannte Verwandtschaftsgruppe zu bilden, für die die Autoren folgenden Stammbaum vorschlagen:[32][33]
| Naldaviricetes |
| |||||||||||||||||||||
Die beiden Virusgattungen in der Familie sind nach Dupuy et al. (2006) nicht phylogenetisch verwandt, was bedeutet, dass dieses Taxon möglicherweise überarbeitet werden muss,[34] was bislang (Stand Mitte April 2024) aber noch nicht geschehen ist. Die Polydnaviriformdae ohne Ichnoviriform sind (wie vermutet) entweder eine Schwesterklade der Baculoviridae oder der Gattung Deltanudivirus (mit Tiplua oleracea nudivirus, ToNV) innerhalb der Nudiviridae.[35]
Weblinks
- Video über Verhaltensänderungen in der Schlupfwespenbeute (englisch). Abgerufen am 22. Juni 2012.
Einzelnachweise
- ↑ ICTV: ICTV Master Species List 2019.v1, New MSL including all taxa updates since the 2018b release, March 2020 (MSL #35)
- ↑ B. A. Federici, Y. Bigot: Origin and evolution of polydnaviruses by symbiogenesis of insect DNA viruses in endoparasitic wasps. In: J Insect Physiol. (2003), Bd. 49(5), S. 419–32. PMID 12770621.
- ↑ J. B. Whitfield: Estimating the age of the polydnavirus/braconid wasp symbiosis. In: Proceedings of the National Academy of Sciences. Band 99, Nummer 11, Mai 2002, S. 7508–7513, ISSN 0027-8424. doi:10.1073/pnas.112067199. PMID 12032313. PMC 124262 (freier Volltext).
- ↑ E. A. Herniou, E. Huguet, J. Thézé, A. Bézier, G. Periquet, J. M. Drezen: When parasitic wasps hijacked viruses: genomic and functional evolution of polydnaviruses. In: Philosophical transactions of the Royal Society of London. Series B, Biological sciences. Band 368, Nummer 1626, September 2013, S. 20130051, ISSN 1471-2970. doi:10.1098/rstb.2013.0051. PMID 23938758. PMC 3758193 (freier Volltext).
- ↑ J. M. Drezen, B. Provost, E. Espagne, L. Cattolico, C. Dupuy, M. Poirié, G. Periquet, E. Huguet: Polydnavirus genome: integrated vs. free virus. In: J Insect Physiol. (2003), Bd. 49(5), S. 407–17. PMID 12770620.
- ↑ J. G. Fleming, M. D. Summers: Polydnavirus DNA is integrated in the DNA of its parasitoid wasp host. In: Proceedings of the National Academy of Sciences. Band 88, Nummer 21, November 1991, S. 9770–9774, ISSN 0027-8424. PMID 1946402. PMC 52802 (freier Volltext).
- ↑ a b c Polydnaviridae, auf: ViralZone, Swiss Institute of Bioinformatics (SIB)
- ↑ B. A. Webb, M. R. Strand, S. E. Dickey, M. H. Beck, R. S. Hilgarth, W. E. Barney, K. Kadash, J. A. Kroemer, K. G. Lindstrom, W. Rattanadechakul, K. S. Shelby, H. Thoetkiattikul, M. W. Turnbull, R. A. Witherell: Polydnavirus genomes reflect their dual roles as mutualists and pathogens. In: Virology. Band 347, Nummer 1, März 2006, S. 160–174, ISSN 0042-6822. doi:10.1016/j.virol.2005.11.010. PMID 16380146.
- ↑ J. G. Fleming, M. D. Summers: Polydnavirus DNA is integrated in the DNA of its parasitoid wasp host. In: Proceedings of the National Academy of Sciences. Band 88, Nummer 21, November 1991, S. 9770–9774, ISSN 0027-8424. PMID 1946402. PMC 52802 (freier Volltext).
- ↑ E. Espagne, C. Dupuy, E. Huguet, L. Cattolico, B. Provost, N. Martins, M. Poirié, G. Periquet, J. M. Drezen: Genome sequence of a polydnavirus: insights into symbiotic virus evolution. In: Science. Band 306, Nummer 5694, Oktober 2004, S. 286–289, ISSN 1095-9203. doi:10.1126/science.1103066. PMID 15472078.
- ↑ H. Thoetkiattikul, M. H. Beck, M. R. Strand: Inhibitor kappaB-like proteins from a polydnavirus inhibit NF-kappaB activation and suppress the insect immune response. In: Proc Natl Acad Sci U S A (2005), Bd. 102(32), S. 11426–31. PMID 16061795; PMC 1183600 (freier Volltext).
- ↑ a b JM. Drezen, S. Savary, M. Poirier, G. Periquet. Polydnaviruses, viral entities domesticated by the parasitoid wasps, Virologie. Volume 3, Number 1, 11-21, Janvier-Février 1999.
- ↑ M. Beck, M. R. Strand: Glc1.8 from Microplitis demolitor bracovirus induces a loss of adhesion and phagocytosis in insect high five and S2 cells. In: J Virol. (2005), Bd. 79(3), S. 1861–70. PMID 15650210; PMC 544146 (freier Volltext).
- ↑ M. H. Beck, M. R. Strand: A novel polydnavirus protein inhibits the insect prophenoloxidase activation pathway. In: Proc Natl Acad Sci U S A (2007), Bd. 104(49), S. 19267–72. PMID 18032603; PMC 2148279 (freier Volltext).
- ↑ Bae Sungwoo; Kim Yonggyun: IkB genes encoded in Cotesia plutellae bracovirus suppress an antiviral response and enhance baculovirus pathogenicity against the diamondback moth, Plutella xylostella. In: Journal Of Invertebrate Pathology (2009), Bd. 102(1), S. 79–87. ISSN 0022-2011
- ↑ Fath-Goodin A.; Kroemer J. A.; Webb B. A.: The Campoletis sonorensis ichnovirus vankyrin protein P-vank-1 inhibits apoptosis in insect Sf9 cells. In: Insect Mol Biol (2009), Bd. 18(4), S. 497–506
- ↑ G. Clavijo, T. Dorémus, M. Ravallec, M. A. Mannucci, V. Jouan, A. N. Volkoff, I. Darboux: Multigenic families in Ichnovirus: a tissue and host specificity study through expression analysis of vankyrins from Hyposoter didymator Ichnovirus. In: PloS one. Band 6, Nummer 11, 2011, S. e27522, ISSN 1932-6203. doi:10.1371/journal.pone.0027522. PMID 22087334. PMC 3210807 (freier Volltext).
- ↑ N. K. Marziano, D. K. Hasegawa, P. Phelan, M. W. Turnbull: Functional interactions between polydnavirus and host cellular innexins. In: Journal of virology. Band 85, Nummer 19, Oktober 2011, S. 10222–10229, ISSN 1098-5514. doi:10.1128/JVI.00691-11. PMID 21813607. PMC 3196458 (freier Volltext).
- ↑ a b A. J. Pruijssers, P. Falabella, J. H. Eum, F. Pennacchio, M. R. Brown, M. R. Strand: Infection by a symbiotic polydnavirus induces wasting and inhibits metamorphosis of the moth Pseudoplusia includens. In: J Exp Biol. (2009), Bd. 212(18), S. 2998–3006. PMID 19717683; PMC 2734494 (freier Volltext).
- ↑ A. H. Grosman, A. Janssen, E. F. de Brito, E. G. Cordeiro, F. Colares, J. O. Fonseca, E. R. Lima, A. Pallini, M. W. Sabelis: Parasitoid increases survival of its pupae by inducing hosts to fight predators. In: PLoS One (2008), Bd. 3(6), S. e2276. PMID 18523578; PMC 2386968 (freier Volltext).
- ↑ A. Reineke, S. Asgari, O. Schmidt: Evolutionary Origin of V enturia canescens Virus-Like Particles, In: Archives of Insect Biochemistry and Physiology (2006), 61:123-133.
- ↑ R. M. Rizki, T. M. Rizki: Parasitoid virus-like particles destroy Drosophila cellular im munity, In: Proceedings of the National Academy of Sciences (1990), Bd. 87, S. 8388–8392.
- ↑ Nicholas Murphy, Jonathan C. Banks, James B. Whitfield, Andrew D. Austin: Phylogeny of the parasitic microgastroid subfamilies (Hymenoptera: Braconidae) based on sequence data from seven genes, with an improved time estimate of the origin of the lineage. In: Molecular Phylogenetics and Evolution. 47. Jahrgang, Nr. 1, 1. April 2008, S. 378–395, doi:10.1016/j.ympev.2008.01.022 (englisch, sciencedirect.com).
- ↑ a b c d e f g Gaelen R. Burke, Michael R. Strand: Polydnaviruses of Parasitic Wasps: Domestication of Viruses To Act as Gene Delivery Vectors. In: Insects. 3. Jahrgang, Nr. 1, 31. Januar 2012, S. 91–119, doi:10.3390/insects3010091, PMID 26467950, PMC 4553618 (freier Volltext) – (englisch, mdpi.com).
- ↑ ICTV: Taxonomy Browser.
- ↑ ICTV: Virus Metadata Resource (VMR).
- ↑ SIB: Bracovirus, auf: ViralZone
- ↑ SIB: Ichnovirus, auf: ViralZone
- ↑ B. A. Federici, D. K. Bideshi, Y. Tan, T. Spears, Y. Bigot: Ascoviruses: superb manipulators of apoptosis for viral replication and transmission. In: Current Topics in Microbiology and Immunology. Band 328, 2009, ISBN 978-3-540-68617-0, S. 171–196, doi:10.1007/978-3-540-68618-7_5, PMID 19216438.
- ↑ Herniou EA, Huguet E, Thézé J, Bézier A, Periquet G, Drezen JM: When parasitic wasps hijacked viruses: genomic and functional evolution of polydnaviruses. In: Philos Trans R Soc Lond B Biol Sci. 368. Jahrgang, Nr. 1626, 2013, doi:10.1098/rstb.2013.0051, PMID 23938758, PMC 3758193 (freier Volltext) – (englisch).
- ↑ A. Bézier, M. Annaheim, J. Herbinière, C. Wetterwald, G. Gyapay, S. Bernard-Samain, P. Wincker, I. Roditi, M. Heller, M. Belghazi, R. Pfister-Wilhem, G. Periquet, C. Dupuy, E. Huguet, A. N. Volkoff, B. Lanzrein, J. M. Drezen: Polydnaviruses of braconid wasps derive from an ancestral nudivirus. In: Science (2009), Bd. 323(5916), S. 926–30, PMID 19213916, doi:10.1126/science.1166788.
- ↑ Eugene V. Koonin, Natalya Yutin: Evolution of the Large Nucleocytoplasmatic DNA Viruses of Eukaryotes and Convergent Origins of Viral Gigantism, in: Advances in Virus research, Band 103, AP 21. Januar 2019, doi:10.1016/bs.aivir.2018.09.002, S. 167–202
- ↑ Eugene V. Koonin, Valerian V. Dolja, Mart Krupovic: Origins and evolution of viruses of eukaryotes: The ultimate modularity, in: Virology Mai 2015; 479–480. 2–25. PMC 5898234 (freier Volltext), PMID 25771806.
- ↑ Dupuy C, Huguet E, Drezen JM: Unfolding the evolutionary story of polydnaviruses. In: Virus Res. 117. Jahrgang, Nr. 1, 2006, S. 81–89, doi:10.1016/j.virusres.2006.01.001, PMID 16460826 (englisch).
- ↑ Annie Bézier, Julien Thézé, Frederick Gavory, Julien Gaillard, Julie Poulain, Jean-Michel Drezen, Elisabeth A. Herniou: The Genome of the Nucleopolyhedrosis-Causing Virus from Tipula oleracea Sheds New Light on the Nudiviridae Family. In: Journal of Virology, 2014, doi:10.1128/JVI.02884-14, PMID 25540386 (englisch).
Auf dieser Seite verwendete Medien
Autor/Urheber: en:User:Ikehiker (original); Pbroks13 (talk) (redraw), Lizenz: CC BY-SA 4.0
Diagram of a Polydnavirus host association.
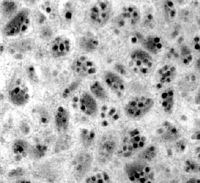
Virus particles of G. indiensis polydnavirus. The virions are formed by 5 to 10 nucleocapsids enclosed by only one viral envelope.

