Phosphonate

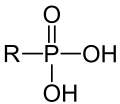
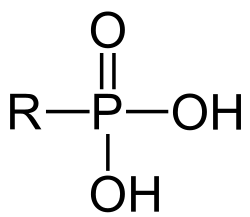
Als Phosphonate werden die Salze und Ester der Phosphonsäure H-P(O)(OH)2 – oder daraus abgeleitete organische Phosphonsäuren R-PO(OH)2 (R = Alkyl-Rest oder Aryl-Rest) — bezeichnet.[1] Es existieren primäre und sekundäre Phosphonate, bei denen entsprechend ein bzw. beide Wasserstoffatome der OH-Gruppen durch eine Metallion, bzw. durch einen organischen Rest ersetzt wurden: H-P(O)(OH)(OM') bzw. H-P(O)(OH)(OR') und H-P(O)(OM')2 bzw. H-P(O)(OR')2 (M'=einwertiges Metall, R'=organischer Rest).[2][1] Wie bei organischen Phosphaten liegen bei den Estern C-O-P-Bindungen vor, die sich im Vergleich zu C-P-Bindungen viel leichter hydrolysieren lassen. In Verbindungen dieses Typs sind die Eigenschaften eines Salzes (bzw. einer Säure) mit den Eigenschaften von organischen Verbindung verknüpft. So gibt es viele Verbindungen dieses Typs, die in Wasser löslich sind. Formal sind Verbindungen vom Typ R-PO(OH)2 keine Phosphonate, sondern zählen zu den organische Phosphonsäuren.[3]
Technische Anwendungen
Ein wichtiger industrieller Gebrauch von Phosphonsäuren und Phosphonaten ist in Kühlwassersystemen, Entsalzungsanlagen und bei der Ölförderung, wo sie die Ausfällung von Salzen verhindern. In der Papier- und Textilindustrie werden sie als Stabilisator für die Peroxidbleiche eingesetzt und komplexieren dort Metalle, welche sonst das Peroxid inaktivieren würden.[4]
In Waschmitteln werden sie als eine Kombination von Komplexbildnern, zur Verhinderung von Ausfällungen und als Stabilisator für Bleichmittel eingesetzt. Sie können ähnliche Eigenschaften wie EDTA haben und als Ersatz von Pentanatriumtriphosphat dienen. Sie sind Komplexbildner und dienen vor allem als Wasserenthärter. Als Builder können sie den Ionentauscher bzw. den Enthärter Zeolith A als Carrier unterstützen. Sie können als Korrosionsinhibitoren mitwirken oder als Stabilisator für Peroxide (z. B. in Bleichmitteln) dienen.[4] 1998 wurden weltweit etwa 56.000 Tonnen Phosphonate verwendet – 40.000 Tonnen in den USA, 15.000 Tonnen in Europa und weniger als 800 Tonnen in Japan.[4]
In der Medizin

Phosphonate werden in der Medizin verwendet, vor allem zur Behandlung von Knochenkrankheiten und von Ca-Metabolismus-Störungen.[4] Unter Bisphosphonaten wird in der Medizin Verbindungen der Phosphonsäure mit der allgemeinen Konstitutionsformel ((O3P)2-C-R1R2)4− verstanden. Sie sind Analoga zu Diphosphaten (Pyrophosphate) (O3P-O-PO3)4− und greifen in die Calcium-Homöostase ein. Sie werden daher unter anderem zur Behandlung der Osteoporose und von Knochenmetastasen eingesetzt.
Synthese
Mono- und Dialkylphosphonate sind über die Michaelis-Arbuzov-Reaktion darstellbar.[5][6] Alkylphosphonate sowie α-halogenierte Phosphonate können durch die Michaelis-Becker-Reaktion dargestellt werden.[7]
Umweltverträglichkeit
Die biologische Abbaubarkeit von Phosphonaten gilt als schlecht, selbst unter anaeroben (Sauerstoffausschluss) Bedingungen. Sie gelten auf aquatische Lebewesen als mäßig toxisch.[8] Phosphonate werden über das Abwasser in die Gewässer eingetragen, wobei der überwiegende Teil aus dem Einsatz in Wasch- und Reinigungsmitteln stammt.[9] Zwei Fallstudien zeigen, dass Phosphonate in relevanten Mengen nicht in Kläranlagen abgeschieden werden und sich in der aquatischen Umwelt akkumulieren können.[9] Weitere Fallstudien zeigen die Absorption von Phosphonaten an Feststoffpartikel sowohl in der Kläranlage als auch im Fließgewässer. So wurden an den Kläranlagen-Einleitstellen signifikant erhöhte Sedimentbeladungen und zum Teil erhöhte Schwebstoffbeladungen festgestellt.[10]
Die Wasser 3.0 gGmbH fasst die Umweltverträglichkeit von Phosphonaten wie folgt zusammen (Stand 2021): „Die Frage nach akkumulativen Eigenschaften in der Umwelt … kann daher derzeit nicht eindeutig beantwortet werden. Weiterhin kann weder eine erhöhte noch keine Beeinträchtigung der Umwelt durch synthetische Phosphonate angenommen bzw. ausgeschlossen werden“.[8]
Literatur
- Philippe Savignac, Bogdan Iorga: Modern Phosphonate Chemistry. CRC Press, 2003, ISBN 0-203-50367-8.
Einzelnachweise
- ↑ a b Eintrag zu Phosphonate und Phosphite. In: Römpp Online. Georg Thieme Verlag, abgerufen am 14. November 2021.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 794–795.
- ↑ Eintrag zu Phosphor-organische Verbindungen. In: Römpp Online. Georg Thieme Verlag, abgerufen am 14. November 2021.
- ↑ a b c d Eugenia Valsami-Jones: Phosphorus in Environmental Technology: Principles and Applications. IWA Publishing, 2004, ISBN 978-1-84339-001-5, S. 149 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Timothy Carl Radsick: The Use of Functionalized Monoalkyl Phosphates and Phosphonates in the ... ProQuest, 2007, ISBN 978-0-549-39821-9, S. 36 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Abraham Clearfield, Konstantinos D. Demadis: Metal Phosphonate Chemistry: From Synthesis to Applications. Royal Society of Chemistry, 2011, ISBN 978-1-84973-356-4, S. 172 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Robert Engel: Handbook of organophosphorus Chemistry. CRC Press, 1992, ISBN 0-8247-8733-1, S. 280 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Mikroschadstoff-Special: Phosphonate - Über Wasch- und Reinigungsmittel, Pestizide sowie Antiscalante in die Umwelt. In: wasserdreinull.de. Abgerufen am 25. Februar 2026 (deutsch).
- ↑ a b Happel, O.; Armbruster, D.; Rott, E.; Minke, R.; Gast, M.: Phosphonate in Wasch- und Reinigungsmitteln und deren Verbleib in der Umwelt. In: tzw.de. DVGW - Technologiezentrum Wasser, 2018, abgerufen am 25. Februar 2026.
- ↑ Oliver Happel, Dominic Armbruster, Heinz-Jürgen Brauch, Eduard Rott, Ralf Minke: Phosphonate in Wasch- und Reinigungsmitteln und deren Verbleib in der Umwelt – Entwicklung von Analyseverfahren und deren praktische Anwendung bei Proben von Oberflächenwasser, Abwasser und Sediment. In: umweltbundesamt.de. Umweltbundesamt, 1. Mai 2021, abgerufen am 25. Februar 2026.
Auf dieser Seite verwendete Medien
Allgemeine Struktur der Phosphonate
Alendronsäure; Alendronat
Struktur von Phosphonsäure (Phosphorige Säure)