Natriumtetrafluoroborat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
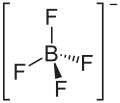 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Natriumtetrafluoroborat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | Na[BF4] | |||||||||||||||
| Kurzbeschreibung | kristalliner, farbloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 109,80 g·mol−1 | |||||||||||||||
| Aggregatzustand | fest | |||||||||||||||
| Dichte | 2,47 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | 384 °C[1] | |||||||||||||||
| Löslichkeit | sehr leicht in Wasser (1080 g·l−1 bei 26 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Natriumtetrafluoroborat ist eine chemische Verbindung aus der Gruppe der Natriumverbindungen, Bor-Halogen-Verbindungen und Fluorkomplexe.
Gewinnung und Darstellung
Wie die meisten der üblichen Tetrafluoroborate kann Natriumtetrafluoroborat durch Reaktion bzw. Neutralisation von Natriumhydroxid oder Natriumcarbonat mit der Tetrafluoridoborsäure umgesetzt werden.
Eigenschaften
Natriumtetrafluoroborat ist ein nicht brennbarer weißer kristalliner Feststoff, welcher sehr leicht in Wasser löslich ist und sich dabei langsam zersetzt.[1]
Verwendung
Natriumtetrafluoroborat wird auch als Schutzmittel beim Sandformgießen von Magnesiumlegierungen genannt.[2] Üblicher ist aber die Verwendung von Borsäure als Zusatz zur Formsandmischung.
Alkalimetallfluoroborate allgemein werden in Flussmitteln für Lötung und Hartlötung verwendet und als Katalysatoren in organischen Synthesen und Polymerisationsreaktionen eingesetzt.[3] In Aluminiumgiessereien werden die Fluoroborate, ebenso wie die Fluorotitanate den Schmelzen als Bestandteil von Produkten zur kornfeinenden Gefügebeeinflussung zugesetzt (siehe Schmelzebehandlung).
Einzelnachweise
- ↑ a b c d e f g Eintrag zu Natriumtetrafluorborat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Januar 2019. (JavaScript erforderlich)
- ↑ Oleg Podobed: Entwicklung von Sandformtechnologien für die Fertigung von Prototypen und Gussteilen aus Magnesiumlegierungen, Dissertation, Technische Universität Bergakademie Freiberg, 2003, urn:nbn:de:swb:105-1910983.
- ↑ Toxikologische Bewertung von Tetrafluorborsäure und Salze (PDF) bei der Berufsgenossenschaft Rohstoffe und chemische Industrie (BG RCI), abgerufen am 22. August 2012.
Auf dieser Seite verwendete Medien
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Struktur des Na+-Ions
Struktur von Tetrafluoroborat-Ion



