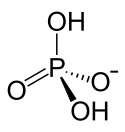
Natriumdihydrogenphosphat
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Natriumdihydrogenphosphat | ||||||||||||
| Andere Namen | |||||||||||||
| Summenformel | NaH2PO4 | ||||||||||||
| Kurzbeschreibung | |||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 119,98 g·mol−1 (wasserfrei) 138,00 g·mol−1 (Monohydrat) 156,01 g·mol−1 (Dihydrat) | ||||||||||||
| Aggregatzustand | fest | ||||||||||||
| Dichte | |||||||||||||
| Schmelzpunkt | |||||||||||||
| pKS-Wert | 7,21[6] | ||||||||||||
| Löslichkeit | sehr gut in Wasser (850 g·l−1 bei 20 °C)[3] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Toxikologische Daten | |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Natriumdihydrogenphosphat ist ein farb- und geruchloses Salz aus den Ionen Na+ und H2PO4−.
Gewinnung und Darstellung
Natriumdihydrogenphosphat wird, wie andere Phosphate auch, aus Erzen, wie beispielsweise Apatit gewonnen.
Im Labor kann die Darstellung durch die Neutralisation von Natronlauge mit Phosphorsäure erfolgen:
Das Dihydrat kann rein aus einer kalten Wasser/Ethanollösung kristallisiert werden.[8]
Eigenschaften
Neben der wasserfreien Verbindung treten noch das Monohydrat (NaH2PO4 · H2O) und das Dihydrat (NaH2PO4 · 2 H2O) auf.
Natriumdihydrogenphosphat reagiert, in Wasser gelöst, sauer (pH 4,5 bei 12 g/l, 25 °C).
Verwendung
Abführmittel
Natriumdihydrogenphosphat ist arzneilich wirksamer Bestandteil von Laxantien.
Pharmazeutischer Hilfsstoff
Natriumdihydrogenphosphat ist als Pharmazeutischer Hilfsstoff Bestandteil von Medikamenten, die in wässriger Form verabreicht werden (z. B. Nasensprays).
Lebensmitteltechnik
In der Lebensmitteltechnik wird Natriumdihydrogenphosphat als Komplexbildner, Säureregulator und Schmelzsalz eingesetzt. Es ist zusammen mit Dinatriumhydrogenphosphat und Natriumphosphat in der EU als Lebensmittelzusatzstoff unter der gemeinsamen Nummer E 339 („Natriumphosphate“) für bestimmte Lebensmittel mit jeweils unterschiedlichen Höchstmengenbeschränkungen zugelassen. Nach der Zusatzstoff-Zulassungsverordnung sind dies – für die meisten zugelassenen Phosphate weitgehend einheitliche – einzelne Festlegungen für eine breite Palette mit zahlreichen unterschiedlichen Lebensmittelsorten. Die zugelassenen Höchstmengen variieren von 0,5 bis hin zu 50 Gramm pro Kilogramm (in Getränkeweißer für Automaten) oder auch dem Fehlen einer festen Beschränkung (quantum satis – nach Bedarf, bei Nahrungsergänzungsmitteln und teils bei Kaugummis). Phosphor steht im Verdacht Hyperaktivität, allergische Reaktionen und Osteoporose auszulösen. Es wurde eine erlaubte Tagesdosis von 70 Milligramm pro Kilogramm Körpergewicht für die Gesamtmenge aufgenommener Phosphorsäure und Phosphate festgelegt.
Phosphatpuffer
Natriumdihydrogenphosphat findet in der Biochemie und Molekularbiologie zur Herstellung von Pufferlösungen Anwendung. Durch Mischen von Natriumdihydrogenphosphat- mit Dinatriumhydrogenphosphat-Lösung oder Zugabe von Natronlauge lässt sich ein Phosphatpuffer mit einem bestimmten pH-Wert (pH 6–8) herstellen.
Sicherheitshinweise
Natriumdihydrogenphosphat kann bei Augenkontakt leichte Reizungen hervorrufen. Es ist nicht brennbar, kann beim Glühen jedoch im weiteren Verlauf zur Freisetzung von Phosphoroxiden führen. Die LD50 für Ratten beträgt bei oraler Applikation 8290 mg/kg Körpergewicht. Die LD50 dermal bei Kaninchen beträgt >7940 mg/kg. Natriumdihydrogenphosphat ist schwach wassergefährdend: Wassergefährdungsklasse 1.
Einzelnachweise
- ↑ Eintrag zu E 339: Sodium phosphates in der Europäischen Datenbank für Lebensmittelzusatzstoffe, abgerufen am 29. Dezember 2020.
- ↑ Eintrag zu SODIUM PHOSPHATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 18. Januar 2022.
- ↑ a b c d Datenblatt Natriumdihydrogenphosphat bei Merck, abgerufen am 25. Dezember 2019.
- ↑ a b c Datenblatt Natriumdihydrogenphosphat (Monohydrat) bei Merck, abgerufen am 25. Dezember 2019.
- ↑ a b c Datenblatt Natriumdihydrogenphosphat (Dihydrat) bei Merck, abgerufen am 25. Dezember 2019.
- ↑ Eintrag zu Phosphorsäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. Mai 2014.
- ↑ a b Eintrag zu Natriumdihydrogenphosphat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 18. November 2022. (JavaScript erforderlich)
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 544.
Auf dieser Seite verwendete Medien
KHP simulated titration curve; phosphoric acid speciation, 3 pK values 2,16; 7,21; 12,32
Struktur des Na+-Ions