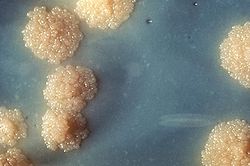
Mycobacterium tuberculosis
| Mycobacterium tuberculosis | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Mycobacterium tuberculosis | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Mycobacterium tuberculosis | ||||||||||||
| (Zopf 1883) Lehmann & Neumann 1896 |

Mycobacterium tuberculosis, deutsch auch Tuberkelbazillus genannt, ist ein Bakterium aus der Familie der Mycobacteriaceae (Mykobakterien). Es handelt sich um den wichtigsten Erreger der Tuberkulose beim Menschen. Auch Tiere können durch M. tuberculosis an Tuberkulose erkranken.
Eigenschaften
M. tuberculosis ist ein stäbchenförmiges, zur aktiven Bewegung unfähiges Bakterium. Die Bakterien sind, wie Robert Koch 1882 entdeckt[1] hatte, säurefest und lassen sich daher mit der Ziehl-Neelsen-Färbung sowie mit speziellen Fluoreszenzfarbstoff-Färbungen (z. B. Auramin-Färbung) mikroskopisch von nicht säurefesten Bakterien und anderen nicht säurefesten Objekten unterscheiden. Die Bakterienzellwand enthält unter anderem Arabinogalaktan und Mykolsäuren, die neben anderen lipophilen Zellwandbestandteilen für die Säurefestigkeit verantwortlich sind.
Weitere charakteristische Eigenschaften sind sein extrem langsames Wachstum (15 bis 20 Stunden bis zur Teilung), die Fähigkeit, schwachen Desinfektionsmitteln zu widerstehen, Aerobie und intrazelluläre Pathogenese. Das Bakterium besitzt die Fähigkeit, in Makrophagen (Fresszellen des Immunsystems) ruhend zu überleben und, nach Jahren wieder aufwachend, sich dann zu teilen (Dormanz). Auf genomischer Ebene codiert ein ungewöhnlich großer Teil seiner Gene die für die Produktion von lipolyse- (fettspaltenden) und lipogenesefähigen (Fettsynthese) Enzyme. Die Lipide in der Zellwand maskieren darunter liegende Molekülstrukturen, die in anderen Bakterien eine geeignete Immunantwort hervorrufen.[2] Zudem ist das Bakterium nicht nur in der Lage, von der eigenen in der Zellwand deponierten Fettschicht zu leben, sondern auch externes Cholesterin, das während der Infektion im Menschen gefunden wird, zu sammeln und zu verwerten.[3]
Intrazelluläre Pathogenese
M. tuberculosis hat mehrere Mechanismen entwickelt, um im Phagosom überleben zu können: er besitzt zunächst eine wachsartige, fettreiche Zellwand, die es ihm ermöglicht, sich gegen seine Zerstörung innerhalb der Immunabwehr zu wehren. Das Phagosom ist nicht in der Lage, die äußere Schicht der Zellwand des Erregers aufzuspalten. Außerdem enthält die äußere Wachsschicht Lipoarabinomannan (LAM), ein Glycolipid, das, zusammen mit einer Phosphatase die Signaltransduktion des Phagosoms stört, so dass diese nicht das volle Zerstörungsprogramm fährt.[4]
Des Weiteren werden vom Bakterium mehrere Enzyme (Katalase, Superoxid-Dismutase und andere) ausgeschieden, die jede Gefahr durch reaktive Sauerstoff- und Stickstoffspezies ausschalten (die Katalase wirkt auch als Peroxinitritase). Zuletzt bringt sich das Bakterium in einen winterschlafähnlichen Zustand (Dormanz), in dem keine DNA-Replikation und Zellteilung stattfindet, und der Organismus auf Sparflamme anaerob von der eigenen Fettschicht lebt. Dadurch werden viele Antibiotika unwirksam, die sonst in die normalen Zellprozesse eingreifen.[5][6]
Hinzu kommt eine erhöhte Mutationsrate durch Ablesefehler der DNA-Polymerase sowie durch von den Makrophagen erzeugte reaktive Sauerstoffspezies (ROS), die auch bei latenter Infektion die DNA des Bakteriums schädigen und zu Mutationen führen. Das bedeutet, dass das Bakterium auch dann Resistenzen entwickeln kann, wenn es sich nicht teilt.[7]
Infektion, Erkrankung, Therapie beim Menschen
Die Übertragung erfolgt in der Regel durch eine Tröpfcheninfektion. Die Haupteintrittspforte ist die Lunge. Die Infektion der Lungen führt zur Knötchenbildung und Zerstörung des Lungengewebes sowie zur Streuung tuberkulöser Herde im Körper. Unterernährte und geschwächte Menschen sind besonders anfällig für die Erkrankung. Heute ist etwa jeder dritte Mensch auf der Welt mit Mycobacterium tuberculosis infiziert. Vor allem in Dritte-Welt-Ländern fällt die Behandlung mit Antibiotika schwer, da sie sich über Monate hinzieht. Darüber hinaus gibt es immer mehr Fälle, bei denen der Erreger gegenüber vielen Antibiotika resistent ist. Jedes Jahr sterben an Tuberkulose 2 Millionen Menschen und sie ist neben AIDS und Malaria die weltweit am weitesten verbreitete Infektionskrankheit.
Infektion und Erkrankung bei Nutz- und Haustieren
Tiere infizieren sich stets durch an offener Tuberkulose erkrankte Menschen. Rinder sind dadurch nicht nur von der Variante M. bovis betroffen; in Äthiopien beispielsweise wurde bei bis zu einem Viertel der freilaufenden Tiere M. tuberculosis gefunden, während eingezäunte Tiere teilweise mit M. bovis infiziert waren. Ursache ist wahrscheinlich die Angewohnheit der dortigen Hirten, Rindern gekauten Tabak zur Parasitenbekämpfung ins Maul zu spucken.[8]
Beobachtet wurde eine Erkrankung weiters bei Schweinen, Pferden, Schafen und Ziegen. Hühner sind weitgehend resistent gegen M. tuberculosis. Bei erkrankten Tieren entwickelt sich meist nur ein schnell abheilender örtlicher Prozess. In solchen Fällen ist es angeraten, die betreuenden Menschen auf Tuberkulose zu untersuchen.
Wesentlich ernster ist die Infektion von Haustieren, die mit dem Menschen in enger häuslicher Gemeinschaft leben. Hunde, Katzen und möglicherweise Papageien werden zuerst von offen tuberkulösen Menschen angesteckt, entwickeln selbst eine meist offene Tuberkulose und bilden dadurch eine gefährliche Ansteckungsquelle für Menschen, die mit ihnen in Kontakt kommen.
Antibiotikaresistenz
M. tuberculosis ist aufgrund mehrerer Eigenschaften in der Lage, Antibiotika unschädlich zu machen. Insbesondere die Undurchlässigkeit der äußeren wachsartigen Zellwand führt dazu, dass Fremdstoffe nur über Transportproteine aufgenommen werden, die sehr selektiv sein können. Weiterhin sind mehrere der funktionierenden Antibiotika auf eine Aktivierung durch Bakterienenzyme angewiesen (Prodrug). Viele andere werden von Effluxpumpen effektiv aus der Zelle entfernt. Zuletzt sind die Angriffspunkte der Antibiotika durchweg Enzyme oder Ribosomen. Da an allen diesen Prozessen Proteine beteiligt sind, genügt oft eine Mutation an der entsprechenden Position im Protein, entweder einen Angriffspunkt zu beseitigen, aktivierende Enzyme zu deaktivieren, gehemmte Enzyme und Effluxpumpen zu überexprimieren, oder den Import zu spezialisieren, damit ein Antibiotikum seinen Effekt auf das Bakterium einbüßt und eine Resistenz entsteht. Im Folgenden eine Tabelle der bekannten Antibiotika bei M. tuberculosis mit ihren Wirk- und Resistenzmechanismen:[9]
| Antibiotikum | Wirkort | Resistenz- gen(e) | Resistenzmechanismus |
|---|---|---|---|
| Isoniazid, Ethionamid | (Prodrug) Fettsäuresynthese | katG, ahpC, ndh | Verlust der Aktivierung |
| inhA | Mutation am Angriffspunkt | ||
| Rifampicin | Elongation der mRNA-Transkription | rpoB | Mutation am Angriffspunkt |
| Pyrazinamid | (Prodrug) Trans-Translation[10] | pncA | Verlust der Aktivierung |
| Streptomycin | Initiation der Translation | rpsL | Mutation am Angriffspunkt |
| Ethambutol | Arabinogalactan-Biosynthese | embB, ? | Mutation am Angriffspunkt |
| Fluorchinolone | DNA-Replikation | gyrA, gyrB | Mutation am Angriffspunkt |
| ? | Effluxpumpen | ||
| MfpA | ? | ||
| Kanamycin | Translation | rrs | Verlust der Ribosemethylierung |
| eis | Abbau des Antibiotikums[11] | ||
| 4-Aminosalicylsäure | (Prodrug) ? | thyA? | ? |
| Makrolide | Translation | erm37 | Ribosom-Methylierung |
| Linezolid, PNU100480 | Initiation der Translation | (23S rRNA) | Mutation am Angriffspunkt |
| D-Cycloserin | Peptidoglykan-Synthese | alr | Mutation am Angriffspunkt |
| TMC207 | ATP-Synthese | atpE, ? | Mutation am Angriffspunkt |
| PA-824, OPC-67683 | (Prodrug) Lipid-Synthese? | Rv3547 | Verlust der Aktivierung |
| MetSox | Glutamat-Synthese | glnA1, glnA3 | Deletion einer Base mit folgender Überexpression[12] |
| Halicin (Arzneimittelzulassung noch nicht erfolgt.) |
Multiresistenz
Gebräuchliche Abkürzungen:
- MDR-TB: multiresistentes Tuberkulosebakterium
- XDR-TB: extrem resistentes Tuberkulosebakterium
Als multiresistent werden M. tuberculosis-Stämme bezeichnet, die mindestens eine Resistenz auf die TB-Standardantibiotika Isoniazid und Rifampicin aufweisen. Die erste größere MDR-TB-Epidemie fand Anfang der 1990er Jahre in New York statt und betraf hauptsächlich HIV-Infizierte und medizinisches Personal. Im Jahr 2007 waren weltweit etwa 20 Prozent aller Isolate multiresistent.[13][14]
Extrem resistent heißen diejenigen MDR-TB-Stämme mit zusätzlicher Resistenz gegen mindestens ein Fluorchinolon-Antibiotikum und mindestens eines der Medikamente Capreomycin, Kanamycin oder Amikacin. Einer der ersten XDR-TB-Ausbrüche fand 2005 in einem ländlichen Krankenhaus in KwaZulu-Natal statt. Die Gefahr solcher Epidemien ist nicht auf Afrika beschränkt, da XDR-TB inzwischen auf sechs Kontinenten zu finden ist und durchschnittlich im Jahr 2007 etwa 10 Prozent der MDR-TB-Fälle ausmachte.[14][15][16]
Mittlerweile treten auch bei Linezolid immer mehr Resistenzen auf.
Die Bezeichnung TDR-TB (totally drug resistant tuberculosis), die u. a. im Zusammenhang mit Tuberkulosefällen in Indien in die Diskussion gebracht wird,[17] ist von der Weltgesundheitsorganisation nicht anerkannt.[18]
Nachweis
Der Goldstandard beim Nachweis ist die Kultivierung im Labor auf einem selektiven Kulturmedium wie Lowenstein-Jensen-Agar und der mikroskopische Nachweis mittels Ziehl-Neelsen-Färbung. Es ist möglich, das Wachstum in Middlebrook 7H10 Agar zu beschleunigen. Unkonventionelle Ansätze sind mikrokalorische Detektion des langsamen Wachstums oder die Erkennung sehr kleiner Mengen typischer flüchtiger Ester (Methylphenylacetat, Methyl-p-anisat, Methylnicotinat) durch Honigbienen.[19][20]
Als neuer Goldstandard könnte sich die Analyse von hitzesterilisiertem Material mittels Massenspektrometrie entwickeln. Unter anderem aufgrund des unterschiedlichen Lipidprofils ist es so in kurzer Zeit und mit hoher Sicherheit möglich, zwischen einzelnen Mycobacterium-Arten zu differenzieren.[21]
Geschichte
Dass die Tuberkulose übertragbar ist, zeigte bereits 1865 der französische Arzt Jean-Antoine Villemin (1827–1892). Dennoch wurde sie weiterhin meist für eine konstitutionelle Erkrankung gehalten. Das Bakterium wurde 1882 von Robert Koch entdeckt und erstmals isoliert, womit Koch die Übertragung durch einen lebenden Mikroorganismus endgültig bewiesen hatte. Durch Kultur in Reinkultur und Tierexperimente konnte er in Form der Kochschen Postulate nachweisen, dass die Tuberkulose durch M. tuberculosis verursacht wird.
Im Blut von an akuter Miliartuberkulose Verstorbener wies Anton Weichselbaum im Jahr 1884 Tuberkelbazillen nach.[22]
Mycobacterium tuberculosis wird auf einen rund 40.000 Jahre alten Vorgänger zurückgeführt, auf den auch Mycobacterium leprae und Mycobacterium bovis zurückgeführt werden.[23]
Karl Flügge entwickelte 1897 die Theorie der Tröpfcheninfektion mit Tuberkelbazillen.[24]
Im Jahr 2019 wurde mit dem Molekül Halicin ein potentiell wirksames Antibiotikum gegen Mycobacterium tuberculosis gefunden.[25]
Meldepflicht
In Deutschland ist der direkte Nachweis von Mycobacterium tuberculosis namentlich meldepflichtig nach § 7 des Infektionsschutzgesetzes.[26] Die Meldepflicht gilt nur soweit der direkte Nachweis auf eine akute Infektion hinweist sowie nachfolgend für das Ergebnis der Resistenzbestimmung; vorab auch für den Nachweis säurefester Stäbchen im Sputum. Die Meldepflicht betrifft in erster Linie die Leitungen von Laboren (§ 8 IfSG).
In der Schweiz ist der positive und negative laboranalytische Befund von Erregern aus dem Mycobacterium tuberculosis-Komplex für Laboratorien meldepflichtig und zwar nach dem Epidemiengesetz (EpG) in Verbindung mit der Epidemienverordnung und Anhang 3 der Verordnung des EDI über die Meldung von Beobachtungen übertragbarer Krankheiten des Menschen.
Literatur
- Karl Bernhard Lehmann, Rudolf Otto Neumann: Atlas und Grundriss der Bakteriologie und Lehrbuch der speciellen bakteriologischen Diagnostik. Lehmann, München 1896.
- W. Köhler et al.: Medizinische Mikrobiologie. Urban & Fischer-Verlag München/Jena 2001, 8. Auflage, ISBN 3-437-41640-5
- I. Comas, S. Gagneux: The past and future of tuberculosis research. In: PLoS Pathog. Band 5, Nummer 10, Oktober 2009, S. e1000600, doi:10.1371/journal.ppat.1000600, PMID 19855821, PMC 2745564 (freier Volltext) (Review).
- Ulrike Roll: Tuberkelbazillus. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 1423 f.
- S. Hähner-Rombach: Das große Sterben – Seuchen machen Geschichte. Berlin 1995, S. 278 ff.
Weblinks
- Genom von Mtu ATCC 25618 / H37Rv beim Sanger-Institut (erstes sequenziertes Genom)
- TubercuList am EPFL (Genom-Datenbank; letztes Update 2011)
- TubercuList am Pasteur-Institut (Genom-Datenbank; letztes Update 2008-Oct)
- TB Database (vergleichende Genomik-Datenbank)
- SIB: Coryneform bacterias: two membrane (Gram+): Morphology typical of Mycobacterium tuberculosis – Zelle von Mycobacterium tuberculosis mit Spore, Interaktive Graphik von SwissBioPics
Einzelnachweise
- ↑ Paul Diepgen, Heinz Goerke: Aschoff/Diepgen/Goerke: Kurze Übersichtstabelle zur Geschichte der Medizin. 7., neubearbeitete Auflage. Springer, Berlin/Göttingen/Heidelberg 1960, S. 48.
- ↑ C. J. Cambier, Kevin K. Takaki u. a.: Mycobacteria manipulate macrophage recruitment through coordinated use of membrane lipids. In: Nature. 2013, doi:10.1038/nature12799.
- ↑ A. Brzostek, J. Pawelczyk u. a.: Mycobacterium tuberculosis is able to accumulate and utilize cholesterol. In: J. Bacteriol. Band 191, Nummer 21, November 2009, S. 6584–6591, ISSN 1098-5530. doi:10.1128/JB.00488-09. PMID 19717592. PMC 2795286 (freier Volltext).
- ↑ Briken V, Porcelli SA, Besra GS, Kremer L: Mycobacterial lipoarabinomannan and related lipoglycans: from biogenesis to modulation of the immune response. In: Mol. Microbiol. 53. Jahrgang, Nr. 2, Juli 2004, S. 391–403, doi:10.1111/j.1365-2958.2004.04183.x, PMID 15228522 (englisch).
- ↑ Hestvik AL, Hmama Z, Av-Gay Y: Mycobacterial manipulation of the host cell. In: FEMS Microbiol. Rev. 29. Jahrgang, Nr. 5, November 2005, S. 1041–50, doi:10.1016/j.femsre.2005.04.013, PMID 16040149 (englisch).
- ↑ Deretic V, Singh S, Master S, et al.: Mycobacterium tuberculosis inhibition of phagolysosome biogenesis and autophagy as a host defence mechanism. In: Cell. Microbiol. 8. Jahrgang, Nr. 5, Mai 2006, S. 719–27, doi:10.1111/j.1462-5822.2006.00705.x, PMID 16611222 (englisch).
- ↑ C. B. Ford, P. L. Lin u. a.: Use of whole genome sequencing to estimate the mutation rate of Mycobacterium tuberculosis during latent infection. In: Nat. Genet. Band 43, Nummer 5, Mai 2011, S. 482–486, ISSN 1546-1718. doi:10.1038/ng.811. PMID 21516081. PMC 310187 (freier Volltext).
- ↑ G. Ameni, M. Vordermeier u. a.: Mycobacterium tuberculosis infection in grazing cattle in central Ethiopia. In: Veterinary journal (London, England : 1997) Band 188, Nummer 3, Juni 2011, S. 359–361. doi:10.1016/j.tvjl.2010.05.005. PMID 20965132. PMC 310382 (freier Volltext).
- ↑ P. E. Almeida Da Silva, J. C. Palomino: Molecular basis and mechanisms of drug resistance in Mycobacterium tuberculosis: classical and new drugs. In: Journal of Antimicrobial Chemotherapy. Band 66, Nummer 7, Juli 2011, S. 1417–1430, ISSN 1460-2091. doi:10.1093/jac/dkr173. PMID 21558086. (Review).
- ↑ W. Shi, X. Zhang u. a.: Pyrazinamide inhibits trans-translation in Mycobacterium tuberculosis. In: Science. Band 333, Nummer 6049, September 2011, S. 1630–1632, ISSN 1095-9203. doi:10.1126/science.1208813. PMID 21835980.
- ↑ W. Chen, T. Biswas u. a.: Unusual regioversatility of acetyltransferase Eis, a cause of drug resistance in XDR-TB. In: Proceedings of the National Academy of Sciences of the United States of America. Band 108, Nummer 24, Juni 2011, S. 9804–9808. doi:10.1073/pnas.1105379108. PMID 21628583. PMC 3116390 (freier Volltext).
- ↑ P. Carroll, S. J. Waddell u. a.: Methionine sulfoximine resistance in Mycobacterium tuberculosis is due to a single nucleotide deletion resulting in increased expression of the major glutamine synthetase, GlnA1. In: Microbial Drug Resistance Band 17, Nummer 3, September 2011, S. 351–355, ISSN 1931-8448. doi:10.1089/mdr.2010.0125. PMID 21875360. PMC 3161625 (freier Volltext).
- ↑ T. R. Frieden, L. F. Sherman u. a.: A multi-institutional outbreak of highly drug-resistant tuberculosis: epidemiology and clinical outcomes. In: JAMA Band 276, Nummer 15, Oktober 1996, S. 1229–1235, ISSN 0098-7484. PMID 8849750.
- ↑ a b N. S. Shah, A. Wright u. a.: Worldwide emergence of extensively drug-resistant tuberculosis. In: Emerging Infect. Dis. Band 13, Nummer 3, März 2007, S. 380–387, ISSN 1080-6040. PMID 17552090. PMC 272591 (freier Volltext).
- ↑ M. C. Raviglione, I. M. Smith: XDR tuberculosis–implications for global public health. In: N. Engl. J. Med. Band 356, Nummer 7, Februar 2007, S. 656–659, ISSN 1533-4406. doi:10.1056/NEJMp068273. PMID 17301295.
- ↑ N. R. Gandhi, A. Moll u. a.: Extensively drug-resistant tuberculosis as a cause of death in patients co-infected with tuberculosis and HIV in a rural area of South Africa. In: The Lancet Band 368, Nummer 9547, November 2006, S. 1575–1580, ISSN 1474-547X. doi:10.1016/S0140-6736(06)69573-1. PMID 17084757.
- ↑ Katherine Rowland: Totally drug-resistant TB emerges in India – Discovery of a deadly form of TB highlights crisis of mismanagement. Website des Magazins Nature. Abgerufen am 18. Februar 2012.
- ↑ WHO:Drug-resistant tuberculosis – Frequently asked questions ( vom 23. Februar 2012 im Internet Archive). Webseite der Weltgesundheitsorganisation. Abgerufen am 18. Februar 2012
- ↑ O. Braissant, D. Wirz u. a.: "The heat is on": rapid microcalorimetric detection of mycobacteria in culture. In: Tuberculosis. Band 90, Nummer 1, Januar 2010, S. 57–59. doi:10.1016/j.tube.2009.11.001. PMID 19969505.
- ↑ D. M. Suckling, R. L. Sagar: Honeybees Apis mellifera can detect the scent of Mycobacterium tuberculosis. In: Tuberculosis. Band 91, Nummer 4, Juli 2011, S. 327–328. doi:10.1016/j.tube.2011.04.008. PMID 21546308.
- ↑ A. El Khéchine, C. Couderc u. a.: Matrix-assisted laser desorption/ionization time-of-flight mass spectrometry identification of mycobacteria in routine clinical practice. In: PLOS ONE. Band 6, Nummer 9, 2011, S. e24720, ISSN 1932-6203. doi:10.1371/journal.pone.0024720. PMID 21935444. PMC 3172293 (freier Volltext).
- ↑ Paul Diepgen, Heinz Goerke: Aschoff/Diepgen/Goerke: Kurze Übersichtstabelle zur Geschichte der Medizin. 7., neubearbeitete Auflage. Springer, Berlin/Göttingen/Heidelberg 1960, S. 48.
- ↑ Z Djelouadji, D Raoult, M Drancourt: Palaeogenomics of Mycobacterium tuberculosis: epidemic bursts with a degrading genome. Lancet Infect Dis. 13 June 2011, doi:10.1016/S1473-3099(11)70093-7.
- ↑ Paul Diepgen, Heinz Goerke: Aschoff/Diepgen/Goerke: Kurze Übersichtstabelle zur Geschichte der Medizin. 7., neubearbeitete Auflage. Springer, Berlin/Göttingen/Heidelberg 1960, S. 48.
- ↑ Julia Merlot: Kampf gegen Resistenzen: Künstliche Intelligenz entdeckt vielversprechendes Antibiotikum – Der Spiegel – Wissenschaft. Der Spiegel, abgerufen am 22. Februar 2020.
- ↑ Tuberkulose. RKI-Ratgeber. In: rki.de. Robert Koch-Institut, 21. Februar 2013, abgerufen am 18. März 2020 (Meldepflicht gemäß IfSG).
Auf dieser Seite verwendete Medien
Autor/Urheber: (of code) -xfi-, Lizenz: CC BY-SA 3.0
The Wikispecies logo created by Zephram Stark based on a concept design by Jeremykemp.
Dies ist eine Nahaufnahme einer Kultur von Mycobacterium tuberculosis, welche die Kolonienmorphologie des Organismus' aufzeigt. Besonders zu beachten ist die farblose, raue Oberfläche, welche eines typisches morphologisches Charakteristikum im Wachstum von Kolonien dieser Spezies Mycobacterium tuberculosis darstellt. Die makroskopische Examination des Wachstumsmusters der Kolonien ist immer noch einer von vielen Wegen, wie diese Mikroorganismen identifiziert werden können.