Molybdän(IV)-chlorid
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
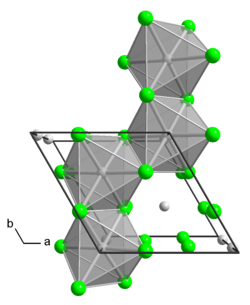 | |||||||||||||||||||
| _ Mo4+ _ Cl− Kristallstruktur von α-MoCl4 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Molybdän(IV)-chlorid | ||||||||||||||||||
| Andere Namen | Molybdäntetrachlorid | ||||||||||||||||||
| Verhältnisformel | MoCl4 | ||||||||||||||||||
| Kurzbeschreibung | schwarzer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 237,75 g·mol−1 | ||||||||||||||||||
| Aggregatzustand | fest[1] | ||||||||||||||||||
| Dichte | 3,193 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Molybdän(IV)-chlorid ist eine anorganische chemische Verbindung des Molybdäns aus der Gruppe der Chloride.
Gewinnung und Darstellung
Molybdän(IV)-chlorid kann durch Reaktion von Molybdän(V)-chlorid mit Benzol, Molybdän(III)-chlorid[1] oder Tetrachlorethylen[4] gewonnen werden.
Eigenschaften
Molybdän(IV)-chlorid ist ein paramagnetisches, licht-, luft- und feuchtigkeitsempfindliches schwarzes Pulver oder schwarz-braune, sechseckige Säulen. Es ist äußerst hydrolyseanfällig und löst sich rückstandslos mit gelber bis rotbrauner Farbe in Wasser, Ethanol und Ether. Beim Erhitzen über 180 °C im Vakuum ist es unter teilweiser Zersetzung in Molybdän(III)-chlorid und Molybdän(V)-chlorid flüchtig. Es besitzt eine trigonale Kristallstruktur mit der Raumgruppe P31c (Raumgruppen-Nr. 163), a = 605,8 pm, c = 1167,4 pm.[1][2] Die Verbindung (α-Form mit Ketten aus trans-kantenverknüpften MoCl6 Oktaedern) wandelt sich 250 °C in die β-Form um, welche aus Ringen von sechs cis-kantenverknüpften MoCl6 Oktaedern besteht.[5] In konzentrierter Salzsäure gelöst, bildet es mit Alkalichloriden Komplexsalze, wie zum Beispiel das apfelgrüne Caesiumpentachlorooxomolybdat(V) Cs2[MoOCl5].
Einzelnachweise
- ↑ a b c d e Georg Brauer: Handbuch der präparativen anorganischen Chemie. 3., umgearb. Auflage. Band 3. Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1533.
- ↑ a b c d Jean d’Ans, Ellen Lax, Roger Blachnik: Taschenbuch für Chemiker und Physiker. Springer DE, 1998, ISBN 3-642-58842-5, S. 574 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ E. L. McCann III and T. M. Brown: Molybdenum(IV) chloride. In: Robert W. Parry (Hrsg.): Inorganic Syntheses. Band 12. McGraw-Hill Book Company, Inc., 1970, ISBN 07-048517-8 (defekt), S. 181–186 (englisch).
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 1470.
Auf dieser Seite verwendete Medien
Autor/Urheber: Andif1, Lizenz: CC BY-SA 4.0
Crystal structure of molybdenum(IV) chloride. Created using Diamond 4. Data from Schaefer, H.; Baumann, H.; Tillack, J.V.; von Schnering, H.G.; Woehrle, H.; Kuhnen, F, Neue Untersuchungen ueber die Chloride das Molybdaens Zeitschrift fuer Anorganische und Allgemeine Chemie, 353, 281-310 (1967)
