Mellitsäureanhydrid
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
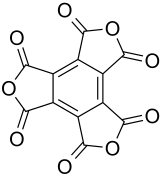 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Mellitsäureanhydrid | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C12O9 | ||||||||||||
| Kurzbeschreibung | weißer Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 288,13 g·mol−1 | ||||||||||||
| Aggregatzustand | fest[2] | ||||||||||||
| Dichte | |||||||||||||
| Schmelzpunkt | >320 °C (Zersetzung)[4] | ||||||||||||
| Löslichkeit |
| ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Mellitsäureanhydrid (genauer: Mellitsäuretrianhydrid) ist das Trianhydrid der Mellitsäure [Benzolhexacarbonsäure C6(COOH)6]. Dieses besteht nur aus Kohlenstoff und Sauerstoff und ist somit ein Kohlenstoffoxid (Dodecakohlenstoffnonaoxid).
Es ist ein weißer, im Vakuum[4] sublimierbarer Feststoff, den Liebig und Wöhler im Jahre 1830 in ihrer Studie über Mellit (Honigstein) isoliert haben und zunächst die Formel C4O3 zugewiesen haben.[1][7][8] Die Substanz wurde im Jahr 1913 von H. Meyer und K. Steiner charakterisiert.[9][4] Der Benzolring behält den aromatischen Charakter.[10][3]
Mellitsäureanhydrid kann verwendet werden, um die thermoplastischen Eigenschaften des Kunststoffs Polyethylenterephthalat (PET) zu verbessern[11] oder mit Cellulose[12] oder Collagen[13] verestert werden, um Produkte mit neuen Eigenschaften zu erhalten.
Einzelnachweise
- ↑ a b F. Wöhler: Ueber die Honigsteinsäure. In: Poggendorfs Annalen der Physik und Chemie, 1826, Bd. 83 (7), S. 325–334 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Eintrag zu Mellitsäuretrianhydrid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 21. November 2022. (JavaScript erforderlich)
- ↑ a b O. Ermer, J. Neudörfl: Structure of Mellitic Trianhydride. In: Helv. Chim. Acta, 2000, Bd. 83, S. 300–309; doi:10.1002/(SICI)1522-2675(20000119)83:1<300::AID-HLCA300>3.0.CO;2-L.
- ↑ a b c Bugge: Chemie: Ein neues Kohlenoxyd. In: Naturwissenschaftliche Wochenschrift, 1914, Bd. 13/29 (12), 22. März 1914, S. 188. Online-Version, abgerufen am 11. Dezember 2009.
- ↑ a b c d Hans Meyer, Karl Steiner: Über die Mellithsäure. In: Monatshefte für Chemie. Band 35, Nr. 5, Mai 1914, S. 475–518, doi:10.1007/BF01519380.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ J. Liebig, F. Wöhler: Ueber die Zusammensetzung der Honigsteinsäure. In: Poggendorfs Annalen der Physik und Chemie, 1830, Bd. 94 (2), S. 161–164 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ O. L. Erdmann, R. F. Marchand: Ueber die Mellithsäure. In: Journal für praktische Chemie, 1848, S. 129–144. Online-Version, abgerufen am 11. Dezember 2009; doi:10.1002/prac.18480430113.
- ↑ Hans Meyer, Karl Steiner: Über ein neues Kohlenoxyd C12O9. In: Berichte der Deutschen Chemischen Gesellschaft, 1913, Bd. 46, S. 813–815; doi:10.1002/cber.191304601105.
- ↑ Patrick W. Fowler, Mark Lillington: Mellitic Trianhydride, C12O9: The Aromatic Oxide of Carbon. In: Journal of Chemical Information and Modeling, 2007, Bd. 47 (3), S. 905–908; doi:10.1021/ci600547n.
- ↑ Patent US4176101.
- ↑ Patent US3526048.
- ↑ Patent US4883864.
Auf dieser Seite verwendete Medien
Structure of benzo[1,2-c:3,4-c':5,6-c'']trifuran-1,3,4,6,7,9-hexaone
