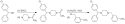Meclozin
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
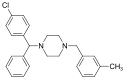
| Strukturformel ohne Stereochemie | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Meclozin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | R06AE05 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | ||||||||||||||||||||||
| Aggregatzustand | fest | |||||||||||||||||||||
| Schmelzpunkt | 206–216 °C unter Zersetzung (Racemat-Dihydrochlorid)[1] | |||||||||||||||||||||
| Siedepunkt | ||||||||||||||||||||||
| pKS-Wert | 3,1; 6,2[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Meclozin ist ein Arzneistoff aus der Gruppe der systemischen H1-Antihistaminika. Es wirkt gegen Übelkeit und Erbrechen und ist erfahrungsgemäß auch während einer Schwangerschaft sicher anwendbar. Seit 2007 ist es in Deutschland jedoch nicht mehr im Handel (ehemaliger Handelsname: Postadoxin N®). Im EU-Ausland sind oder waren Präparate unter dem Namen Postafene oder Agyrax bekannt.
Synthese
Die Synthese von Meclozin geht vom (4-Chlorphenyl)-phenylmethanol aus, welches zunächst nach Halogenierung mittels Thionylchlorid und Reaktion mit Acetylpiperazin zu einer 4-Chlorphenylphenylpiperazinylmethan-Zwischenverbindung umgesetzt wird. Nach sauer Abspaltung der Acetylgruppe erfolgt eine N-Alkylierung am Piperazinring mit 3-Methylbenzylchlorid zum racemischen Zielmolekül.[6]
Alternativ kann der letzte Syntheseschritt als reduktive N-Alkylierung am Piperazinring mit 3-Methylbenzaldehyd durchgeführt werden.[7][5]
Bei der Synthese entsteht das Racemat. Für pharmazeutische Anwendungen wird die Verbindung in das Dihydrochlorid überführt.
Klinische Angaben
Meclozin wird verwendet gegen Übelkeit und Erbrechen, insbesondere bei Reisekrankheit und bei Schwangerschaftserbrechen.
Die Sicherheit für die Anwendung während einer Schwangerschaft ist gut belegt,[8] es gilt sogar bei Schwangerschaftserbrechen als Mittel der Wahl.[9][10] Als Alternative kommt unter anderem Doxylamin in Frage.
Pharmakologische Eigenschaften
Meclozin wirkt durch kompetitive Hemmung an Histamin-H1-Rezeptoren. Da es als Antihistaminikum der ersten Generation die Blut-Hirn-Schranke überwindet, wirkt es nicht nur antiemetisch, sondern macht auch müde.
Stereoisomerie
Meclozin enthält ein stereogenes Zentrum und ist chiral. Der Arzneistoff wird als Racemat {1:1-Gemisch aus (R)-1-[(4-Chlorphenyl)-phenylmethyl]-4-[(3-methylphenyl)methyl]piperazin und (S)-1-[(4-Chlorphenyl)-phenylmethyl]-4-[(3-methylphenyl)methyl]piperazin} eingesetzt.
Einzelnachweise
- ↑ M. Brandstätter-Kuhnert, R. Hoffmann, M. Senn: Thermo-Microscopic and Spectrophotometric Determination of Antihistamines and Related Compounds, in: Microchem J., 1963, 7, S. 357–374.
- ↑ a b c Eintrag zu Meclozine in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ Eintrag zu Meclozin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 14. Januar 2019.
- ↑ a b Datenblatt Meclizine dihydrochloride, ≥97% (HPLC) bei Sigma-Aldrich, abgerufen am 31. Oktober 2016 (PDF).
- ↑ a b c A. Kleemann, J. Engel, B. Kutscher, D. Reichert: Pharmaceutical Substances – Synthesis, Patents, Applications, 4. Auflage, Thieme 2001, ISBN 3-13-115134-X.
- ↑ J.-H. Fuhrkop, G. Li: Organic Synthesis - Concepts and Methods, Wiley-VCH 2003, S. 237, ISBN 978-3-527-30272-7.
- ↑ US 2 709 169 (UCB, 1955).
- ↑ Källén B, Mottet I: Delivery outcome after the use of meclozine in early pregnancy. In: European Journal of Epidemiology. 18. Jahrgang, Nr. 7, 2003, S. 665–669, PMID 12952140 ((Seite nicht mehr abrufbar, Suche in Webarchiven: Online) [abgerufen am 17. September 2010]).
- ↑ ANTIEMETISCHE THERAPIE BEI SCHWANGERSCHAFTSERBRECHEN bei arznei-telegramm.de.
- ↑ Embryotox: Arzneimittelsicherheit in Schwangerschaft und Stillzeit: Datenbank Medikamente und Wirkstoffe: Meclozin.
Auf dieser Seite verwendete Medien
Globales Harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS) Piktogramm für gesundheitsgefährdende Stoffe.
(±)-Meclozine enantiomers structural formulae
Synthese von Meclozin
Synthese von Meclozin
chemical structure of Meclizine without stereochemistry