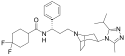
Maraviroc
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Maraviroc | |||||||||||||||||||||
| Summenformel | C29H41F2N5O | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | J05AX09 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus | CR5-Korezeptor-Antagonist | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 513,67 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Maraviroc (MVC, Handelsname: Celsentri, Hersteller: Pfizer) ist eine komplexe chemische Verbindung, die als Arzneistoff zur Behandlung von HIV-Infektionen und deren Folgen eingesetzt wird.[2] Er gehört zur Gruppe der Entry-Inhibitoren (Corezeptor-Antagonisten).
Pharmakologie
Maraviroc ist ein Entry-Inhibitor, der als selektiver Inhibitor den menschlichen Chemokinrezeptor CCR5 blockiert und somit das Andocken von HI-Viren an menschliche Zellen, insbesondere Makrophagen, verhindert. Die Zelle wird nicht infiziert. Seine Wirkung ist jedoch auf CCR5 nutzende (R5) HI-Viren beschränkt. Mittlerweile ist es mit Hilfe bioinformatischer Methoden möglich, CCR5 nutzende HI-Viren von CXCR4 nutzenden HI-Viren mit sehr hoher Genauigkeit zu unterscheiden.[3]
Pharmakokinetik
Maraviroc wird aus dem Magendarmtrakt resorbiert. Die empfohlene Dosierung beträgt zweimal täglich 150, 300 oder 600 mg in Abhängigkeit von der übrigen HAART, die durch Interaktion das Verhalten von Maraviroc mehr oder weniger beeinflusst. Die Bioverfügbarkeit liegt bei 23 bis 33 %. Die Einnahme des Arzneimittels kann mit oder ohne Nahrung erfolgen. Der Wirkstoff wird zu 76 % an Plasmaproteine gebunden, das Verteilungsvolumen wurde mit 2,8 ± 0,9 l/kg berechnet.
Maraviroc wird über Cytochrom P450 Monooxygenasen verstoffwechselt. Ein relevanter induktorischer oder inhibitorischer Effekt wurde nicht nachgewiesen. Wichtigstes Stoffwechselprodukt ist ein am Stickstoff desalkylierter Metabolit. Die Substanz wird hauptsächlich über den Stuhl ausgeschieden (ca. 25 % unverändert); 8 % einer Dosis von 300 mg erscheinen unverändert im Urin. Nach intravenöser Gabe beträgt Eliminationshalbwertzeit ca. 13 Stunden.
Bei Patienten mit angeborener oder medikamentös induzierter Niereninsuffizienz ist unter Umständen eine Dosisanpassung erforderlich (Einbeziehung der übrigen HAART-Medikamente). Bei leichter oder mittlerer Einschränkung der Leberfunktion sind die Blutspiegel um ca. 25 bis 46 % erhöht. Für diese Patientengruppe liegen noch nicht ausreichend Daten vor. Studien bei Kindern und älteren Patienten wurden noch nicht durchgeführt.
Nebenwirkungen
Durchfall, allgemeines Krankheitsgefühl, Magenschmerzen, Blähungen, Appetitlosigkeit, Kopfschmerzen, Schlafstörungen, Depressionen, Hautausschlag, Schwächegefühl oder Kraftlosigkeit, Anämie sowie der Anstieg von Leberenzymen sind die am häufigsten berichteten unerwünschten Ereignisse.[4] Zudem kann es zu lebensgefährlichen Hautreaktionen und allergischen Reaktionen sowie Lebererkrankungen kommen.[4] Weiterhin sind schwere Nebenwirkungen durch eine Wechselwirkung mit Grapefruit bekannt.[5]
Off-Label-Use
Es gibt Berichte, wonach Maraviroc erfolgreich gegen die progressive multifokale Leukenzephalopathie im Rahmen eines Immunrekonstitutionssyndroms wirkt.[6] Die Wirkung wird auf die immunmodulatorischen Eigenschaften von Maraviroc zurückgeführt. Studien zum Thema gibt es bislang nicht. Maraviroc wird als potentielles Medikament gegen COVID-19 in Betracht gezogen.[7]
Einzelnachweise
- ↑ Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von 4,4-difluoro-N-[(1S)-3-[(1R,5S)-3-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)-8-azabicyclo[3.2.1]octan-8-yl]-1-phenylpropyl]cyclohexane-1-carboxamide im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 7. Juli 2020.
- ↑ AIDS Meds - Amerikanische HIV Medikamenten Website.
- ↑ Jan Nikolaj Dybowski, Dominik Heider, Daniel Hoffmann: Prediction of Co-Receptor Usage of HIV-1 from Genotype. In: PLoS Computational Biology. 6. Jahrgang, Nr. 4, 15. April 2010, S. e1000743, doi:10.1371/journal.pcbi.1000743 (ploscompbiol.org [abgerufen am 26. November 2012]).
- ↑ a b Celsentri Filmtabletten: Gebrauchsinformationen für Anwender. ViiV Healthcare, Mai 2020, abgerufen am 11. August 2020.
- ↑ Medikamenten-Überdosis durch Grapefruit
- ↑ Guidelines for the Prevention and Treatment of Opportunistic Infections in HIV-Infected Adults and Adolescents.
- ↑ Glecaprevir and Maraviroc are high-affinity inhibitors of SARS-CoV-2 main protease: possible implication in COVID-19 therapy, Shamsi et al., In: Bioscience Reports, Band 40, Ausgabe 6, Juni 2020
Weblinks
Auf dieser Seite verwendete Medien
Globales Harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS) Piktogramm für gesundheitsgefährdende Stoffe.