Lithium-Cobaltdioxid-Akkumulator
Der Lithium-Cobaltdioxid-Akkumulator, auch LiCoO2-Akku, ist ein Lithium-Ionen-Akkumulator mit Lithium-Cobalt(III)-oxid (LiCoO2) als positivem Elektrodenmaterial. Von etwa 1990 bis 2010 verwendeten die meisten handelsüblichen Mobilgeräte einen Lithium-Cobaltdioxid-Akkumulator, der auch der erste kommerziell verfügbare Typ von Lithium-Ionen-Akkumulator war. Aufgrund dieser Dominanz am Markt war in dieser Zeit der Oberbegriff Lithium-Ionen-Akkumulator in vielen Fällen gleichbedeutend mit der Variante Lithium-Cobaltdioxid-Akkumulator. Das gilt heute nicht mehr, da Lithium-Ionen-Akkumulatoren mit verschiedener chemischer Zusammensetzung verkauft werden.
Wie alle Lithium-Ionen-Akkumulatoren können auch LiCoO2-Akkus als Lithium-Polymer-Akkumulator ausgeführt sein.
Lithium-Cobaltdioxid-Akkumulatoren neigen bei Überlastung zu thermischem Durchgehen.[1]
Geschichte
Der Lithium-Cobaltdioxid-Akkumulator war der erste kommerziell verfügbare Akkumulator mit Lithium-Ionen, der auf der Minuspolseite kein Lithiummetall nutzte. Die Brauchbarkeit von LiCoO2 als Elektrodenmaterial wurde 1980 von einer Forschergruppe um John B. Goodenough an der University of Oxford entdeckt.[2] Die positive Elektrode besteht aus der namensgebenden Substanz Lithium-Cobalt(III)-oxid. Der erste kommerziell erhältliche Li-Ionen-Akku wurde als Lithium-Cobaltdioxid-Akkumulator von Sony im Jahr 1991 auf den Markt gebracht und in der Hi8-Videokamera CCD TR 1 eingesetzt, hatte zwei in Serie geschaltete Zellen, eine Akkupack-Spannung von 7,2 V und eine Kapazität von etwa 1200 mAh.
Aufbau
Die negative Elektrode eines handelsüblichen Lithium-Cobaltdioxid-Akkumulators besteht aus Graphit, die positive Elektrode besteht aus Lithiumcobaltdioxid (LiCoO2) und der Elektrolyt ist ein Lithiumsalz in einer organischen Lösung. Als Ableitermaterialien werden Kupfer und Aluminium eingesetzt.[3]
Der Elektrolyt besteht aus einem Gemisch aprotischer Lösungsmittel wie Ethylencarbonat, Propylencarbonat, Dimethylcarbonat, Diethylcarbonat oder 1,2-Dimethoxyethan sowie aus darin gelöstem Lithiumhexafluorophosphat (LiPF6). Der Elektrolyt muss wasserfrei sein (Gehalt an H2O < 20 ppm), da sonst das Wasser mit dem Leitsalz LiPF6 zu HF (Flusssäure) reagiert.
Das Lithium selbst macht nur einen Bruchteil des verwendeten Batteriematerials aus. Gerade einmal 1 bis 1,5 % sind es, beim Rest handelt es sich um die Materialien der Kathode, der Anode oder der leitenden Kupferschichten.
Reaktionsgleichung
Halb-Reaktion der positiven Elektrode (Lithium-Cobaltdioxid-Schicht): [4][5]
Halb-Reaktion der negativen Elektrode (Graphitschicht):
Gesamtreaktion (Links: Laden, Rechts: Entladen):
Bei starkem Überladen (Zellspannung über 4,6 V) wird der Elektrolyt zersetzt. Bei zu schnellem Laden entsteht auf der Graphitelektrode metallisches Lithium, das mit dem Elektrolyten reagiert und ihn so verbraucht. Außerdem kann es durch das metallische Lithium zu Kurzschlüssen und dadurch zur Überhitzung und zum Brand kommen.
Anwendung
Bis etwa 2010 enthielten die meisten Lithium-Ionen-Akkumulatoren Lithium-Cobaltdioxid als positives Elektrodenmaterial, unter anderem Akkus von Apple (iPhone 6 Plus[6]), Microsoft, Samsung und Sony sowie Elektroautos von Daimler und Volkswagen.
Lithium-Ionen-Akkumulatoren enthalten auch im Jahre 2020 weiterhin noch einen Cobaltoxidanteil, vor allem wenn es um hohe Energiedichten oder auch hohe Entladeströme geht. Allerdings handelt es sich dabei meist nicht mehr um das ursprüngliche Lithium-Cobalt(III)-oxid LiCoO2, sondern um dem LiCoO2 verwandte Mischoxide wie die Lithium-Nickel-Mangan-Cobalt-Oxide NMC im NMC-Akkumulator oder Lithium-Nickel-Cobalt-Aluminium-Oxide NCA.
Handhabung und Gefahren

Bei mechanischen Beschädigungen, Überladen, Kurzschluss oder zu starkem Laden tiefentladener Akkus können Kurzschlüsse und/oder stark exotherme, nicht zu stoppende Reaktionen entstehen. Durch die starke Wärmeentwicklung können sich die Bestandteile der Zelle auflösen (z. B. der Separator), es kommt (wenn nicht ursächlich) zum inneren Kurzschluss und ab Temperaturen von ca. 180 °C bei dem verwendeten Lithium-Cobalt(III)-oxid zur Freisetzung von Sauerstoff in der Zelle, was letztendlich zum unkontrollierten und von außen nicht mehr beeinflussbaren thermischen Durchgehen bis zum Brand führt.[7]
Brennende Lithium-Ionen-Akkumulatoren geben giftige und reizende Dämpfe ab[8].
Brennende Lithium-Cobaltdioxid-Akkumulatoren und andere Lithium-Ionen-Akkumulatoren sollen mit viel Wasser gelöscht werden[8][9]. Hat der Prozess des thermischen Durchgehens eingesetzt, ist ein Ersticken des Brandes durch die von der Umgebungsluft unabhängige Sauerstofferzeugung in der Zelle zwar nicht mehr möglich, aber Kühlung mittels Wasser kann weitere Zellen schützen und ein Übergreifen des Brandes verhindern. Eine weitere Maßnahme bei kleinen Akkumulatoren bzw. einzelnen Zellen ist das kontrollierte Abbrennen-Lassen des Akkus.
Im Passagierflugzeug Boeing 787 Dreamliner sind Lithium-Cobaltdioxid-Akkumulatoren verbaut, die zu zwei Bränden im Januar 2013 führten.[10] Die Ursache ist letztendlich nicht geklärt worden.
Einzelnachweise
- ↑ Daniel Doughty, Ahmad Pesaran: Vehicle Battery Safety Roadmap Guidance. National Renewable Energy Laboratory, abgerufen am 19. Januar 2013.
- ↑ K. Mizushima, P. C. Jones, Philip J. Wiseman, John B. Goodenough: LixCoO2 (0 < x ≤ 1): A new cathode material for batteries of high energy density. In: Materials Research Bulletin. Band 15, Nr. 6. Elsevier, Juni 1980, S. 783–789, doi:10.1016/0025-5408(80)90012-4.
- ↑ A look inside a iphone 6 plus battery ( des vom 27. September 2017 im Internet Archive). Abgerufen am 27. September 2017 (englisch).
- ↑ H. J. Bergveld, W. S. Kruijt, P. H. L. Notten: Battery Management Systems: Design by Modelling. Springer, 2002, ISBN 978-94-017-0843-2, S. 107–108, 113.
- ↑ S Dhameja: Electric Vehicle Battery Systems. Newnes Press, 2001, ISBN 978-0-7506-9916-7, S. 12.
- ↑ A look inside a iphone 6 plus battery ( des vom 27. September 2017 im Internet Archive). Abgerufen am 27. September 2017 (englisch).
- ↑ Vehicle Battery Safety Roadmap Guidance. (PDF) National Renewable Energy Laboratory, U.S. Department of Energy, S. 108, abgerufen am 10. Oktober 2017.
- ↑ a b Lithium-Batterien und Lithium-Ionen-Akkus, Mitteilung des Umweltbundesamtes zum Umgang mit Lithiumakkus, abgerufen am 4. März 2020
- ↑ Thilo Jörgl: Lithium-Ionen-Akkus am besten mit Wasser löschen, Experte rät bei Bränden von anderen Löschmitteln ab. Mitteilung des Huss Verlag am 24. September 2018, abgerufen am 4. März 2020
- ↑ Daniel Michaels: Batteries Like Those on Dreamliner Raised Concerns In: The Wall Street Journal, 18. Januar 2013. Abgerufen am 19. Januar 2013
Auf dieser Seite verwendete Medien
Autor/Urheber: Henry Mühlpfordt / *File:Galvanic Cell.svg: Gringer, Lizenz: CC BY-SA 3.0
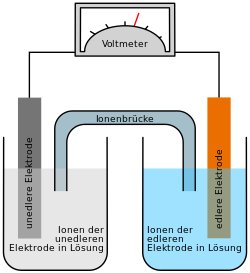
Galvanische Zelle
NTSB photos of the burned auxiliary power unit battery from a JAL Boeing 787 that caught fire on Jan. 7 at Boston's Logan International Airport. The dimensions of the battery are 19x13.2x10.2 inches and it weighs approximately 63 pounds (new).