Lignane


Lignane sind eine Stoffgruppe, die als Naturstoff in Pflanzen vorkommen, z. B. in der Taigawurzel, in der Baldrianwurzel und in verschiedenen essbaren Pflanzenteilen wie z. B. Lein- und Sesamsamen, Getreidekörnern, Früchten (z. B. in Schisandra) und Gemüse.
Lignane sind farblose, kristalline und geruchlose Verbindungen. Die sogenannten Enterolignane sind Stoffwechselprodukte, die im menschlichen Darm durch den bakteriellen Abbau der pflanzlichen Lignane entstehen, z. B. Enterolacton aus dem Lignan Sesamin.[1]
Struktur
Lignane zeichnen sich durch dimere C6C3-Körper (Phenylpropanoide) aus, die über das mittlere (β)-C-Atom verbunden sind. Unterschiedliche Strukturvarianten ergeben sich durch Anordnung und Verknüpfung der C3-Seitenketten. Viele Lignane weisen zusätzliche Heterocyclen auf, z. B. zwei Tetrahydrofuranringe in den Sesaminderivaten (Diepoxylignanen) oder ein Laktonring in den Lignanoliden. Wenn zwei Kohlenstoffe durch eine CC-Bindung verbunden sind, spricht man von Cyclolignanen, zu denen z. B. das Podophyllotoxin sowie die typischen Lignane aus Schisandra zählen.

In Pflanzen kommen Lignane in der Regel frei oder glycosidisch gebunden vor. Durch Polymerisation der C6C3-Körper (= Monolignole) entsteht das sogenannte Lignin, das in der pflanzlichen Zellwand vorkommt und für die Verholzung der Pflanzenzellen sorgt. Lignane und Lignin sind völlig unterschiedliche Verbindungen, die nicht miteinander verwechselt werden sollten. Lignin zählt zur Gruppe der unlöslichen Ballaststoffe.
Aufgaben und Bedeutung

In der Pflanze fungieren Lignane offenbar als Abwehrstoffe gegen Erkrankungen und Infektionen und scheinen auch eine Kontrolle über das Pflanzenwachstum auszuüben. Für den Menschen sind einige pflanzliche Lignane auch aus ernährungswissenschaftlicher Sicht interessant: Aufgrund ihrer östrogenartigen Wirkungen und anderer biochemischer Eigenschaften sind sie möglicherweise für die Vorbeugung gegen Herz-Kreislauferkrankungen und andere chronische Erkrankungen von Bedeutung.[2]
Des Weiteren werden Lignane als pflanzliche Sedativa eingesetzt. Die schlaffördernden Wirkungen haben ihnen auch die Bezeichnung als „Schlaflignane“ eingebracht. Traditionell wird z. B. die Baldrianwurzel, die Schlaflignane enthält, zur Beruhigung und Schlafförderung genutzt. Die als Schlaflignane bezeichneten Olivilverbindungen setzen an den gleichen Rezeptoren im Gehirn (Adenosin-A1-Rezeptoren) an wie das körpereigene Adenosin. Vergleichbar mit dem Adenosin fördern die Lignane den Schlaf, sie wirken wie ein pflanzliches Adenosin.[3][4][5][6] Damit die Lignane aus dem Baldrian schlaffördernd wirken können, müssen sie in ausreichender Konzentration vorhanden sein. Dabei spielt die Wahl des Extraktionsmittels eine Rolle. In Untersuchungen konnte nachgewiesen werden, dass nur aus Extrakten, die mit Hilfe des Lösungsmittels Methanol aus der Pflanze gewonnen wurden, die schlaffördernden Lignane in der erforderlichen Menge freigesetzt werden. Wurde stattdessen zur Extraktion das Lösungsmittel Ethanol genutzt, konnte die Lignan-Wirkung nicht festgestellt werden.[7]
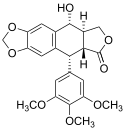
Einige Lignane sind cytotoxisch, darunter das Podophyllotoxin, dessen Derivat Etoposid als Cytostatikum eingesetzt wird.
Vorkommen in Lebensmitteln
Lignane finden sich vor allem in Leinsamen und Kürbiskernen.
| Lebensmittel | Lignane µg/100 g |
|---|---|
| Leinsamen | 370.000[8] 371.100[9] 384.500[10] |
| Kürbiskerne | 20.300[10] 21.400[9] |
| Erdbeeren | 1.578[9] |
| Oliven | 1.254[9] |
| Tee, Schwarz | 1.100[8] |
| Cranberry | 1.054[9] |
| Rotwein | 1.000[8] |
| Sonnenblumenkerne | 818[10] |
| Haferkleie | 790[10] |
| Kürbis | 695[10] |
| Weizenkleie | 664[10] |
| Sesamsamen | 661[10] |
| Brombeere | 569[10] |
| Knoblauch | 520[10] |
| Erdnüsse | 460[10] |
| Linsen | 457[10] |
| Spargel | 442[10] |
| Brokkoli | 256[10] 437[9] |
| Weizen, ganzes Korn | 410[10] |
| Karotten | 381[10] |
| Süßkartoffel | 336[10] |
| Aprikose, getrocknet | 328[10] |
| Nüsse | 96–257[9] |
| Sojabohnen | 10–200[8] |
| Roggen | 112[9] |
| Gerste | 58[9] |
Weblinks
Einzelnachweise
- ↑ José L. Peñalvo, Satu-M. Heinonen, Anna-M. Aura, Herman Adlercreutz: Dietary sesamin is converted to enterolactone in humans. In: The Journal of Nutrition. Band 135, Nr. 5, Mai 2005, S. 1056–1062, PMID 15867281.
- ↑ Peterson et al. 2010. Dietary lignans: physiology and potential for cardiovascular disease risk reduction. Nutr Rev. 2010 October; 68(10): 571–603.
- ↑ Britta Schumacher et al.: Lignans isolated from valerian: Identification and characterization of a new olivil derivative with partial agonistic activity at A(1) adenosine receptors. J Nat Prod 2002; 65:1479-1485
- ↑ Christa E. Müller et al.: Interactions of valerian extracts and a fixed valerian-hop extract combination with adenosine receptors. Life Sciences 2002; 71:1939-1949
- ↑ E. A. Abourashed et al.: In vitro binding experiments with a Valerian, hops and their fixed combination extract (Ze91019) to selected central nervous system receptors. Phytomedicine 2004; 11:633–638
- ↑ Cica Vissiennon et al.: Valerian Extract Ze 911 Inhibits Postsynaptic Potentials by Activation of Adenosine A1 Receptors in Rat Cortical Neurons. Planta Med 2006; 72:579-583.
- ↑ K. Sichardt et al.: Modulation of postsynaptic potentials in rat cortical neurons by valerian extracts macerated with different alcohols: involvement of adenosine A(1)- and GABA(A)-receptors. Phytother Res 2007; 21(10):932-7.
- ↑ a b c d Untersuchung auf östrogenartige Stoffe mit einem Biotest. In: laves.niedersachsen.de. Niedersächsisches Landesamt für Verbraucherschutz und Lebensmittelsicherheit, 2011, ehemals im (nicht mehr online verfügbar); abgerufen am 2. August 2020. (Seite nicht mehr abrufbar. Suche in Webarchiven)
- ↑ a b c d e f g h i Antonie Danz: Phytoöstrogene - Pflanzenstoffe mit Hormonwirkung. In: ugb.de. Der Verband für Unabhängige Gesundheitsberatung (UGB), 2015, abgerufen am 2. August 2020.
- ↑ a b c d e f g h i j k l m n o p q Regina Verena Piller: Phytoöstrogene in der Ernährung und ihr Einfluss auf das Risiko für Brustkrebs (Dissertation). In: mediatum.ub.tum.de. Technische Universität München, 12. Juni 2006, abgerufen am 2. August 2020.
Auf dieser Seite verwendete Medien
Autor/Urheber: Stanislav Doronenko, Lizenz: CC BY 2.5
Eleutherococcus senticosus
Chemical structure of podophyllotoxin.
Autor/Urheber: Grünspecht92, Lizenz: CC BY-SA 4.0
Liganolid, Diepoxylignan, 2,7'-Cyclolignan, 2,2'-Cyclolignan
Struktur des Dibenzylbutans, ein Lignan