LDL-Rezeptor
| LDL-Rezeptor | ||
|---|---|---|
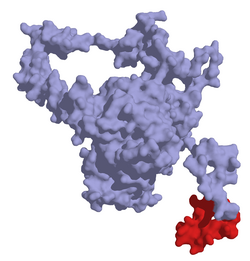 | ||
| Oberflächenmodell der extrazellulären Domäne des LDLR nach PDB 1N7D | ||
Vorhandene Strukturdaten: 1ajj, 1d2j, 1f5y, 1f8z, 1hj7, 1hz8, 1i0u, 1ijq, 1ldl, 1ldr, 1n7d, 1xfe, 2fcw | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 839 Aminosäuren; 93,1 kDa | |
| Bezeichner | ||
| Gen-Name | LDLR | |
| Externe IDs | ||
| Vorkommen | ||
| Homologie-Familie | LDL-Rezeptor | |
| Übergeordnetes Taxon | vielzellige Tiere | |
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 3949 | 16835 |
| Ensembl | ENSG00000130164 | ENSMUSG00000032193 |
| UniProt | P01130 | Q3TVR4 |
| Refseq (mRNA) | NM_000527 | XM_979020 |
| Refseq (Protein) | NP_000518 | XP_984114 |
| Genlocus | Chr 19: 11.06 – 11.1 Mb | Chr 9: 21.47 – 21.5 Mb |
| PubMed-Suche | 3949 | 16835 |
Der LDL-Rezeptor (low density lipoprotein receptor) ist ein Protein, das in Zellmembranen aller Tiere verankert ist. Es ist ein sogenannter Membranrezeptor, der mit seinen außerhalb der Zelle gelegenen Bindungsstellen die spezifische Bindung an das Apoprotein B-100, den Proteinanteil der LDL-Nahrungsfette vermittelt. Nachdem das LDL so gebunden ist, wird es in das Innere der Zelle transportiert.[1]
Für die Aufklärung des vom LDL-Rezeptor genutzten Aufnahmemechanismus und die Bedeutung für den Cholesterinhaushalt wurden Joseph Leonard Goldstein und Michael S. Brown 1985 mit dem Nobelpreis ausgezeichnet.[2]
Synthese
LDL-Rezeptoren werden synthetisiert, wenn die Cholesterinkonzentration innerhalb der Zelle zu gering ist. Die Transkription des LDL-Rezeptor-Gens wird durch SREBP2 aktiviert.
Das 44,36 Kilobasen lange Gen, das für den Rezeptor kodiert, enthält 18 Exons. Die 5174 Basen der mRNA werden am Endoplasmatischen Reticulum in ein 839 Aminosäuren enthaltendes und 93,1 kDa schweres Protein übersetzt. Dieses wird im Golgi-Apparat glykosyliert und dann an die Zelloberfläche transportiert. Etwa 700 der 839 Aminosäuren bilden den extrazellulären Teil des Rezeptors.[1]
Funktion
Transport von LDL aus dem Blutplasma in die Zelle
LDL-Rezeptoren findet man auf nahezu allen Zelltypen, da sie die Versorgung der Körperzellen mit dem in der LDL transportierten Cholesterin sicherstellen. Die beladenen Rezeptoren konzentrieren sich an bestimmten Stellen der Zelloberfläche, sogenannten Coated Pits, und werden zusammen mit dem LDL-Partikel innerhalb weniger Minuten durch Endozytose in die Zelle geschleust. Hierbei schnüren sich die Coated Pits von der Plasmamembran in Richtung des Zellinneren ab und bilden kleine, membranumhüllte Kugeln, die Coated Vesicles. Diese Vesikel sind durch eine Clathrinhülle stabilisiert, die aus vielen zusammengelagerten Clathrin-Molekülen (in Form von Triskelions) besteht. Die Clathrinhülle zerfällt kurz nach der Abschnürung des Vesikels, das dadurch zu einem sogenannten Endosom wird. In diesem fällt kontinuierlich der pH-Wert, während das Endosom "reift". In einem CURL (Compartment for Uncoupling of Receptor and Ligand) genannten Stadium trennt sich aufgrund des sauren Milieus das LDL vom LDL-Rezeptor.
Während die Rezeptoren erneut an die Oberfläche der Zellmembran transportiert werden (Rezeptor-Recycling), fusionieren im Zellinneren die LDL-haltigen Endosomen mit Lysosomen zu sekundären Lysosomen. Dort werden die LDL-Partikel enzymatisch abgebaut. Der Proteinanteil wird in Aminosäuren zerlegt und die Cholesterinester durch eine lysosomale Lipase in Cholesterin und freie Fettsäuren gespalten. Das so freigesetzte Cholesterin kann dann in die Zellmembran eingefügt werden (siehe auch Membrantransport), in den entsprechenden Geweben zur Synthese von Steroidhormonen verwendet oder als Cholesterin-Ester gespeichert werden.[3] Alternativ erfolgt eine Aufnahme von LDL in Zellen über den Scavenger-Pathway.
Aufnahme anderer Proteine
Der LDL-Rezeptor ist auch dasjenige Protein, das den Transport von Tat-Protein des HI-Virus in Neuronen bewerkstelligt. Er ist damit ein Faktor bei der HIV-Infektion.[4]
Gendefekt des Rezeptors
Ein genetischer Defekt des LDL-Rezeptors ist die Ursache für die vererbliche familiäre Hypercholesterinämie. Die Patienten besitzen wenig bis keine funktionsfähigen LDL-Rezeptoren. Insbesondere bei der homozygoten Form der familiären Hypercholesterinämie (HoFH) zeigt sich ein weitestgehender Funktionsverlust des LDL-Rezeptors, während bei der heterozygoten Form der Krankheit meist noch eine Restfunktion des Rezeptors vorliegt. Da sowohl die Transkription des LDL-Rezeptors als auch die zelluläre Eigensynthese von Cholesterin durch intrazelluläres Cholesterin revers reguliert werden, entsteht ein Teufelskreis mit der Folge eines dramatisch erhöhten LDL-Cholesterinspiegels im Serum, der begleitet wird von einer intrazellulären Überproduktion an Cholesterin. Schon im Kindesalter leiden manche Betroffene an einer sich rasch ausbreitenden Arteriosklerose. Patienten mit der homozygoten Form fallen dabei meist mit Gesamtcholesterinwerten von 650 bis 1000 mg/dl sowie LDL-Cholesterinwerten von > 500 mg/dl auf.[5][6]
Bei HoFH-Patienten zeigt sich ein direkter Zusammenhang zwischen erhöhten LDL-Cholesterin-Spiegeln und dem Risiko kardiovaskulärer Ereignisse (wie z. B. Herzinfarkt, Schlaganfall).[7][8] Für die homozygote Form der familiären Hypercholesterinämie (HoFH) ist eine ausgeprägte Arteriosklerose bereits in jungen Jahren typisch.[9][10]
Die cholesterinabhängige Transkriptionsregulation des LDL-Rezeptors kann jedoch zur Therapie heterozygoter LDL-Rezeptordefekte genutzt werden: Durch pharmakologische Hemmung der zellulären Cholesterinsynthese (Statine) verarmen die Zellen an Cholesterin und erhöhen die Transkription des gesunden Allels, so dass die LDL-Rezeptorlevel Werte erreichen, die denen von Gesunden ähnlich sind. Als Folge steigt die LDL-Aufnahme in die Zelle und die erhöhten LDL-Spiegel im Serum werden reduziert.[11]
Bei Patienten mit homozygoter familiärer Hypercholesterinämie (HoFH) funktioniert dieser Therapieansatz meist nur unzureichend: Durch den genetischen Defekt ist in der Regel die Bindung des LDL-Cholesterins an die LDL-Rezeptoren stark beeinträchtigt[6]. Ein 2013 zugelassener Behandlungsansatz bei HoFH-Patienten ist die Hemmung des mikrosomalen Transportproteins (MTP) mit dem MTP-Hemmer Lomitapid.
Einzelnachweise
- ↑ a b UniProt P01130
- ↑ The Nobel Foundation: The Nobel Prize in Physiology or Medicine 1985. Abgerufen am 6. Mai 2010 (engl.).
- ↑ H. Jeon, S. C. Blacklow: Structure and physiologic function of the low-density lipoprotein receptor. In: Annu. Rev. Biochem. 74. Jahrgang, 2005, S. 535–562, doi:10.1146/annurev.biochem.74.082803.133354, PMID 15952897.
- ↑ Y. Liu, M. Jones, C. M. Hingtgen et al.: Uptake of HIV-1 tat protein mediated by low-density lipoprotein receptor-related protein disrupts the neuronal metabolic balance of the receptor ligands. In: Nat. Med. 6. Jahrgang, Nr. 12, Dezember 2000, S. 1380–1387, doi:10.1038/82199, PMID 11100124.
- ↑ A. D. Marais: Familial hypercholesterolaemia. In: Clin. Biochem. Rev. Band 25, Nr. 1, 2004, S. 49–86.
- ↑ a b F. J. Raal, R. D. Santos: Homozygous familial hypercholesterolemia: Current perspectives on diagnosis and treatment. In: Atherosclerosis. Band 223, Nr. 2, 2012, S. 262–268.
- ↑ J. L. Goldstein, H. H. Hobbs et al.: Familial hypercholesterolemia. New York, McGraw-Hill 2001
- ↑ S. Moorjani, M. Roy et al.: Mutations of low-density-lipoprotein-receptor gene, variation in plasma cholesterol, and expression of coronary heart disease in homozygous familial hypercholesterolaemia. In: Lancet, Band 341, Nr. 8856, 1993, S. 1303–1306.
- ↑ Rader DJ, Cohen J, Hobbs HH. Monogenic hypercholesterolemia: new insights in pathogenesis and treatment. J Clin Invest 2003; 111:1795–1803
- ↑ Z. Reiner et al.: ESC/EAS guidelines for the management of dyslipidaemias. In: European Heart Journal, Band 32, 2011, S. 1769–1818.
- ↑ Y. Saito: Critical appraisal of the role of pitavastatin in treating dyslipidemias and achieving lipid goals. In: Vasc Health Risk Manag. 5. Jahrgang, 2009, S. 921–936, PMID 19997573, PMC 2788597 (freier Volltext).
Weblinks
Auf dieser Seite verwendete Medien
3d structure of LDL receptor (LDLR) extracellular domain (40-699) after PDB 1N7D. Ref.: G.Rudenko et al. (2003). 'MAD'ly phasing the extracellular domain of the LDL receptor: a medium-sized protein, large tungsten clusters and multiple non-isomorphous crystals.. Acta Crystallogr D Biol Crystallogr, 59, 1978-1986. PMID 14573953 [DOI no: 10.1107/S0907444903021383]
