Kynureninase
| Kynureninase | ||
|---|---|---|
 | ||
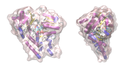
| Bänder/Oberflächenmodell der Kynureninase des Menschen, mit PLP und einem Inhibitor (Kalotten), nach PDB 3E9K | ||
Vorhandene Strukturdaten: 2hzp | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 465 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Homodimer | |
| Kofaktor | Pyridoxalphosphat | |
| Bezeichner | ||
| Gen-Name | KYNU | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 3.7.1.3, Hydrolase | |
| Reaktionsart | Hydrolyse einer C-C-Bindung | |
| Substrat | 3-Hydroxykynurenin + H2O | |
| Produkte | 3-Hydroxyanthranilat + Alanin | |
| Vorkommen | ||
| Homologie-Familie | Kynureninase | |
| Übergeordnetes Taxon | Lebewesen | |
Bei Kynureninase handelt es sich um dasjenige Enzym, das von 3-Hydroxykynurenin ein Molekül Alanin abspaltet. Diese Reaktion ist ein Teilschritt im Abbau der Aminosäure Tryptophan und in der Nicotinsäure-Biosynthese. Kynureninase kommt in allen Lebewesen vor. Beim Menschen ist sie in allen Gewebetypen zu finden, besonders aber in Plazenta, Leber und Lunge. Erhöhte Werte des Enzyms wurden in der Nähe von Infektionen festgestellt.[1]
Mutationen im KYNU-Gen können zum Mangel an Kynureninase führen. Die Folge ist Vitamin-B3-Mangel und eine verstärkte Ausscheidung der Tryptophan-Abbauprodukte Kynurenin, 3-Hydroxykynurenin und Xanthurensäure im Urin.[2][3]
Varianten des Enzyms werden mit Bluthochdruck bei Han-Chinesen in Zusammenhang gebracht.[4]
Katalysierte Reaktion
L-Alanin wird durch Hydrolyse von 3-Hydroxy-L-Kynurenin abgespalten und es entsteht 3-Hydroxyanthranilat.
Weblinks
Einzelnachweise
- ↑ UniProt Q16719
- ↑ Kynureninasemangel. In: Online Mendelian Inheritance in Man. (englisch).
- ↑ M Christensen, M Duno, AM Lund, F Skovby, E Christensen: Xanthurenic aciduria due to a mutation in KYNU encoding kynureninase. In: J. Inherit. Metab. Dis.. 30, Nr. 2, April 2007, S. 248–255. doi:10.1007/s10545-007-0396-2. PMID 17334708.
- ↑ Y Zhang, KX Zhang, X He et al.: [A polymorphism of kynureninase gene in a hypertensive candidate chromosomal region is associated with essential hypertension]. In: Zhonghua Xin Xue Guan Bing Za Zhi. 33, Nr. 7, Juli 2005, S. 588–591. PMID 16080802.
Auf dieser Seite verwendete Medien
Struktur von 3-Hydroxyanthranilat
The reaction mechanism of KYNU. The color scheme is as follows: KYNU, PLP, substrate names, inorganic molecules, 3hAn's moiety, Ala's moiety . Created in ISIS/Draw 2.5 --> Dell Photo Editor.
Struktur von 3-Hydroxy-L-kynurenin
Struktur von L-Alanin unter physiologischen Bedingungen