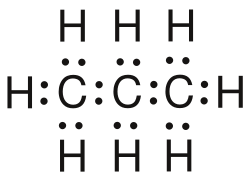Konstitutionsformel
Die Konstitutionsformel ist eine chemische Darstellungsweise. Durch die Konstitutionsformel kann ausgedrückt werden, wie die Atome eines Moleküls miteinander durch chemische Bindungen verbunden sind.
| Strukturformeln | andere Darstellungsweisen | ||||||
|---|---|---|---|---|---|---|---|
| Elektronen- formel | Valenzstrich- formel | Keilstrich- formel | Skelett- formel | Konstitutions- formel | Summen- formel | Verhältnis- formel | |
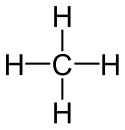
| Methan |  |  | 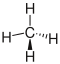 | existiert nicht | CH4 | CH4 | CH4 |
| Propan |  |  |  | CH3–CH2–CH3 oder CH3 CH2 CH3 | C3H8 | C3H8 | |
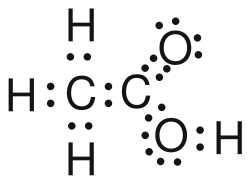
| Essigsäure |  |  | 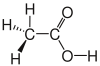 |  | CH3–COOH oder CH3 COOH | C2H4O2 | CH2O |
| Wasser | existiert nicht | H–O–H oder H O H | H2O | H2O | |||
Im Gegensatz zur Summenformel und zur Verhältnisformel, aus denen lediglich Anzahl und/oder Zahlenverhältnis der Atome unterschiedlicher Elemente hervorgehen, liefert die Konstitutionsformel auch topologische Informationen, aus denen sich beispielsweise die Zuordnung des dargestellten Stoffes zu einer Verbindungsklasse ermitteln lässt. Die Konstitutionsformel entspricht somit der Halbstrukturformel (Gruppenformel) im eigentlichen Sinne.[1]
Weitere Informationen zur räumlichen Zusammensetzung eines Moleküls liefern einige Strukturformeln, wie bspw. die Keilstrichformel. Die Begriffe Strukturformel, Valenzstrichformel und Konstitutionsformel werden häufig miteinander verwechselt und übereinstimmend verwendet.
Als einer der ersten Chemiker verwendete Edward Frankland 1866 in einem Lehrbuch Konstitutionsformeln zur Darstellung chemischer Verbindungen.[2] Konstitutionsformeln waren eine der ersten Anwendungen der frühen Mathematischen Graphentheorie.[3][4][5]
Einzelbelege
- ↑ Brink, Klaus: DIN 32641 – Chemische Formeln, in Praxis der Naturwissenschaften-Chemie, 2/49, 2000, Seite 16f.
- ↑ Edward Frankland: Lecture Notes for Chemical Students. Van Voorst, London, 1866, S. 23–26 (Volltext in der Google-Buchsuche).
- ↑ Norman L. Biggs, E. Keith Lloyd, Robin J. Wilson: Graph Theory 1736-1936. Oxford University Press, 1999, ISBN 0-19-853916-9.
- ↑ James Joseph Sylvester: Chemistry and Algebra. In: Nature. Band 17, S. 284.
- ↑ Arthur Cayley: Chemical Graphs. In: Philosophical Magazine. Band 47, 1874, S. 444–446.
Siehe auch
Auf dieser Seite verwendete Medien
Struktur von Methan
Autor/Urheber: Holger87, Lizenz: CC BY-SA 3.0
Wasser in der Elektronenschreibweise (Lewis-Schreibweise)
Autor/Urheber: Holger87, Lizenz: CC BY-SA 3.0
Essigsäure in der Elektronenschreibweise (Lewis-Schreibweise)
Essigsäure
Propane
Autor/Urheber: Holger87, Lizenz: CC BY-SA 3.0
Methan in der Elektronenschreibweise (Lewis-Schreibweise)
Propan in der Elektronenschreibweise (Lewis-Schreibweise)