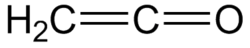Ketene
| Ketene |
 Allgemeine Struktur |
Struktur der Stammverbindung Keten |
Ketene (Betonung auf der zweiten Silbe: Ketene) sind eine Gruppe organischer Verbindungen mit der allgemeinen Formel RR'C=C=O. R und R' können beliebige Reste sein. Ethenon (=Keten) ist der einfachste Vertreter dieser Stoffgruppe mit der Formel H2C=C=O. Ketene sind sehr reaktiv, fast alle dimerisieren sofort zum entsprechenden Diketen. Ketene sind formal innere Anhydride der entsprechenden Carbonsäuren.
Geschichte
Ketene wurden zuerst von Hermann Staudinger 1905 in Form von Diphenylketen entdeckt (Umsetzung von -Chlordiphenylacetylchlorid mit Zink) und systematisch untersucht.[1] Inspiriert war er von den ersten Beispielen reaktiver organischer Zwischenprodukte und stabiler Radikale, die Moses Gomberg 1900 entdeckte (Verbindungen mit Triphenylmethylgruppe). Staudinger fand mit den Ketenen eine neue derartige Stoffklasse.[2]
Herstellung
Industriell erzeugt man Keten durch katalytische Hochtemperatur-Pyrolyse von Aceton oder Essigsäure bei 700 °C.
- Ketensynthese durch Pyrolyse von Aceton. Als Nebenprodukt entsteht Methan.
Allgemein sind Ketene durch Umsetzung von Carbonsäurehalogeniden, die mindestens einen α-ständigen Wasserstoff tragen, mit Basen wie Triethylamin in situ zugänglich:[3]
Ketene können auch durch eine Wolff-Umlagerung entstehen.
Reaktionen
Ketene sind durch ihre kumulierten Doppelbindungen sehr reaktionsfreudig.[4]
Bildung von Carbonsäureestern
Durch Reaktion mit Alkoholen entstehen Carbonsäureester:
Bildung von Carbonsäureanhydrid
Ein Keten reagiert mit einer Carbonsäure zu einem Carbonsäureanhydrid:
Bildung von Carbonsäureamiden
Ketene reagieren mit Ammoniak zu primären Carbonsäureamiden:
Bei der Reaktion von Ketenen mit primären Aminen entstehen sekundäre Amide:
Ketene reagieren mit sekundären Aminen zu tertiären Amiden:
Hydrolyse
Durch Reaktion mit Wasser entstehen aus Ketenen Carbonsäuren:
Bildung von Enolacetaten
Mit enolisierbaren Carbonylverbindungen entstehen aus Ketenen Enolacetate. Das folgende Beispiel zeigt die Reaktion von Ethenon mit Aceton unter Bildung eines Propen-2-yl-acetats:
Dimerisierung
Bei Raumtemperatur dimerisiert Keten schnell zu Diketen, kann jedoch durch Erhitzen wiedergewonnen werden:
[2+2]-Cycloaddition
Ketene können u. a. mit Alkenen, Carbonylverbindungen, Carbodiimiden und mit Iminen unter [2+2]-Cycloaddition reagieren. Das Beispiel zeigt die Synthese eines β-Lactams durch die Reaktion von einem Keten mit einem Imin (Siehe Staudinger-Synthese):[5][6]
Einzelnachweise
- ↑ Staudinger, Ketene, eine neue Körperklasse. Berichte der deutschen chemischen Gesellschaft, Band 38, 1905, S. 1735–1739.
- ↑ Thomas T. Tidwell, The first century of Ketenes (1905-2005): the birth of a family of reactive intermediates, Angewandte Chemie, Int. Edition, Band 44, 2005, S. 5778–5785.
- ↑ Siegfried Hauptmann: Organische Chemie, 2. Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 410, ISBN 3-342-00280-8.
- ↑ Siegfried Hauptmann: Organische Chemie: mit 65 Tabellen. Deutscher Verlag für Grundstoffindustrie, Leipzig 1985, ISBN 3-87144-902-4, S. 410–412.
- ↑ Jie Jack Li: Name reactions. A collection of detailed reaction mechanisms. 3. Auflage. Springer-Verlag, Berlin 2006, ISBN 978-3-540-30030-4, S. 561–562, doi:10.1007/3-540-30031-7.
- ↑ Hermann Staudinger: Zur Kenntnis der Ketene. Diphenylketen. In: Justus Liebigs Annalen der Chemie. Band 356, Nr. 1–2. John Wiley & Sons, Inc., 1907, S. 51–123, doi:10.1002/jlac.19073560106.
Auf dieser Seite verwendete Medien
General structure of ketenes
Autor/Urheber: Nossy123, Lizenz: CC BY-SA 4.0
[2+2] cycloaddition ketene and imine
Keten-Synthese
Autor/Urheber: Nossy123, Lizenz: CC BY-SA 4.0
Formation of tertiary carboxamide
Autor/Urheber: Nossy123, Lizenz: CC BY-SA 4.0
Formation of Propen-2-yl acetate
Autor/Urheber: Nossy123, Lizenz: CC BY-SA 4.0
Formation of primary carboxamide
Ethenone
Autor/Urheber: Nossy123, Lizenz: CC BY-SA 4.0
Formation of secondary carboxamide
Autor/Urheber: Nossy123, Lizenz: CC BY-SA 4.0
Formation of carboxylic anhydride