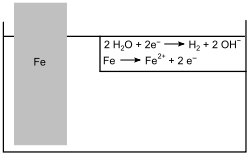Korrosionsschutz
Als Korrosionsschutz werden Maßnahmen zur Vermeidung von Schäden bezeichnet, die durch Korrosion an metallischen Bauteilen hervorgerufen werden können. Da eine absolute Korrosionsbeständigkeit nicht erreicht werden kann, zielen die ergriffenen Schutzmaßnahmen im Allgemeinen darauf, die Geschwindigkeit des korrosiven Angriffs so weit zu verringern, dass eine Schädigung des Bauteils während seiner Lebensdauer vermieden werden kann.
Allgemeines
Der Begriff Korrosion wird nicht mehr nur für metallische Werkstoffe, sondern auch für Glas, Kunststoffe, Baustoffe angewandt. Das angreifende Medium wird als korrosives Mittel bezeichnet. Kommt es durch einen Korrosionsangriff zu einer Beeinträchtigung der Funktionalität eines Bauteils, so ist dies ein Korrosionsschaden.
Nach DIN EN ISO 8044 werden u. a. folgende Korrosionsarten unterschieden:
- Flächenkorrosion, bei der die Oberfläche gleichmäßig beschädigt wird
- Muldenkorrosion, bei der die Oberfläche ungleichmäßig stark beschädigt wird
- Lochkorrosion, die nur kleine Bereiche der Oberfläche zerstört
- Spaltkorrosion, bei der die Werkstoffoberfläche in schmalen Spalten, z. B. in Schweißnähten, angegriffen wird

Um die chemischen Korrosionsprozesse zu verhindern, gibt es verschiedene Verfahren und Vorgehensweisen, die man allgemein als Korrosionsschutz bezeichnet. Im Folgenden wird auf den metallischen Korrosionsschutz näher eingegangen.
Es wird zwischen aktivem[1] und passivem Korrosionsschutz unterschieden. In Anlehnung an den Begriff „konstruktiver Holzschutz“ kann auch bei metallischen Werkstoffen durch geeignete Konstruktion ein gewisser Korrosionsschutz erreicht werden.
Passiver Korrosionsschutz

Passiver Korrosionsschutz umfasst alle Maßnahmen, welche eine gegen korrosive Medien abschirmende Wirkung erzielen.
Konstruktiver Korrosionsschutz
Maßnahmen wie Überdachungen, Spritzschutz und Gefälle zum Ablauf von Flüssigkeiten verringern den Kontakt zu korrosiv wirkenden Medien wie Wasser.
Korrosionsschutz durch Beschichtungen
Durch geeignete Überzüge wie Beschichtungen (Korrosionsschutzfarbe) kann ein Werkstoff gegenüber korrosiven Gasen und Flüssigkeiten nahezu isoliert werden. Bindemittel wie Kunstharze werden häufig mit Zusatzstoffen wie Eisenglimmer-Pigmenten angereichert, um die abschirmende Wirkung zu verbessern und die Beständigkeit zu erhöhen. Pigmente wie Zinkstaub, Zinkphosphat, Zinkchromat oder Bleimennige werden auch als aktive Pigmente bezeichnet, da sie zusätzlich eine chemische oder galvanische Rostschutzwirkung haben.
Als flüssig, pastös oder pulverförmig aufgetragene Beschichtungsstoffe[2] werden Kunstharze wie EP oder PU, Kunststoffe wie PVC sowie Kunststofffolien, Öle, Lack, Gummi oder Hartparaffine verwendet.
Anorganische oder metallische Überzüge können ebenso durch eine Passivierung gebildet werden oder durch Auftrag von Umwandlungsschichten mit eher nichtmetallischem Charakter oder Konversionsschichten wie bei der Phosphatierung, Chromatierung, Eloxierung, Harteloxierung sowie der Feuerverzinkungen, die ihrerseits wiederum eine schützende Passivierungsschicht ausbilden und darüber hinaus bei Beschädigung den Untergrund als Opferanode schützen.
Große und lange Pipelines aus Stahl für den Wassertransport werden bevorzugt zum Korrosionsschutz mit einer Innenbeschichtung aus Zementmörtel ausgekleidet. Durch die Zumischung geeigneter Kunststoffe kann die Korrosionsfestigkeit weiter verbessert werden.[3] Die wesentlichen Vorteile dieser Art der Beschichtung sind:
- geringe Kosten
- weitgehend Beständigkeit gegen korrosive Wässer bis zu einem pH-Wert größer 4,0;[4] diese Beständigkeit gilt nicht für Deionat.
- Selbstheilung schmaler Risse, die bis zur Eisenoberfläche gehen[5]
Auch galvanotechnisch oder chemisch erzeugte, metallische Deckschichten aus Zinn, Gold, Nickel, Kupfer, Chrom, Zink oder Legierungsschichten wie Nickel-Phosphor (chemisch Nickel) oder Zink-Nickel bewirken einen Korrosionsschutz. Ebenfalls findet die Feuerverzinkung (ein Schmelztauchverfahren) breite Anwendung. Die Schutzwirkung basiert bei Metallschichten auf ihrer Eigenschaft, selbst nicht zu korrodieren (Edelmetalle) oder aber auf der Barrierewirkung durch Bildung einer dichten Oxidschicht auf der Oberfläche (sog. Passivschicht), die als Korrosionsschutz dient. Einige Metalle sind in der Lage, „von selbst“ eine Deckschicht zu bilden, die den Grundwerkstoff schützt, wie die Patina auf Kupfer oder Zink.
Bei metallischen Schichten hängt die Schutzwirkung bei Schichtverletzungen von der Art der Schicht ab. Unedlere Schichten schützen das Werkstück kathodisch und fungieren dabei als Opferanode – die Schicht löst sich bevorzugt auf und erhält somit möglichst lang die Funktion des Bauteils. Selbst kleinere Fehlstellen oder Schäden in der Schicht haben daher zunächst keine gravierenden Auswirkungen (sog. Fernwirkung). Ein klassisches Beispiel ist die Verzinkung von Stahl, aber auch der Schutz von Wasserbauwerken durch Anbringen von Opferanoden aus Zink-, Aluminium- oder Magnesium-Legierungen wie bei Schiffen, Schleusen, Spundwänden, Bootsteilen oder Schienen. Edlere Schichten als das Grundmaterial schützen dieses anodisch, haben aber den großen Nachteil, dass bei einer Beschädigung der Schicht der darunterliegende, unedlere Grundwerkstoff beschleunigt aufgelöst wird (Kontaktkorrosion).
Einen solchen Korrosionsschutz bietet Weißblech, bei dem Zinn als Beschichtungsmaterial verwendet wird, sodass auch Lebensmittel damit verpackt werden können. Allerdings entstehen nach einiger Zeit, wenn die Dose offen steht, Zinnionen, die toxisch beispielsweise auf Kresse wirken. Deshalb werden Dosen zusätzlich lackiert.
Bei Rostumwandlern wird der Korrosionsschutz dadurch erreicht, dass die ursprünglichen, porösen Eisenoxide abgelöst und die obere Eisenschicht weiter oxidiert wird zu einem Eisenoxid mit glatter Oberfläche, das eine Aufnahme von Wasser und somit Weiterrosten verhindert. Dafür wird Phosphorsäure (Phosphatierung) oder auch Tannin gemischt mit Zusatzstoffen eingesetzt. Nach der Behandlung ist eine Versiegelung mit Polymer-Lacken üblich, um einen dauerhafteren Schutz zu erreichen. Im Handel werden auch Produkte angeboten, die beide Funktionen verbinden.[6][7]
Aktiver kathodischer Korrosionsschutz
Mit Fremdstrom
Kathodischer Korrosionsschutz – kurz KKS – kann durch das Anlegen einer Spannung an eine Fremdstrom-Anode erreicht werden. Bei Erdöl-, Gas-, Fernwärme- und Wasser-Pipelines werden in bestimmten Abständen Elektroden in einigen hundert Metern Abstand von der Leitung im Boden versenkt, die mit der Pipeline und dem Erdboden einen Stromkreis bilden. Dabei kann die Spannung (in der Größenordnung von wenigen Volt) des aus Boden und metallischer Rohrleitung bestehenden galvanischen Elements ausgeglichen werden. Die erforderliche Gegenspannung hängt dabei auch von Wassergehalt und der Zusammensetzung des Bodens ab. Zur Abgrenzung einzelner KKS-Bereiche werden Isoliertrennstellen in die Leitung eingesetzt, die die Leitfähigkeit der Pipeline unterbrechen. Dies ermöglicht es, den Schutzstrom besser zu steuern und Fehler eingrenzen zu können.
Im Brückenbau, besonders bei Autobahnbrücken, wird der KKS mittels Fremdstromanode durchgeführt. Dazu wird ein Anodengitter aus beschichtetem Titan auf die zu schützende Oberfläche aufgebracht und mit Spritzbeton circa 2 cm bis 3 cm eingespritzt. Der Spritzbeton dient dabei als Elektrolyt. Der Strom wird über Gleichrichter in die Bewehrung eingeleitet und so der kathodische Schutz erreicht. Die Maßnahme wird laufend mit einem automatischen Überwachungssystem überprüft.
- Korrosion bei Baustahl
- Anodengitter für den kathodischen Korrosionsschutz
- Korrosion an einer Säule der Lieserschluchtbrücke
- KKS-Felder bei Lieserschluchtbrücke
Elektroden für den kathodischen Korrosionsschutz werden auch aus titanummanteltem Kupfer (englisch titanium clad copper) oder Silber-Silberchlorid eingesetzt.
Ohne Fremdstrom



Aktiver Korrosionsschutz ohne Fremdstrom schützt vornehmlich Metalle, die oft in Berührung mit korrosiven Substanzen wie Wasser kommen. Als Anode dient ein unedlerer Stoff, der für das edlere Metall geopfert wird. Beim Korrosionsschutz mittels Opferanode werden je nach Anwendung Anoden aus unterschiedlichen Werkstoffen verwendet. Die Opferanode muss mit dem zu schützenden Metall leitfähig verbunden sein, um einen Schutz zu erreichen. Im resultierenden Stromkreis fließt ein Strom von wenigen Milliampere, der aus der Redoxreaktion der Oxidation dieser Opferanode gespeist wird.
Im Falle von Eisen und Magnesium läuft die Reaktion wie folgt ab:
Sobald Magnesium oder Eisen mit dem Wasser in Kontakt kommt, wird es zu Mg2+ bzw. Fe2+ oxidiert. Dabei entsteht entsprechend der elektrochemischen Spannungsreihe ein Potenzialunterschied zwischen dem Magnesium und dem Eisen von 1,9 V (Standardpotentiale bei 25 °C; 101,3 kPa; pH=0; Ionenaktivitäten=1). Da das Magnesium mit einem Potenzialunterschied zum Wasserstoff von −2,362 V ein wesentlich negativeres Potenzial als Eisen mit −0,41 V aufweist, wird Magnesium an der Anode oxidiert und das Eisen unter Elektronenaufnahme reduziert. Diese Reaktion läuft nur sehr langsam ab, kann aber durch veränderte Bedingungen beschleunigt werden. Die auf das Wasser treffenden Elektronen spalten dieses nun in H2 und 2OH− auf. Das Eisen verändert sich nicht, da es die vom Magnesium abgegebenen Elektronen wieder aufnehmen kann. Das Magnesium hingegen löst sich nach und nach auf und muss nach vollständigem Abbau erneuert werden.
Die Magnesiumanode wird bei kugelförmigen Behältern mittig positioniert, damit das Potenzial an allen Oberflächen des Behälters denselben Wert annimmt. Bei zylindrischen Behältern wird die Anode so angebracht, dass zum Behälterböden in etwa der gleiche Abstand besteht wie zu den kreisrunden Behälterwänden. Die Anode ist also kürzer als der Behälter tief ist. Vielfach wird die Anode zur Wandung des Behälters isoliert eingebaut, da sonst ein höherer Schutzstrom an der Einbaustelle fließen würde, während der übrige Behälter weniger gut geschützt würde. Der Stromkreis wird dann über ein Kabel geschlossen, das auf der Außenseite des Behälters mit der Anode und der Behälterwandung verbunden ist. In das Kabel kann zudem ein Strommessgerät für Gleichstrom eingeschleift werden, das den fließenden Strom im Milliamperebereich misst und so die Funktionsfähigkeit der Anode anzeigt.
Um aus Stahl gefertigte Schiffe vor Korrosion durch das Meerwasser zu schützen, werden außen am Schiffsrumpf in regelmäßigen Abständen Magnesiumanoden angebracht.

Eisen steht in der elektrochemischen Spannungsreihe positiver als Zink, d. h. Zink ist unedler als Eisen und stellt im galvanischen Element die Anode dar, und Eisen ist die Kathode. Eisen als edleres Metall ist daher so lange kathodisch geschützt, bis das Zink wegkorrodiert ist.
Zur Feststellung der Korrosionsfestigkeit von Beschichtungen werden genormte Umweltprüfungen durchgeführt. Hierbei werden zum Beispiel Oberflächen mit Ritzprüfgeräten leicht verletzt, und dann einem Salzsprühnebel ausgesetzt.
Beispiel
Ein einfacher Versuch zum Korrosionsschutz:
- Ein ungeschützter Eisennagel wird in angesäuertes Salzwasser gegeben. Nach einiger Zeit geht Eisen in Lösung und korrodiert (soweit keine Opferanode vorhanden ist). Des Weiteren bildet sich Wasserstoff (H2) am Eisennagel.
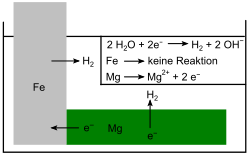
- Der Eisennagel wird mit dem unedleren Magnesium geschützt. Es kommt zur Bildung eines Lokalelements, indem Magnesium (Mg) als Anode wirkt und somit für das Eisen (Fe) opfert. Auch hier bildet sich Wasserstoff H2 an der Fe-Kathode. Der Grund hierfür ist der Elektronenfluss (e−) vom Mg zum Fe, da Mg unedler ist als Eisen und somit ein größeres Reduktionsvermögen besitzt.
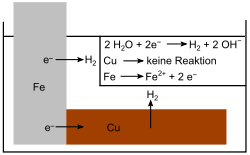
- Wird statt dem Magnesium das edlere Kupfer (Cu) verwendet, wirkt das Eisen als Anode und das Kupfer kann das Eisen nicht vor der Korrosion schützen. Das Eisen wird schneller oxidiert, als wenn kein Kupfer anwesend ist, denn der Elektronenfluss verläuft nun vom Fe zum Cu.
- Abb. 1: Eisen in wässriger Lösung
- Abb. 2: Eisen mit Magnesiumanode in wässriger Lösung
- Abb. 3: Eisen und Kupferanode in wässriger Lösung
Siehe auch
- Feuerverzinken
- Filmverzinkung
- Gesellschaft für Korrosionsschutz
- Zinklamellenüberzug
- Heißschrauben-Compound
- Sherardisieren (Diffusionsverzinken)
Literatur
- Bernhard Wietek: KKS in der Brückeninstandsetzung. Seminar KKS in Innsbruck 2000.
- Ulrich Bette, W. Vesper: Taschenbuch für den Kathodischen Korrosionsschutz. 7. Auflage. Vulkan, 2005, ISBN 3-8027-2932-3.
- R. P. Gieler, A. Dimmig-Osburg: Kunststoffe für den Bautenschutz und die Betoninstandsetzung. Birkhäuser Verlag, Berlin 2006, ISBN 3-7643-6345-2.
Weblinks
Einzelnachweise
- ↑ Was ist aktiver Korrosionsschutz? Abgerufen am 30. März 2021.
- ↑ DIN EN ISO 12 944 Teil 1
- ↑ B. Heinrich, H. Hildebrand, M. Schulze, W. Schenk, in: 3R international. 17. Jg., Heft 7, Juli 1978, S. 455.
- ↑ W. Schwenk, in: Zentralblatt für Industriebau. 26. Jg., Nr. 5, Sept.1980, S. 309.
- ↑ W. Schwenk, in: Zentralblatt für Industriebau. 26. Jg., Nr. 5, Sept.1980, S. 308.
- ↑ hammerite.de: Technisches Merkblatt Rostschutzfarbe, abgerufen am 15. April 2016.
- ↑ motipdupli.com: Technisches Merkblatt Bob Rostversiegelung, abgerufen am 15. April 2016.
Auf dieser Seite verwendete Medien
Autor/Urheber: Dr. Peter Klamser, Klostersiedlung 49, 39435 Egeln, klamser@gmail.com, Lizenz: CC BY-SA 3.0
gebrauchte Magnesiumanode für kathodische Korrosionsschutzanlage mit Maßstab
Autor/Urheber: Bertbau, Lizenz: CC BY-SA 4.0
KKS-Felder bei der Lieserschluchtbrücke in Kärnten
Autor/Urheber: Dr. Peter Klamser, Klostersiedlung 49, 39435 Egeln, klamser@gmail.com, Lizenz: CC BY-SA 3.0
Korrosionsscchutzstrommessgrät an einer kathodischen Korrosionsschutzanlage
Autor/Urheber: Roland Mattern, Lizenz: CC BY 3.0
Eisennagel mit Kupfer-Anode
Autor/Urheber: Dr. Peter Klamser, Klosterseidlung 49, 39435 Egeln, klamser@gmail.com, Lizenz: CC BY-SA 3.0
Deckel eines Boilers mit kathodischem Korrosionsschutz
Autor/Urheber: Roland Mattern, Lizenz: CC BY 3.0
Eisennagel mit Magnesium-Anode
Autor/Urheber: Trissi1234, Lizenz: CC BY-SA 4.0
Feuerverzinkte Wendeltreppe
Autor/Urheber: Bertbau, Lizenz: CC BY-SA 4.0
Korrosion bei Säule der Lieserschluchtbrücke der Tauernautobahn in Kärnten
Autor/Urheber: Roland Mattern, Lizenz: CC BY 3.0
Korrosionsschutz von Stahl durch Zinkschicht