Hofmann-Umlagerung
Bei der Hofmann-Umlagerung (auch Hofmann-Abbau oder Hofmann-Säureamid-Abbau) handelt es sich um eine Namensreaktion in der Organischen Chemie, die nach ihrem Entdecker August Wilhelm von Hofmann (1818–1892) benannt wurde. Hierbei wird ein unsubstituiertes Carbonsäureamid mit Brom Br2 in Gegenwart einer Base in Wasser umgesetzt. Dabei entsteht ein um die Carbonyl-Gruppe gekürztes Amin.[1][2][3] Diese Eliminierung der Carbonyl-Gruppe des Amids ist eng mit der Curtius-Reaktion, dem Lossen-Abbau und der Schmidt-Reaktion verwandt.[4]
Übersichtsreaktion
Die Hofmann-Umlagerung ist ein Abbau von Carbonsäureamiden zu primären Aminen:
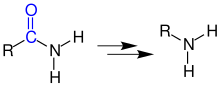
Mechanismus
Im ersten Schritt greift das Hydroxidion ein Proton der Aminogruppe an. Im nächsten Schritt bindet ein positiv polarisiertes Brom-Atom an das negativ geladene Stickstoff-Atom. Diese beiden Reaktionsschritte können auch in einen zusammengefasst werden: Im alkalischen Milieu bildet sich aus Brom das reaktive Hypobromit, das mit seiner positiven Partialladung die nucleophile Aminogruppe angreift, es entsteht ein N-Bromamid. Dieses kann wegen seiner NH-Acidität durch ein weiteres Hydroxidion deprotoniert werden. Von diesem Anion wird das Bromid abgespalten und der Rest R (Alkyl- oder Arylrest) des Nitrens wandert unter Bildung eines Isocyanats zum Stickstoff. Das Isocyanat lagert Wasser an und reagiert zu einer Carbamidsäure. Diese ist in wässriger alkalischer Lösung nicht stabil und decarboxyliert. Es entsteht ein primäres Amin.[5]

Bei den verwandten Reaktionen wie der Curtius-Umlagerung, der Schmidt-Reaktion oder dem Lossen-Abbau lässt sich im entsprechenden Reaktionsschritt das Intermediat Nitren nicht tatsächlich als Zwischenprodukt formulieren. Vielmehr bildet sich in einer konzertierten Reaktion über eine Umlagerung das Isocyanat unmittelbar aus dem N-Bromamid.
Varianten
Brom kann durch andere Reagenzien, wie Chlor (Cl2) oder N-Bromsuccinimid (NBS) mit 1,8-Diazabicyclo[5.4.0]undec-7-en (DBU) als Base ersetzt werden. Im folgenden Beispiel wird das intermediäre Isocyanat durch Methanol zu einem Urethan umgesetzt:[6]
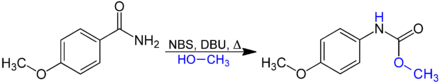
Als Alternative zu Brom kann auch [Bis(trifluoracetoxy)iod]benzol eingesetzt werden.[7]
Einzelnachweise
- ↑ A. W. Hofmann: Ueber die Einwirkung des Broms in alkalischer Lösung auf Amide. In: Berichte der deutschen chemischen Gesellschaft. Band 14, Nr. 2, Juli 1881, S. 2725–2736, doi:10.1002/cber.188101402242.
- ↑ Everett S. Wallis, John F. Lane: The Hofmann Reaction. In: Organic reactions. Band 3, Nr. 7, 1946, S. 267–306, doi:10.1002/0471264180.or003.07 (Übersichtsartikel).
- ↑ T. Shioiri: The Hofmann reaction. In: Comprehensive Organic Synthesis. Volume 6: Heteroatom Manipulation, 1991, S. 800–806 (Übersichtsartikel). Der Artikel ist ein Unterkapitel in: Takayuki Shioiri: Degradation Reactions. In: Ian Fleming, Barry M. Trost (Hrsg.): Comprehensive Organic Synthesis. Volume 6: Heteroatom Manipulation. Pergamon, Oxford 1991, ISBN 978-0-08-052349-1, S. 795–828, doi:10.1016/B978-0-08-052349-1.00172-4.
- ↑ T. Laue, A. Plagens: Namens- und Schlagwortreaktionen der Organischen Chemie. Teubner Verlag, 2006, ISBN 3-8351-0091-2, S. 189–190.
- ↑ K. Peter C. Vollhardt, Neil E. Schore, Übersetzung herausgegeben von Holger Butenschön: Organische Chemie. Weinheim 2020, ISBN 978-3-527-34582-3, S. 1110–1111
- ↑ J. W. Keillor, X Huang: Methyl Carbamate Formation via modified Hofmann Rearrangement Reactions: Methyl N-(p-Methoxyphenyl)carbamate In: Organic Syntheses. 78, 2002, S. 234, doi:10.15227/orgsyn.078.0234; Coll. Vol. 10, 2004, S. 549 (PDF).
- ↑ M. R. Almond,J. B. Stimmel, E. A. Thompson, G. M. Loudon: Hofmann Rearrangement under mildly acidic Conditions using (I,I-bis(Trifluoroacetoxy))iodobenzene: Cyclobutylamine Hydrochloride from Cyclobutanecarboxamide In: Organic Syntheses. 66, 1988, S. 132, doi:10.15227/orgsyn.066.0132; Coll. Vol. 8, 1993, S. 132 (PDF).
Auf dieser Seite verwendete Medien
Struktur von Hofmann-Umlagerung
Autor/Urheber: Jü, Lizenz: CC BY-SA 4.0
Schematische Präsentation des Hofmann-Abbaus von Carbonsäureamiden zu primären Aminen


