Heptanal
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Heptanal | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C7H14O | ||||||||||||||||||
| Kurzbeschreibung | farblose Flüssigkeit mit unangenehmem Geruch[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 114,19 g·mol−1 | ||||||||||||||||||
| Aggregatzustand | flüssig | ||||||||||||||||||
| Dichte | 0,82 g·cm−3 (20 °C)[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | 153 °C[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit | schlecht in Wasser (1,25 g·l−1 bei 25 °C)[2] | ||||||||||||||||||
| Brechungsindex | 1,4113[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Heptanal ist ein Aldehyd und eine farblose Flüssigkeit mit scharfem unangenehmen Geruch. Der Trivialname lautet Heptaldehyd.
Vorkommen

Heptanal kommt natürlich in den essentiellen Ölen von Ylang-Ylang (Cananga odorata),[4] Muskatellersalbei (Salvia sclarea),[4] Zitrone (Citrus x limon),[4] Bitterorange (Citrus x aurantium),[4] Rose (Rosa),[4] Hyazinthe (Hyacinthus)[4] und Gartenhyazinthe[5] vor.
Darstellung
Die Entstehung von Heptanal bei der fraktionierten Destillation von Rizinusöl[6] wurde bereits 1878 beschrieben. Die großtechnische Darstellung beruht auf der pyrolytischen Spaltung von Ricinolsäureestern[7] (Arkema-Verfahren) und auf der Hydroformylierung von 1-Hexen mit Rhodium-2-Ethylhexanoat als Katalysator unter Zusatz von 2-Ethylhexansäure (Oxea-Verfahren):[8]

Eigenschaften
Heptanal ist eine entzündliche wenig flüchtige farblose Flüssigkeit von durchdringend fruchtigem bis ölig-fettigem Geruch,[9] welche mit Alkoholen mischbar[4] und praktisch unlöslich in Wasser ist.[2] Wegen seiner Oxidationsempfindlichkeit wird Heptanal unter Stickstoff abgefüllt und mit 100ppm Hydrochinon stabilisiert.[10]
Heptanal bildet entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt von 39,5 °C.[2] Der Explosionsbereich liegt zwischen 1,1 Vol.‑% als untere Explosionsgrenze (UEG) und 5,2 Vol.‑% als obere Explosionsgrenze (OEG).[2] Die Zündtemperatur beträgt 205 °C.[2] Der Stoff fällt somit in die Temperaturklasse T3.
Verwendung
Aus Heptanal kann durch Reduktion mittels Wasserstoffaddition 1-Heptanol produziert werden:
Bei der Oxidation von Heptanal mit Sauerstoff in Gegenwart von Rhodium-Katalysatoren bei 50 °C wird in 95 %iger Ausbeute Heptansäure erhalten.[11] In einer Knoevenagel-Reaktion reagiert Heptanal mit Benzaldehyd unter basischer Katalyse mit hoher Ausbeute und Selektivität (> 90 %) zum alpha-Pentylzimtaldehyd (wegen des jasmintypischen Geruchs auch Jasminaldehyd genannt),[12] das meist als cis/trans-Isomerengemisch in Parfümzubereitungen Verwendung findet.[13]
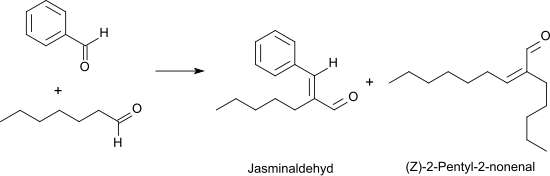
Als Nebenprodukt entsteht durch Selbstkondensation des Heptanals das unangenehm ranzig riechende (Z)-2-Pentyl-2-nonenal.[14] Heptanal kann in Gegenwart von wässriger Borsäure bei azeotroper Entfernung des Wassers praktisch quantitativ in (Z)-2-Pentyl-2-nonenal überführt werden.[15]

Vollständige Hydrierung liefert den auch durch Guerbet-Reaktion aus 1-Heptanol zugänglichen verzweigten primären Alkohol 2-Pentylnonan-1-ol.[16]
Sicherheitshinweise
Das Einatmen, das Verschlucken oder die Aufnahme über die Haut kann zu Gesundheitsschäden führen. Es kann die Atemwege, Verdauungswege und Augen reizen: z. B. Brennen, Kratzen. Es kann weiterhin die Haut reizen: z. B. Brennen, Juckreiz.
Einzelnachweise
- ↑ Eintrag zu HEPTANAL in der CosIng-Datenbank der EU-Kommission, abgerufen am 23. Oktober 2021.
- ↑ a b c d e f g h i j k l m n Eintrag zu Önanthaldehyd in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2020. (JavaScript erforderlich)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-274.
- ↑ a b c d e f g George A. Burdock: Fenaroli’s Handbook of Flavor Ingredients. 5. Auflage. CRC Press, Boca Raton, Fl. 2005, ISBN 0-8493-3034-3, S. 781 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ N-HEPTANAL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 25. Juli 2023.
- ↑ F. Krafft, Distillation of castor oil, under educed pressure, Analyst, 3, 329a (1878).
- ↑ A. Chauvel, G. Lefebvre, Petrochemical Processes: Technical and Economic Characteristics, Band 2, S. 277, Editions Technip, Paris, 1989, ISBN 2-7108-0563-4.
- ↑ Patentanmeldung DE102007053385A1: Verfahren zur Herstellung von Aldehyden. Angemeldet am 9. November 2007, veröffentlicht am 20. Mai 2009, Anmelder: Oxea Deutschland GmbH, Erfinder: Andreas Fischbach et al.
- ↑ Richtwerte für gesättigte azyklische aliphatische C4- bis C11-Aldehyde in der Innenraumluft, Bundesgesundheitsbl - Gesundheitsforsch –Gesundheitsschutz, 2009, 52:650–659, doi:10.1007/s00103-009-0860-2.
- ↑ Acros Organics, Sicherheitsdatenblatt, Heptaldehyde, stabilized, überarb. am 19. November 2012.
- ↑ Patent DE10010771C1: Verfahren zur Herstellung aliphatischer Carbonsäuren aus Aldehyden. Angemeldet am 4. März 2000, veröffentlicht am 3. Mai 2001, Anmelder: Celanese Chem Europe GmbH, Erfinder: Helmut Springer, Peter Lappe.
- ↑ M. Perez-Sanchez, P. Dominguez de Maria, Synthesis of natural fragrance jasminaldehyde using silica-immobilized piperazine as organocatalyst, Catal. Sci. Technol., 3, 2732-2736 (2013), doi:10.1039/C3CY00313B
- ↑ Riechstofflexikon A, alpha-Amylzimtaldehyd, Letzte Änderung am 4. August 2000.
- ↑ J. M. Hornback, Organic Chemistry, 2nd edition, S. 886, Thomson Brooks/Cole, 2006, ISBN 0-534-49317-3.
- ↑ R.D. Offenhauer, S.F. Nelsen, Aldehyde and ketone condensation reactions catalyzed by boric acid, J. Org. Chem., 33(2), 775-777 (1968), doi:10.1021/jo01266a059.
- ↑ G.H. Knothe:Lipid Chemistry, Guerbet Compounds ( vom 21. Mai 2016 im Internet Archive), AOCS Lipid Library, 22. Dezember 2011.
Auf dieser Seite verwendete Medien
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for flammable substances
Autor/Urheber: ChemDoc 2010, Lizenz: CC BY-SA 3.0
alpha-Amylcinnamic aldehyde (Jasmine aldehyde) by aldol condensation of benzaldehyde with heptanal
1-Heptanol synthesis
Autor/Urheber:
André Karwath aka Aka
, Lizenz: CC BY-SA 2.5Dieses Bild zeigt eine ganze und eine aufgeschnittene Zitrone.
Autor/Urheber: ChemDoc 2010, Lizenz: CC BY-SA 3.0
2-Pentyl-2-nonenal by self-condensation of heptanal
Autor/Urheber: Jü, Lizenz: CC BY-SA 4.0
Hydroformylation of 1-Hexene: Synthesis of Heptanal








