Hashimoto-Thyreoiditis
| Klassifikation nach ICD-10 | |
|---|---|
| E06.3 | Hashimoto-Thyreoiditis Hashitoxikose (transitorisch) Lymphozytäre Thyreoiditis Struma lymphomatosa (Hashimoto) |
| ICD-10 online (WHO-Version 2019) | |
Die Hashimoto-Thyreoiditis (Synonyme: Hashimoto-Thyroiditis, Struma lymphomatosa Hashimoto, (chronische) lymphozytäre Thyreoiditis, Ord-Thyreoiditis, Hashimoto-Krankheit) ist eine Autoimmunerkrankung, die zu einer chronischen Entzündung der Schilddrüse führt. Bei dieser Erkrankung wird Schilddrüsengewebe infolge eines fehlgeleiteten Immunprozesses durch T-Lymphozyten zerstört. Darüber hinaus ist eine Antikörperbildung gegen schilddrüsenspezifische Antigene nachweisbar. Die Erkrankung führt auf Dauer zu einer Schilddrüsenunterfunktion, wobei sich zu Beginn – bedingt durch die Zerstörung des Schilddrüsengewebes – auch Phasen der Überfunktion zeigen können. Der Krankheitsverlauf ist bei den meisten Erkrankten leicht und bei einigen mittelschwer oder schwer. Die Symptome sind vielfältig und – gerade am Beginn der Erkrankung – schwierig einzuordnen. Die Hashimoto-Thyreoiditis ist derzeit nicht heilbar; sie kann nicht ursächlich behandelt werden. Wenn die Schilddrüse wegen ihrer chronischen Entzündung nicht mehr ausreichend Schilddrüsenhormone herstellen kann, muss die Unterfunktion durch eine Substitution therapiert werden: der Erkrankte nimmt täglich orale Schilddrüsenhormone ein.
Die Krankheit wurde nach dem japanischen Arzt Hakaru Hashimoto (1881–1934) benannt, der sie 1912 als Erster beschrieb.[1] Der Charakter als Autoimmunerkrankung wurde 1956 von Deborah Doniach und Ivan Roitt erkannt.
Formen

Es sind zwei verschiedene Verlaufsformen bekannt:
- Die Hashimoto-Thyreoiditis i. e. S. (Autoimmunthyreopathie Typ 1A und 2A), mit einer Vergrößerung (Hypertrophie) der Schilddrüse („Kropf“ oder „Struma“)
- Die Ord-Thyreoiditis (Autoimmunthyreopathie Typ 1B und 2B), mit einer Verkleinerung (Atrophie) der Schilddrüse. Sie wurde nach William Miller Ord benannt, der sie erstmals 1878 beschrieb.[2]
Da sich Symptome, Diagnostik, Therapie und Prognose der beiden Formen nicht wesentlich unterscheiden und beide Formen jeweils ineinander übergehen können, werden sie heute in der Regel unter dem Begriff der Hashimoto-Thyreoiditis zusammengefasst. Bei beiden Verlaufsformen (die atrophe Form ist viel häufiger als die hypertrophe Form) kommt es auf Dauer zu einer Schilddrüsenunterfunktion, wobei sich zu Beginn der Erkrankung – bedingt durch die Zerstörung des Schilddrüsengewebes – auch Phasen der Überfunktion zeigen können (sog. „Leck-Hyperthyreose“, im Extremfall Hashitoxikose). Die Krankheit gilt als nicht heilbar, aber sehr gut behandelbar.
Die Hashimoto-Thyreoiditis wird zur Gruppe der polyendokrinen Autoimmunerkrankungen gezählt und tritt daher gehäuft mit weiteren Leiden wie Morbus Addison, Diabetes mellitus vom Typ I, Zöliakie, Vitiligo und Hypoparathyreoidismus auf (siehe #Assoziierte Erkrankungen).
Epidemiologie
Die Hashimoto-Thyreoiditis ist eine der häufigsten Autoimmunerkrankungen des Menschen und die häufigste Ursache der primären Schilddrüsenunterfunktion. Eine US-amerikanische Erhebung aus dem Jahr 2003[3] fand bei 10 % der Probanden einer Bevölkerungsstichprobe erhöhte Antikörper, bei 4,3 % subklinische und bei 0,3 % klinisch manifeste Hypothyreosen. Eine neuere Studie[4] fand 10 % klinische und subklinische Hypothyreosen. Lehrbüchern zufolge liegt die Erkrankungshäufigkeit der mit einer Hashimoto-Thyreoiditis häufig einhergehenden Schilddrüsenunterfunktion in Westeuropa bei 1–2 %; subklinische Verläufe sind jedoch häufiger und liegen im Bereich von 6–8 %.[5] Frauen erkranken deutlich häufiger als Männer (Verhältnis 2:1 bis 5:1). Es finden sich familiäre Häufungen, d. h., es wird nur die Veranlagung für Hashimoto vererbt. Beobachtungen zeigen, dass die Hashimoto-Thyreoiditis in zeitlichem Zusammenhang mit hormonellen Umstellungen (Pubertät, Entbindung, Wechseljahre) und Belastungssituationen entstehen kann.
Ursachen
Die genauen Wirkfaktoren, die zum Ausbruch einer Hashimoto-Thyreoiditis führen können, sind noch nicht hinreichend geklärt. Zur Debatte stehen neben einer familiären (genetischen) Vorbelastung auch Stress, schwer verlaufende Viruserkrankungen (wie Pfeiffer-Drüsenfieber, Gürtelrose), Dysfunktionen der Nebennierenrinde, Mikrochimerismus und Umwelteinwirkungen. Überzufällig häufig findet sich die Hashimoto-Thyreoiditis beim PCO-Syndrom.[6] Debattiert wird zurzeit über die Bedeutung einer übermäßigen Jodzufuhr für den Ausbruch der Krankheit. Als relativ sicher kann gelten, dass sie, genau wie Morbus Basedow, durch sehr hohe Joddosen (Jodexzess) ausgelöst werden kann (z. B. durch jodhaltige Kontrastmittel). Mögliche Gefahren, die von einer Jodierung der Nahrungsmittel (als Folge der Futtermitteljodierung bei Nutztieren und der Kochsalzjodierung) ausgehen, werden diskutiert (vgl. Jodmangel, Jodunverträglichkeit).
Neue Studien zeigen, dass auch eine milde (ggf. asymptomatische) COVID-19-Erkrankung eine Hashimoto-Thyreoiditis auslösen kann.[7][8][9]
Symptome und Krankheitsverlauf
Symptome
Aufgrund der möglichen anfänglichen Hyperthyreose (Schilddrüsenüberfunktion) können für eine gewisse Zeit folgende Symptome und Befunde auftreten: Nervosität, Abgeschlagenheit, Schwäche, vermehrtes Schwitzen, Wärmeintoleranz, Tremor, Überaktivität, Palpitationen, veränderter Appetit (meist gesteigert), verändertes Gewicht (meist Gewichtsabnahme), Zyklusstörungen, Tachykardie und Herzrhythmusstörungen, arterielle Hypertonie, warm-feuchte und weiche Haut, Hyperreflexie, Muskelschwäche.[10]
Langfristig folgt schließlich das Einsetzen der Hypothyreose (Schilddrüsenunterfunktion) mit folgenden Symptomen und Befunden:[11] Müdigkeit und Schwäche[12], Abgeschlagenheit, Schläfrigkeit, mentale Beeinträchtigung, Konzentrationsschwierigkeiten und Gedächtnisschwäche,[12] Depression, Kältegefühl[12] und Kälteintoleranz, kalte Gliedmaßen,[12] Heiserkeit, trockene Haut, raue Haut,[12] verminderte Schweißneigung, Gewichtszunahme, Appetitlosigkeit, Verstopfung, Zyklusstörungen, verminderte Fruchtbarkeit, Gelenkschmerzen, Missempfindungen (Parästhesien), beeinträchtigtes Hörvermögen,[12] Luftnot,[12] verlangsamte Bewegungen, verlangsamtes Sprechen, Bradykardie, Myxödem, verzögerte Reflexe, diffuser Haarausfall,[12] periphere Ödeme,[12] Ergüsse in serösen Höhlen,[12] Karpaltunnelsyndrom.[12]
Zu den allgemeinen Symptomen der veränderten Stoffwechsellage kommen bei einem Teil der Patienten noch spezifische Veränderungen wie Struma oder endokrine Orbitopathie,[13] selten auch eine schmerzhafte Schilddrüse.[12]
Assoziierte Erkrankungen
Die Hashimoto-Thyreoiditis ist mit einer Reihe anderer Erkrankungen assoziiert.[13] Das heißt, diese anderen Erkrankungen treten unabhängig von einer etwaigen Behandlung überzufällig häufig bei Hashimoto-Patienten auf. Ein ursächlicher Zusammenhang ist mit solch einer Assoziation aber nicht notwendigerweise gegeben. Zu den assoziierten Erkrankungen zählen der Morbus Basedow und das B-Zell-Lymphom der Schilddrüse, Depressionen und die Hashimoto-Enzephalopathie. Schwache Assoziationen finden sich mit dem papillären Schilddrüsenkarzinom und mit Brustkrebs. Die Hashimoto-Thyreoiditis ist darüber hinaus als Autoimmunerkrankung mit anderen Autoimmunerkrankungen assoziiert; hierzu zählen im Falle der Hashimoto-Thyreoiditis insbesondere die polyendokrinen Autoimmunerkrankungen (Vitiligo, perniziöse Anämie bei Autoimmungastritis,[14] Morbus Addison,[14] Alopecia areata, Diabetes mellitus Typ I[14]), die Zöliakie,[14] die rheumatoide Arthritis[14] und andere Erkrankungen des rheumatischen Formenkreises, Autoimmunhepatitis, primär biliäre Zirrhose, Dermatitis herpetiformis, Autoimmunthrombozytopenie, Systemischer Lupus erythematodes,[12] Sjögren-Syndrom[12] oder die Nesselsucht[15][16].
Krankheitsverlauf
Der Krankheitsverlauf ist bei einem Großteil der Erkrankten leicht, doch sind auch mittelschwere und schwere Verläufe bekannt. Die Symptome sind vielfältig und – gerade am Beginn der Erkrankung – schwierig einzuordnen. Die Vielzahl und Variabilität der Symptome sowie der schleichende Verlauf erschweren die Diagnose.
Symptome einer Unterfunktion können bereits bei subklinischen (noch als euthyreot geltenden) Wertekonstellationen auftreten, weil der individuelle Wertespielraum in der Regel sehr viel kleiner ist als das auf statistischen Auswertungen beruhende, interindividuelle Referenzwertspektrum. Selbst subklinische Wertekonstellationen können daher bereits eine Minderung der Lebensqualität nach sich ziehen.
In extrem seltenen Fällen geht mit der Krankheit die Hashimoto-Enzephalopathie einher mit neurologischen Symptomen wie epileptischen Anfällen oder psychiatrischen Symptomen wie Halluzinationen.
Diagnose

Diagnostisch relevant sind:
- Thyreoperoxidase-Antikörper (Antikörper gegen Thyreoperoxidase = Thyroidperoxidase) (TPO-AK), auch Mikrosomale Antikörper (MAK) genannt
- Antikörper gegen Thyreoglobulin (Tg-AK bzw. TAK)
Im weit überwiegenden Teil der Fälle sind die TPO-Antikörper erhöht (mit oder ohne Erhöhung der Tg-AK). In einem weitaus geringeren Teil der Fälle sind nur die Tg-Antikörper (stärker) erhöht. In sehr seltenen Fällen liegt eine Hashimoto-Thyreoiditis vor, ohne dass die genannten Antikörper nachweisbar sind. Die Diagnose wird dann anhand anderer Kriterien (Struma ohne andere Erklärung oder lymphozytäre Infiltration in der Schilddrüsenpunktion) gestellt.
Für eine Beurteilung der Stoffwechsellage der Schilddrüse sind folgende Hormonwerte relevant:
- TSH (Thyroidea-Stimulierendes Hormon)
- T3 (Trijodthyronin), bzw. freies T3 (= fT3)
- T4 (Levothyroxin = L-Thyroxin = Tetrajodthyronin), bzw. freies T4 (= fT4)
Eine Schilddrüsendiagnostik, die sich ausschließlich auf den TSH-Wert stützt, ist zur Erkennung einer Hashimoto-Thyreoiditis meist nicht aussagekräftig genug, denn auch ein normwertiger TSH-Spiegel oder normwertige freie T3- und T4-Werte sind keine Ausschlusskriterien für eine Hashimoto-Thyreoiditis.
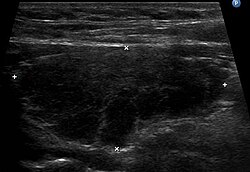
Sehr wichtig für die Diagnose ist zudem ein Sonogramm der Schilddrüse. Typischerweise erscheint die Schilddrüse im Ultraschallbild inhomogen und echoarm, was auf die laufende Zerstörung hinweist. Zudem kann die im Doppler-Sonogramm erkennbare verstärkte Durchblutung ein Hinweis auf eine Entzündung sein. Auch die Größe der Schilddrüse kann im Sonogramm beurteilt werden. Da die hypertrophe Form der Hashimoto-Thyreoiditis mit einer Struma einhergehen kann, sind Größen über ca. 18 ml (Frauen) bzw. ca. 25 ml (Männer) Gesamtvolumen als auffällig anzusehen. Kleine Schilddrüsen mit einer Größe unter 6 ml (Frauen) bzw. 8 ml (Männer) sind hingegen typisch für die atrophische Verlaufsform (Ord-Thyreoiditis), wobei einschränkend angemerkt werden muss, dass diese Größenangaben – je nach Autor – stark schwanken und Gegenstand der Diskussion sind. In Deutschland ist die sogenannte atrophische Verlaufsform mit schrumpfender Schilddrüse weitaus häufiger als die hypertrophe Form mit Kropfbildung (Struma).
Insbesondere zu Beginn der Erkrankung kann die Unterscheidung zwischen Hashimoto-Thyreoiditis und Morbus Basedow (eine Autoimmunerkrankung, die zur Überproduktion von Schilddrüsenhormonen führt) schwierig sein, da auch bei Hashimoto anfängliche Überfunktionsschübe vorliegen können und bei Morbus Basedow TPO-Ak und Tg-Ak positiv sein können. Gegebenenfalls kann eine Schilddrüsenszintigraphie Klarheit bringen, da sie bei Morbus Basedow einen erhöhten Uptake des Radiopharmakons zeigt, bei der Hashimoto-Thyreoiditis dagegen einen verminderten.
Endgültige Sicherheit bringt die histologische (feingeweblich-mikroskopische) Untersuchung von Schilddrüsengewebe, das mittels einer Feinnadelpunktion gewonnen wurde. Bei der Hashimoto-Thyreoiditis erkennt man neben anderen Kriterien vor allem ein dichtes Infiltrat von Lymphozyten und auch Lymphfollikel (siehe Abbildung), die Ausdruck der entzündlichen Vorgänge sind.
Diagnosekriterien
Für die Diagnostik einer Hashimoto-Thyreoiditis wurden unterschiedliche Kriteriensysteme entwickelt, die aber inhaltlich ähnlich sind.
Nach den Kriterien der Japan Thyroid Association wird folgendermaßen entschieden[17]:
| Klasse | Kriterien |
|---|---|
| Klinische Zeichen (A) | Vergrößerte Schilddrüse (Struma) ohne andere erklärende Ursache (z. B. Jodmangel, Morbus Basedow oder Schilddrüsenautonomie) |
| Laborbefunde (B) | positive MAK- bzw. TPO-Antikörper positive Tg-Antikörper lymphozytäre Infiltration in der punktionszytologischen Untersuchung |
- Definitive Diagnose: A + mind. ein Kriterium aus B erfüllt
- Verdachtsdiagnose 1: Hypothyreose ohne andere erklärbare Ursache
- Verdachtsdiagnose 2: Antikörper ohne Schilddrüsenfunktionsstörung oder Struma
- Mögliche Diagnose: Hypoechogene und/oder inhomogene Struktur in der Schilddrüsensonographie
Behandlung
Die Hashimoto-Thyreoiditis als Autoimmunprozess ist derzeit nicht heilbar und wird auch nicht ursächlich behandelt. Wenn die Schilddrüse aufgrund der chronischen Entzündung nicht mehr ausreichend Schilddrüsenhormone herstellen kann, muss die Unterfunktion durch (einschleichende) Substitution therapiert werden.
Die Substitution erfolgt durch tägliche orale Einnahme der Schilddrüsenhormone. Wegen des hohen physiologischen Hormonspiegels in den frühen Morgenstunden wird empfohlen, die Tablette am Morgen ca. 30 Minuten vor der ersten Mahlzeit einzunehmen. Dafür stehen unterschiedliche Möglichkeiten zur Verfügung: die alleinige Einnahme von Thyroxin (T4, Levothyroxin), wenn die Umwandlung von T4 zu T3 im Körper nicht gestört ist, oder eine Kombination aus T4 und T3 entweder als Kombinationspräparat mit festem T4/T3-Verhältnis oder mit frei dosierbaren Einzelpräparaten.
Der TSH-Wert und eventuell auch die Hormonspiegel fT3 und fT4 müssen regelmäßig überprüft werden, da sich im Laufe der Erkrankung Veränderungen einstellen können, die eine Dosisanpassung erfordern. Zusätzlich sollte die Schilddrüse in regelmäßigen Abständen (alle 6 bis 12 Monate) sonografisch kontrolliert werden.
Die erfolgreiche Einstellung dauert oft mehrere Monate bis zu 2 Jahre. Je länger eine Unterfunktion bereits andauert und je schwerer sie ist, desto langwieriger ist es in der Regel, einen befriedigenden Hormonstatus und Wohlbefinden zu erreichen. Da auch Schwankungen oder Schübe zum Krankheitsbild gehören können, ist bei der Dosisfindung teilweise viel Geduld erforderlich.
Die Substitutionstherapie ist in der Regel lebenslang erforderlich. Bei einer guten Einstellung ist der Patient meist beschwerdefrei und die Lebenserwartung nicht vermindert. Bei schweren Verläufen können die Beschwerden trotz Hormontherapie bestehen bleiben.
Bei L-Thyroxin können sich bereits geringe Dosisänderungen (z. B. von 12,5 μg) bemerkbar machen (geringe therapeutische Breite). Daher sollte möglichst kein Wechsel auf ein Präparat eines anderen Herstellers erfolgen, da nicht gewährleistet ist, dass die aufgenommene Wirkstoffmenge vergleichbar ist (Bioverfügbarkeit).[18] Deshalb findet sich L-Thyroxin auch auf der Substitutionsausschlussliste.[19]
Es gibt zwar Studien, die darauf hindeuten, dass sich eine Supplementierung mit dem Spurenelement Selen positiv auf den Immunprozess auswirkt.[20] Für eine damit einhergehende positive Wirkung auf die Schilddrüse fehlen jedoch aussagekräftige Belege.[21]
Behandlungsfehler
Jod in Tablettenform hingegen sollte bei einer Hashimoto-Thyreoiditis nicht zusätzlich eingenommen werden, da ein Jodüberschuss die Entzündung der Schilddrüse fördern kann. Daneben können getrocknete Algen und Seetang einen hohen Jodgehalt aufweisen, sodass es bereits bei kleinen Portionen zu einer hohen Jodzufuhr kommen kann.[22] Ansonsten gelten die in der Nahrung enthaltenen Jodmengen als unbedenklich.[23]
Literatur
- Petra-Maria Schumm-Draeger: Schilddrüsendiagnostik und -therapie. Update 2005. In: Bayerisches Ärzteblatt. Nr. 4. Bayerische Landesärztekammer, München 2005, S. 236–243 (bayerisches-aerzteblatt.de [PDF; abgerufen am 6. Juni 2016]).
- Terry F. Davies: Ord-Hashimoto’s disease. Renaming a common disorder–again. In: Thyroid. Official journal of the American Thyroid Association. Band 13, Nr. 4, April 2003, S. 317, doi:10.1089/105072503321669776, PMID 12820593.
Weblinks
Einzelnachweise
- ↑ Hakaru Hashimoto: Zur Kenntnis der lymphomatösen Veränderung der Schilddrüse (Struma lymphomatosa). In: Deutsche Gesellschaft für Chirurgie (Hrsg.): Archiv für klinische Chirurgie. Band 97. Springer, Berlin Januar 1912, S. 219–248.
- ↑ William Miller Ord: On myxœdema, a term proposed to be applied to an essential condition in the „cretinoid“ affection occasionally observed in middle-aged women. In: Royal Medical and Chirurgical Society of London (Hrsg.): Medico-Chirurgical Transactions. Band 61. Longmann, London 1878, S. 57–78.5, PMC 2150242 (freier Volltext).
- ↑ Joseph G. Hollowell et al.: Serum TSH, T(4), and thyroid antibodies in the United States population (1988 to 1994). National Health and Nutrition Examination Survey (NHANES III). In: The Journal of Clinical Endocrinology & Metabolism. Band 87, Nr. 2. Endocrine Society, Chevy Chase (Md.) März 2002, S. 489–499, doi:10.1210/jcem.87.2.8182, PMID 11836274.
- ↑ P. Valeix et al.: Thyroid hormone levels and thyroid dysfunction of French adults participating in the SU.VI.MAX study. In: Annales d’endocrinologie. Band 65, Nr. 6. Elsevier Masson, Amsterdam / Jena Dezember 2004, S. 477–486, PMID 15731735 (französisch: Statut thyroïdien et fréquences des dysthyroïdies chez les adultes inclus dans l’étude SU.VI.MAX en 1994-1995.).
- ↑ Meinhard Classen, Volker Diehl, Kurt Kochsiek, Wolfgang E. Berdel (Hrsg.): Innere Medizin. 5. Auflage. Urban & Fischer, München / Jena 2004, ISBN 3-437-42830-6.
- ↑ Christoph Keck (Hrsg.): Kinderwunschbehandlung in der gynäkologischen Praxis. Thieme, Stuttgart / New York (NY) 2014, ISBN 978-3-13-171671-2, S. 171.
- ↑ Kuan Peng, Xue Li, Deliang Yang, Shirley C.W. Chan, Jiayi Zhou, Eric Y.F. Wan, Celine S.L. Chui, Francisco T.T. Lai, Carlos K.H. Wong, Esther W.Y. Chan, Wai Keung Leung, Chak-Sing Lau, Ian C.K. Wong: Risk of autoimmune diseases following COVID-19 and the potential protective effect from vaccination: a population-based cohort study. In: eClinicalMedicine. Band 63, 16. August 2023, ISSN 2589-5370, S. 102154, doi:10.1016/j.eclinm.2023.102154 (thelancet.com [abgerufen am 21. August 2023]).
- ↑ Falko Tesch, Franz Ehm, Annika Vivirito, Danny Wende, Manuel Batram, Friedrich Loser, Simone Menzer, Josephine Jacob, Martin Roessler, Martin Seifert, Barbara Kind, Christina König, Claudia Schulte, Tilo Buschmann, Dagmar Hertle, Pedro Ballesteros, Stefan Baßler, Barbara Bertele, Thomas Bitterer, Cordula Riederer, Franziska Sobik, Lukas Reitzle, Christa Scheidt-Nave, Jochen Schmitt: Correction to: Incident autoimmune diseases in association with SARS-CoV-2 infection: A matched cohort study. In: Clinical Rheumatology. 5. Juli 2023, ISSN 1434-9949, doi:10.1007/s10067-023-06692-8 (springer.com [abgerufen am 21. August 2023]).
- ↑ Alessandro Rossini, Sara Cassibba, Francesca Perticone, Simone Vasilij Benatti, Serena Venturelli, Greta Carioli, Arianna Ghirardi, Marco Rizzi, Tiziano Barbui, Roberto Trevisan, Silvia Ippolito: Increased prevalence of autoimmune thyroid disease after COVID-19: A single-center, prospective study. In: Frontiers in Endocrinology. Band 14, 2023, ISSN 1664-2392, doi:10.3389/fendo.2023.1126683/full (frontiersin.org [abgerufen am 21. August 2023]).
- ↑ Lewis E. Braverman, David S. Cooper: Introduction to Thyrotoxicosis. In: Lewis E. Braverman, David S. Cooper: Werner & Ingbar’s the thyroid: a fundamental and clinical text. Lippincott Williams & Wilkins, Philadelphia 2013, S. 354–355, ISBN 978-1-4511-2063-9.
- ↑ Lewis E. Braverman, David S. Cooper: Introduction to Hypothyroidism. In: Lewis E. Braverman, David S. Cooper: Werner & Ingbar’s the thyroid: a fundamental and clinical text. Lippincott Williams & Wilkins, Philadelphia 2013, S. 523–524, ISBN 978-1-4511-2063-9.
- ↑ a b c d e f g h i j k l m n Jens Zimmermann, George Kahaly: Erkrankungen der Schilddrüse. In: Manfred Dietel et al. (Hrsg.): Harrisons Innere Medizin. 2. Auflage. ABW Wissenschaftsverlag, Berlin 2003, ISBN 3-936072-10-8, S. 2262–2263.
- ↑ a b Anthony P. Weetman: Chronic Autoimmune Thyroiditis. In: Lewis E. Braverman, David S. Cooper: Werner & Ingbar’s the thyroid: a fundamental and clinical text. Lippincott Williams & Wilkins, Philadelphia 2013, S. 525–535, ISBN 978-1-4511-2063-9.
- ↑ a b c d e D. Graf, D. Veit, S. Veit, K. Mann: Autoimmunthyreoiditis und assoziierte Autoimmunerkrankungen. In: J. Feldkamp (Hrsg.): Schilddrüse 2019: Schilddrüse und Autoimmunität. Lehmanns Media, Berlin 2019, ISBN 978-3-96543-161-4, S. 127–129.
- ↑ Jeanine Barone: Hashimoto’s Thyroiditis and Chronic Hives. In: EndocrineWeb. Remedy Health Media, 1. Dezember 2021, abgerufen am 5. Februar 2022 (englisch).
- ↑ Subothini Sara Selvendran, Nikhil Aggarwal: Chronic urticaria and thyroid autoimmunity: a perplexing association. In: Oxford Medical Case Reports (OMCR). National Center for Biotechnology Information, U.S. National Library of Medicine, 22. Februar 2018, abgerufen am 5. Februar 2022 (englisch).
- ↑ Japan Thyroid Association: Guidelines for the Diagnosis of Chronic Thyroiditis
- ↑ Der Arzneimittelbrief. Unabhängige Arzneimittelinformation: Bioäquivalenz von Levothyroxin-Präparaten. 2009, abgerufen am 23. Oktober 2021.
- ↑ Gemeinsamer Bundesausschuss: Anlage VII zum Abschnitt M der Arzneimittel-Richtlinie. 1. November 2021, abgerufen am 20. November 2021.
- ↑ Konstantinos A. Toulis et al.: Selenium supplementation in the treatment of Hashimoto’s thyroiditis. A systematic review and a meta-analysis. In: Thyroid. Official journal of the American Thyroid Association. Band 20, Nr. 10, Oktober 2010, S. 1163–1173, doi:10.1089/thy.2009.0351, PMID 20883174.
- ↑ Selen bei Hashimoto? In: Gute Pillen – Schlechte Pillen. 19. April 2021, abgerufen am 24. April 2021.
- ↑ Bundesinstitut für Risikobewertung: Gesundheitliche Risiken durch zu hohen Jodgehalt in getrockneten Algen Aktualisierte Stellungnahme Nr. 026/2007 des BfR vom 22. Juni 2004*. 12. Juni 2007, abgerufen am 24. Oktober 2021.
- ↑ R. Gärtner, P. C. Scriba: Warum Jod vermeiden bei Hashimoto-Thyreoiditis? In: BDI aktuell. Nr. 2, 2004, S. 24 (online [PDF; abgerufen am 4. März 2015]).
Auf dieser Seite verwendete Medien
Autor/Urheber: Patho, Lizenz: CC BY-SA 3.0
Hashimoto's thyroiditis with lymphoid infiltration. Autoantibodies against thyroid peroxidase and thyroglobulin were elevated.
Autor/Urheber: Drahreg01, Lizenz: CC BY-SA 3.0
Sonogramm der Schilddrüse (rechter Lappen im Längsschnitt) bei Hashimoto-Thyreoiditis in der hypertrophen Verlaufsform. Typische Echoarmut.


