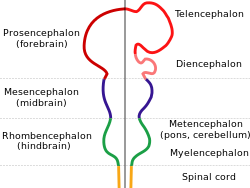Gehirnentwicklung beim Menschen
Die Gehirnentwicklung beim Menschen (auch: Hirnentwicklung) beginnt in der dritten Schwangerschaftswoche und ist erst nach der Pubertät, mehr als 20 Jahre nach der Geburt, weitgehend abgeschlossen.[1]
Ab dem zwölften Lebensjahr könnte man den Menschen hirnphysiologisch als mehr oder weniger erwachsen ansehen. Zu diesem Zeitpunkt ist auch der größte Teil des Hirnwachstums abgeschlossen.[2]
Unter den Primaten verfügt der Mensch über das größte Gehirn in Relation zu seiner Körpermasse. Dies ermöglicht ihm seine typisch menschlichen Fähigkeiten wie ausgeprägte Lernfähigkeit, komplexes Sozialverhalten und die Kommunikation durch Sprache.[3]
Die Abschnitte der Gehirnentwicklung
Die Entwicklung des menschlichen Gehirns kann in mehrere Abschnitte unterteilt werden, die jedoch gleitend ineinander übergehen.
Pränatale Gehirnentwicklung
Ab der dritten Entwicklungswoche, beginnt beim menschlichen Embryo die Entwicklung von Gehirn und Nervensystem.[4] Dazu bildet sich entlang des Rückenmarks aus der Neuralplatte (eine Zellplatte am Rücken des Embryos) ein Rohr aus Nervengewebe, das Neuralrohr. In diesem wachsen die entstehenden Nervenzellen bis zu ihrem Bestimmungsort, wobei sie sich an radial ausgerichteten Gliazellen orientieren.
In der vierten bis sechsten Woche formieren sich die Neuronen zu drei Ausbuchtungen, den Primärvesikeln. Aus diesen werden die Hirnareale Vorderhirn, Mittelhirn und Hinterhirn gebildet.[5] Auf dem Primärvesikel des Vorderhirns sitzt außerdem die Augenknospe, auf dem des Hinterhirns die Ohrknospe. Aus zwei Ausbuchtungen des Vorderhirns werden schließlich die beiden Gehirnhälften. Diese durchlaufen ein schnelles Wachstum und fangen an, sich über das Hinterhirn auszubreiten. Ab der elften Woche beginnt sich das Kleinhirn zu entwickeln. Bei der Geburt verfügt das Gehirn dann über seine vollständige Anzahl an Nervenzellen.
Bei der Betrachtung der Entwicklung des Nervensystems und damit des Gehirns ergeben sich grob fünf unterscheidbare Stadien:[6]
- Neuronale Induktion
- Neuronale Proliferation
- Migration, Aggregation und Differenzierung
- Bildung der Verbindungen
- neuronale Apoptose und Selektion der synaptischen Verschaltungen
Neuronale Induktion
Bei der neuronalen Induktion geht es darum, dass sich ein Teil des Ektoderms (die äußere Zellschicht des Embryos) in Gewebe umwandelt, das für die Bildung von Nervenzellen geeignet ist, nämlich die Neuroektoderm (die Neuralplatte). Das heißt, hier wird erstmals die Voraussetzung dafür geschaffen, dass sich ein Nervensystem und somit ein Gehirn entwickeln kann. Dieser Vorgang wird durch eine komplexe Wirkungskette verschiedener Induktions-Moleküle bewirkt:
- Grundlegend dafür ist die Hemmung der Ausschüttung von BMP (bone morphogenetic protein), das ansonsten die neuronale Entwicklung verhindern würde. Diese Hemmung wiederum wird durch Substanzen, wie Follistatin, Chordin und Noggin hervorgerufen, die im Chordafortsatz gebildet werden. Der Chordafortsatz ist ein sternförmiges Gebilde im Mesoderm (mittlere Zellschicht des frühen Embryos), das dazu mit dem Ektoderm verschmilzt. Dies ist die eine Seite der Differenzierung der Zellen im Ektoderm hin zu neuronalen Stammzellen, die durch das Mesoderm, also eine andere Zellschicht, induziert wird.
- Es gibt aber darüber hinaus noch einen weiteren Wirkungsfaktor. So haben neuere Untersuchungen gezeigt, dass bereits in einem früheren Stadium FGF (fibroblast growth factor) dazu dient, die Transkription von BMP zu unterdrücken. Außerdem ist FGF nötig, um zu einer neuronalen Ausgestaltung der Zellen zu führen.[7][8] Schließlich kommt es zur Differenzierung des Neuronalrohrs selbst, was zur Ausbildung der drei bekannten Gehirnareale in dieser Reihenfolge führt: Vorderhirn, Mittelhirn und Hinterhirn, sowie Rückenmark. Die Differenzierung wird durch Modulation der Genexpression induziert:
- Zunächst bewirkt am Vorderhirn die Prächordalplatte durch Expression von Transkriptionsfaktoren wie Emx (empty spiracle), Lim und Otx (orthodenticle) die Differenzierung der Zellen.
- Diese Aufgabe übernehmen am Mittel- und Hinterhirn der Cordafortsatz und das paraxiale Mesoderm.
- Weiterhin scheint der Isthmus-Organisator eine wichtige Rolle bei der Gliederung des Gehirns durch Expression von FGF und en (engrailed) zu spielen.[8] In diesem Zustand sind die Zellen noch nicht besonders spezialisiert und kleinere Gewebeschäden können leicht ausgeglichen werden. So kann man zum Beispiel Gewebe des Vorderhirn-Augen-Feldes entfernen, ohne dass es zu bleibenden Schäden kommen würde, da der Verlust an Zellen einfach durch vermehrte Zellteilung ausgeglichen wird.[9]
Neuronale Proliferation
Etwa ab dem 23. Tag der Schwangerschaft kommt es zur sogenannten Proliferation, eine Phase verstärkter Zellteilung der Neuronen-Stammzellen. Während die Anzahl an Zellen im Neuronalrohr mit ca. 125.000 Zellen relativ klein ist, kommt es – sobald das Neuronalrohr verschlossen ist – zu einem sprunghaften Anstieg der Teilungsrate, an der in diesem Stadium alle Zellen beteiligt sind. Dabei wandern die Zellen in einem Teilungszyklus von der Außenfläche des Neuronalrohrs zur Innenfläche, mit der sie durch einen dünnen Fortsatz verbunden sind. Bevor sie sich teilen, ziehen die Zellen diese Fortsätze ein, um sie nach der Teilung sofort wieder zu bilden. Je nachdem, ob der Teilungszyklus symmetrisch (d. h. vertikal) oder asymmetrisch (d. h. horizontal) ist, entstehen dabei zwei neue Zellen, die ihre Teilungsfähigkeit behalten, oder je eine Zelle mit und eine ohne erneute Teilungsfähigkeit.[10] Nach mehreren Teilungszyklen, abhängig vom Hirngebiet und der dortigen Zelldichte, scheiden die Zellen aus dem Teilungszyklus aus und wandern aus der Ventrikularschicht in die intermediäre Schicht, wo sie zu postmitotischen Neuronen differenzieren. Die intermediäre Schicht besteht dann letztendlich aus jungen Zellen ohne jegliche Teilungsfähigkeit und Vorstufen von Gliazellen mit lebenslanger Teilungsfähigkeit. Diesen Vorgang der Teilung und Differenzierung bezeichnet man als Neurogenese. Es ist noch unklar, wie genau die Bildung der verschiedenen Nerven- und Gliazellen an den verschiedenen Positionen im Nervensystem koordiniert ist. Prinzipiell scheint sie im Gehirn jedoch ähnlich wie im Rückenmark abzulaufen: Jede Nerven-Vorläuferzelle erhält durch außerhalb des Neuralrohrs produzierte Signale eine positionelle Information zugewiesen. Diese Position in Zusammenhang mit dem Zeitpunkt, zu dem die Zelle gebildet wurde, bestimmt dann ihr späteres Schicksal. Der Gradient an SHH-Molekülen (sonic hedgehog-Moleküle) ist dabei primär bestimmend für die spätere Region. Abhängig von seiner Konzentration fällt die Kontrolle von Homöodomänen Transkriptionsfaktoren der Klasse I, die unterdrückt werden, und Faktoren der Klasse II, die induziert werden, in den Neuronen-Vorläuferzellen aus. SHH führt somit zur Bildung von fünf verschiedenen Streifen ventraler Vorläuferzellen. Diese Muster bestimmen später, welche Transkriptionsfaktoren in den neuronalen Zellen exprimiert werden.[7][11]
Ebenfalls eine Rolle für die spätere Differenzierung scheint der Zeitpunkt des Ausscheidens aus dem Teilungszyklus zu spielen. Drei Aussagen lassen sich treffen:
- Große Neuronen oder solche mit relativ langen Axonen werden allgemein früher angelegt als kleine Nervenzellen oder solche mit relativ kurzen Axonen.
- Das Muster der Zeitpunkte, zu denen die Zellen aus dem Teilungszyklus ausscheiden, unterscheidet sich je nach Hirnregion. So hören zum Beispiel Zellen in der Großhirnrinde, die näher an der Oberfläche liegen, später auf sich zu teilen. Bei der Netzhaut des Auges ist es dagegen genau umgekehrt: Hier hören Zellen, die in oberflächlicheren Schichten der Netzhaut liegen, früher auf sich zu teilen.
- Obwohl die ersten Gliazellen zusammen mit den ersten Nervenzellen entstehen, überdauert ihre Produktion die der Nervenzellen.
Migration, Aggregation und Differenzierung
Die Wanderung der Zellen danach ist amöboid, das heißt, die Zellen senden einen Fortsatz aus, an dem sie entlang „fließen“. Dabei orientieren sie sich an speziellen Gliazellen, die von der Ventrikularschicht Fortsätze bis zum Neuronalrohr gebildet haben. Die durchschnittliche Wanderungsgeschwindigkeit beträgt dabei ca. 0,1 Millimeter pro Tag.[12] Gelegentlich kommt es auch vor, dass Zellen ihren Bestimmungsort verfehlen und in falsche Positionen gelangen. Diese können aber später eliminiert werden. Sobald die Nervenzellen ihre endgültige Position erreicht haben, beginnen sie, Aggregate – Zellansammlungen – und damit die verschiedenen Strukturen des Gehirns zu bilden. Moleküle an der Zelloberfläche ermöglichen es den Zellen dabei wahrscheinlich, sich untereinander zu erkennen und aneinander zu binden. Darüber hinaus nehmen die Neuronen aber auch eine bestimmte Orientierung ein. So ist beispielsweise die Ausrichtung der Pyramidenzellen so, dass ihre apikalen (von ihrer Spitze ausgehenden) Dendriten senkrecht zur Gehirnoberfläche stehen, ihre Axone dagegen in Richtung der weißen Substanz verlaufen. Außerdem findet bei den Nervenzellen in dieser Phase der Differenzierung die Wahl der Erregungsleitung und -übertragung in den Synapsen statt.
Bildung der Verbindungen
Die meisten Nervenzellen in Gehirnen von Säugetieren sind multipolar, das heißt, sie bilden zahlreiche sich verjüngende Dendriten, aber nur ein einzelnes Axon. Die Bildung dieser Strukturen findet statt, wenn die Zelle ihre endgültige Position erreicht hat. Wie es den wachsenden Nervenfasern dabei gelingt, ihren vorbestimmten Weg zu finden, hängt von einer Reihe komplexer Mechanismen ab. Es sind dabei drei Fragestellungen zu unterscheiden:
- Wie finden die Axone ihren Weg? (pathway selection) – Einige Nervenfasern scheinen an einem chemischen Gradienten entlang zu wachsen. Andere wiederum orientieren sich möglicherweise an ihren Nachbarn.[13]
- Wie erkennen sie das Zielgebiet? (target selection) – Das richtige Zielgebiet ist wahrscheinlich genetisch vordefiniert.[13]
- Wie erkennen sie die Zielzelle? (address selection) – Hier spielen vor allem aktivitätsabhängige Prozesse eine große Rolle. Eng damit verwandt sind die molekularen und zellularen Prozesse des Lernens in Organismen.[13]
Ist die Zielzelle erkannt, kommt es zur Ausbildung von Synapsen zwischen den Nervenzellen. Dabei ist der NGF (Nerve Growth Factor) entscheidend; ohne ihn kommt es nicht zur Ausbildung eines funktionierenden Nervensystems.[10] Der Zeitpunkt, wann es zur Synaptogenese (Bildung der Synapsen) kommt, ist dabei von Gehirnregion zu Gehirnregion verschieden. Teilweise dauert sie sogar über die Schwangerschaft hinaus an. Im präfrontalen Kortex etwa hält sie bis zum Jugendalter hin an.[11]
Neuronale Apoptose und Selektion der synaptischen Verschaltungen
Etwa zeitgleich mit dem Prozess der Synaptogenese kommt es zur Apoptose, das ist das kontrollierte Sterben von Zellen. Da im frühen Stadium der Entwicklung des Nervensystems sehr viele Zellen gebildet wurden, kommt es je nach Gehirnregion zur Apoptose von bis zu 85 % der Neuronen. Dies geschieht dadurch, dass alle Nervenzellen um synaptische Kontakte konkurrieren. Neuronen, die nicht in der Lage sind, eine bestimmte Zahl an Verschaltungen auszubilden, sterben in der Folge ab. Damit werden gleich zwei Ziele erreicht: Zum einen den quantitativen Ausgleich von untereinander in Verbindung stehenden Neuronpopulationen und zum anderen die Auflösung von fehlgeschlagenen, inkorrekten Verbindungen.[11] Die Zahl an überlebenden Nervenzellen ist damit abhängig von den benötigten synaptischen Kontakten, die sich aus dem Zielgebiet des Nervenverbandes ergeben. So verbleiben beispielsweise mehr motorische Neuronen im Rückenmark, wenn man dem Embryo eine zusätzliche Extremität einpflanzt. Auslösende Faktoren für die Apoptose können dabei sein:
- apoptogene Membranrezeptoren werden aktiviert, insbesondere durch TNF-α oder zelltod-spezifische Liganden wie FAS,
- kerngebundene Rezeptoren werden aktiviert,
- verschiedene Stressfaktoren wirken ein,
- und wichtigster Auslöser ist das Fehlen von „Überlebenssignalen“ – wachstumsauslösende Moleküle wie NGF, BDNF, CNTF.[14]
Etwas später passt sich dann außerdem die Zahl der Synapsen an. Zum Beispiel werden bei erwachsenen Säugetieren die einzelnen Muskelzellen in den Extremitäten von nur einer einzigen Synapse innerviert. In der Entwicklung kommt es jedoch zu einer Phase der mehrfachen Innervation. Während der zweiten und dritten Woche nach der Geburt verschwinden dann alle überzähligen Synapsen bis auf eine pro Muskelzelle. Auch hier kommt es also zu einer Art Anpassung an die gegebenen Umstände, die aktivitätsabhängig gesteuert ist. Die Aktivität kann entweder von der Zelle selbst (endogene Aktivität) oder von von außen ankommenden Signalen stammen (funktionelle Aktivität). Durchschnittlich degenerieren so etwa 40 % der ursprünglich gebildeten Synapsen wieder.[11]
Entwicklung des Großhirns und der Großhirnrinde
Zur Entwicklung der beiden Gehirnhälften kommt es, indem sie aus der lateralen Wand des Prosencephalus (das am weitesten „mundwärts“ gelegene Primärvesikel des embryonalen Hirns, bestehend aus End- und Zwischenhirn) beidseitig Ausstülpungen bilden, die sich immer weiter vergrößern.[15] Prinzipiell lagern sich die Perikaryen (graue Substanz) bei der Entwicklung des Gehirns um den zentralen Liquorraum an, wohingegen die Axone (weiße Substanz) weiter außen liegen. Allerdings kommt es in den Bereichen der Großhirnhemisphäre und des Kleinhirns auch zur Bildung grauer Substanz an der Oberfläche, sogenannter Rinde. Dies geschieht, indem Neuronen, die ursprünglich in unmittelbarer Nachbarschaft zu den Vesikeln gebildet wurden, an die äußeren Bereiche der Großhirnhemisphäre abwandern. Schließlich bildet sich so eine 6-schichtige und ca. 2 mm dicke Schicht aus 10 bis 14 Milliarden Nerven- und etwa zehnmal so vielen Gliazellen heraus. Ab der 18. Schwangerschaftswoche hat die Großhirnrinde dann ihre typische Form, die durch die Fissuren (Spalten), Sulci (Furchen) und Gyri (Windungen) gekennzeichnet ist.[16] Neuronen im Inneren dagegen bilden die sogenannten Basalganglien.[17]
Entwicklung des Kleinhirns
Auch im Kleinhirn liegt graue Substanz sowohl im Inneren als Kerngebiet als auch oberflächlich als dreigliedrige Rinde vor. Die Histogenese (Entwicklung) des Kleinhirns findet ab der fünften Woche statt und geht dabei von zwei verschiedenen Zonen aus:
- innere Keimschicht der Flügelplatten des Metencephalons: Hier werden jene Zellen gebildet, die von der 6. bis zur 8. Woche auswandern und dabei die Kerngebiete bilden. Weiterhin ab der neunten Woche Neuroblasten für die Purkinje-Zellen, die ebenfalls abwandern, und schlussendlich noch die Sternzellen, Korbzellen und Golgi-Zellen.
- rostraler Teil der Rautenlippen: Er stellt den Bildungsort für die Körnerzellen dar, die ab der 11. Woche zur Kleinhirnoberfläche abwandern und die äußere Körnerschicht bilden. Damit ist die Entwicklung des Kleinhirns aber noch lange nicht abgeschlossen. Die Bildung des neuronalen Netzwerkes der Purkinje-Zellen und die Wanderung der Neuronen der äußeren Körnerschicht dauert noch einige Jahre über die Geburt hinaus an.[18]
Während der gesamten Schwangerschaft ist das neuronale Netzwerk äußerst fragil und daher anfällig für jegliche Umwelteinflüsse, die ihm Schaden könnten. So kann z. B. Alkohol zum fetalen Alkoholsyndrom führen, was mit erheblichen Schäden verbunden sein kann.[19][4][20]
Postnatale Gehirnentwicklung
Auch wenn bei der Geburt bereits alle Nervenzellen vorhanden sind, so ist die Entwicklung des Gehirns noch lange nicht abgeschlossen. Ein funktionsfähiges Netzwerk muss sich erst noch entwickeln; zum Zeitpunkt der Geburt ist erst ein grobes Gerüst angelegt. Daher wachsen Gehirn und Nervennetz bis zum sechsten Lebensjahr äußerst zügig, danach verlangsamt sich die Entwicklung, bis sie letztendlich jenseits des 20. Lebensjahrs abgeschlossen ist.
Myelinisierung
Werden Nervenzellen myelinisiert, so bildet sich um sie herum ein Mantel aus Oligodrendrogliazellen, was zu einer erheblich verbesserten Leitungsfähigkeit führt und damit notwendig ist, um sinnvolle, intakte Verknüpfungen im Gehirn auszubilden. Sie beginnt schon im zweiten Drittel der Schwangerschaft, erreicht innerhalb der ersten acht Lebensmonate aber ihren Höhepunkt. Letztendlich führt das – in Kombination mit der Selektion von Verbindungen – dazu, dass die Geschwindigkeit der Nervenimpulse sich um das 16fache erhöht.[5][11] Bei der Myelinisierung lassen sich folgende Regeln für die Reihenfolge feststellen, in der die Axone ummantelt werden:
- proximale werden vor distalen Verbindungen myelinisiert,
- sensorische Neuronen kommen vor motorischen,
- zuerst spezifische Afferenzen, die vom Thalamus kommen, dann die unspezifischen,
- die zentralen werden vor den polaren Bereichen des Großhirns myelinisiert,
- occipitale werden vor temporalen Polen myelinisiert.
Auch das Größenwachstum des Gehirns ist durch die Ummantelung der Nervenfasern mit der Myelin-Scheide erklärbar – denn die Zahl der Neuronen selbst nimmt nicht zu.[4]
Synaptogenese und Selektion von Synapsen
Auch der Vorgang der Synaptogenese ist bei der Geburt mit gerade einmal durchschnittlich 2.500 Synapsen pro Neuron noch lange nicht abgeschlossen. Bei Kleinkindern liegt diese Zahl schon bei 15.000, das Gehirn eines Zweijährigen enthält schon so viele Synapsen wie das eines Erwachsenen und das eines Dreijährigen sogar doppelt so viele. Bis zum zehnten Lebensjahr werden sie daraufhin wieder abgebaut. Diese enorme Zahl an Verbindungen pro Nervenzelle lässt auf eine sehr hohe Anpassungs- und Lernfähigkeit im Alter von zwei bis zehn Jahren schließen.[5][4] Außerdem findet im Zeitraum nach der Geburt der Großteil an Selektionsprozessen von neuronalen Verbindungen statt. In Zusammenschau mit den obigen Punkten deutet dies darauf hin, dass die Entwicklung des Gehirns maßgeblich von seiner Umwelt mitbestimmt und nur die Grundlage dieser Entwicklung pränatal genetisch determiniert gelegt wird.[6][5] Das erwachsene Gehirn ist dann nur noch begrenzt veränderbar und umbaufähig.[4]
Entwicklung von Denk- und Erinnerungsprozessen
Das Vermögen zur Bildung von Erinnerungen ist schon im Kleinkind angelegt, jedoch ist der Zeitraum, für den eine Erinnerung gespeichert werden kann, anfangs noch recht kurz. Er beträgt bei einem Alter von
- 6 Monaten: 24 Stunden,
- 9 Monaten: 1 Monat
und nimmt im Laufe der Zeit immer weiter zu. Deswegen erinnert man sich im Allgemeinen nicht an Ereignisse aus dem 3. bis 4. Lebensjahr und nur sehr schwach an die aus dem 5. bis 6.[4] Ab etwa vier Jahren wird die Kommunikation zwischen rechter und linker Gehirnhälfte entscheidend verbessert, was zum logischen, analytischen Denken befähigt. Studien mit dem MRT haben außerdem gezeigt, dass der Anteil an grauer Substanz und weißer Substanz im Gehirn sich etwa ab 12 Jahren bis zum Erwachsenenalter zu Gunsten der weißen verschiebt.[21][4]
Entwicklungsstörungen
Abhängig vom Stadium der Gehirnentwicklung kann es bei schädlichen äußeren Einflüssen zu Schädigungen des Gehirns und Störungen in seiner Entwicklung kommen. Genetische, toxische und infektiöse Einflüsse stehen dabei im ersten und zweiten Drittel der Schwangerschaft im Vordergrund, im letzten dagegen hypoxisch-ischämische, infektiöse oder thromboembolische Ereignisse.[11]
Literatur
- Tony Smith: Anatomie-Atlas. DK-Verlag, München 2007, ISBN 978-3-8310-1116-2 Titel der englischsprachigen Originalausgabe: Human Body. DK-Verlag, London 2002.
- Renate Huch, Klaus D. Jürgens (Hrsg.): Mensch – Körper – Krankheit. 6. Auflage. Urban & Fischer Verlag, München 2011, ISBN 978-3-437-26792-5.
- Olav Wieser et al.: Anatomie, Neuer Kaiser Verlag, Klagenfurt, 2006, ISBN 978-3-7043-6057-1 Titel der italienischen Originalausgabe: Atlante de Anatomia, Giunto Gruppo Editorale, Firenze, 2000.
- Ralf Burger et al.: Natura 12 – Biologie für Gymnasien, Ernst Klett Verlag, 1. Auflage, Stuttgart, 2010, ISBN 978-3-12-045570-7.
- Fred T. Adams: Der Weg zum Homo sapiens. Suhrkamp Verlag, Frankfurt am Main 1971; Titel der englischsprachigen Originalausgabe: The Way to Modern Man. Teachers College, Columbia University, New York, 1968.
- W. Maxwell Cowan: Entwicklung des Gehirns, In: Spektrum der Wissenschaft: Verständliche Forschung: Gehirn und Nervensystem. 9. Auflage. Heidelberg 1988, ISBN 3-922508-21-9.
- William H. Calvin: Die Symphonie des Denkens – Wie aus Neuronen Bewusstsein entsteht. Carl Hanser Verlag, Wien 1993, ISBN 3-446-17279-3; Titel der englischsprachigen Originalausgabe: The Cerebral Symphony – Seastore Beflections in the Structure of Consciousness, 1989.
Weblinks
- Grundlagen der Gehirnentwicklung. Auf: embryology.ch, einem Projekt der Universitäten von Fribourg, Lausanne und Bern; abgerufen am 20. Juli 2020
- Alexander Gottschalk: Vorlesung: Entwicklung des Nervensystems. (PDF) Universität Frankfurt, 2010; abgerufen am 20. Juli 2020.
- Entwicklung und Plastizität (PDF) Universität des Saarlandes; abgerufen am 20. Juli 2020
Einzelnachweise
- ↑ Jay N. Giedd: The Amazing Teen Brain. In: Scientific American. Band 312, Nr. 5, 2015, S. 32–37, doi:10.1038/scientificamerican0615-32
Interview mit Jay Giedd, Professor für Psychiatrie, University of California, San Diego.
Rätsel Pubertät. Nebel hinter der Stirn. In: spiegel.de. 4. Mai 2010. - ↑ Die Gehirnwellen bei Erwachsenen und bei Kindern. 25. März 2023, abgerufen am 14. Juni 2025.
- ↑ Robert D. Martin: Hirngröße und menschliche Evolution. In: Spektrum der Wissenschaft. 1. September 1995; abgerufen am 3. Oktober 2016.
- ↑ a b c d e f g Andreas Meyer-Lindenberg, Gregor Hasler: Entwicklung von Gehirn und Nervensystem. Neurologen und Psychiater im Netz; abgerufen am 19. April 2015
- ↑ a b c d Martin R. Textor: Gehirnentwicklung im Kleinkindalter – Konsequenzen für die frühkindliche Bildung. 2002, Überarbeitung und Erweiterung 2010.
- ↑ a b Kipp, Cengiz Yavas, Bettina Burgardt: Die Entwicklung des Gehirns und ihre Risiken. (PDF) Vortrag an der Universität des Saarlandes. In: Seminar zu neuropsychologischen Entwicklungsstörungen, 2006.
- ↑ a b Neuronale Entwicklung. diss.fu-berlin.de; abgerufen am 20. April 2015
- ↑ a b Molekulare Mechanismen während der frühembryonalen Entwicklung des ZNS. ( vom 22. April 2015 im Internet Archive) embryology.ch; abgerufen am
- ↑ Neuronale Grundlagen. entwicklungsdiagnostik.de; abgerufen am 20. April 2015
- ↑ a b A. Gottschalk:Vorlesung: Entwicklung des Nervensystems. ( vom 4. März 2016 im Internet Archive), Universität Frankfurt, 2010; abgerufen am 20. April 2015
- ↑ a b c d e f Matthias Keller, Georg Simbruner: Neurophysiologie der menschlichen Hirnentwicklung: prä-, peri- und postnatale Störungen. In: Liane Kaufmann, Hans-Christoph Nuerk, Kerstin Konrad, Klaus Willmes (Hrsg.): Kognitive Entwicklungsneuropsychologie. Hogrefe, Göttingen u. a. 2007, S. 11–24, ISBN 978-3-8017-1898-5.
- ↑ Nervenzellwanderung. In: Lexikon der Wissenschaft, Spektrum – Verständliche Forschung, Heidelberg 2000.
- ↑ a b c Karl-Friedrich Fischbach, Heinz Gert de Couet und Markus Hofbauer: Neurogenetik. In: Wilhelm Seyffert: Lehrbuch der Genetik. Gustav Fischer Verlag, 1998, ISBN 3-8274-0787-7, 43. Kapitel; abgerufen am 21. April 2015
- ↑ Apoptose. ( vom 4. März 2016 im Internet Archive) embryology.ch; abgerufen am 22. April 2015
- ↑ Eintrag zu Isocortex im Flexikon, einem Wiki der Firma DocCheck, abgerufen am 19. April 2015.
- ↑ Lexikon der Naturwissenschaft: Großhirnrinde, In: Spektrum Akademischer Verlag, Heidelberg, 2000.
- ↑ Grundlagen der Gehirnentwicklung – Histogenese der Großhirnrinde. ( vom 28. April 2016 im Internet Archive) embryology.ch; abgerufen am 20. April 2015
- ↑ Grundlagen der Gehirnentwicklung – Histogenese der Kleinhirnrinde. ( vom 24. September 2015 im Internet Archive) embryology.ch; abgerufen am 20. April 2015
- ↑ JC Bell, C Raynes-Greenow et al. Maternal Alcohol Consumption during Pregnancy and the Risk of Orofacial Clefts in Infants: a Systematic Review and Meta-Analysis. In: Paediatric and Perinatal Epidemiology. 2014 Jul;28(4):322-32. ISSN 1365-3016. doi:10.1111/ppe.12131. PMID 24800624.
- ↑ Chrysanthy Ikonomidou et al.: Ethanol-Induces Apoptotic Neurodegeneration and Fetal Alcohol Syndrom. In: Science vom 11. Februar 2000. doi:10.1126/science.287.5455.1056.
- ↑ Johanna Braig: Neurologische Grundlagen der Entwicklung. In: Rolf Oerter, Leo Montada (Hrsg.): Entwicklungspsychologie. Kapitel 3. Beltz PVU, Weinheim 2008.
Auf dieser Seite verwendete Medien
(c) I, Nrets, CC BY-SA 3.0
Illustration zeigt die Hauptunterteilungen des Vertebratengehirns während der Embryogenese. Das Neuralrohr (nicht illustriert) differenziert zunächst in
linke Bildhälfte: Prosencephalon, Mesencephalon und Rhombencephalon. Dieses sogenannte "Dreibläschenstadium" wird ungefähr in der 4. Woche erreicht!.
rechte Bildhälfte: Im Fünfbläschenstadium unterscheidet man 5 Regionen: Telencephalon, Diencephalon, Mesencephalon, Metencephalon und Myelencephalon.
Der Rest des Neuralrohres differenziert in das Rückenmark.