Flüssige organische Wasserstoffträger
Als flüssige organische Wasserstoffträger (englisch: liquid organic hydrogen carriers, LOHC) werden organische Verbindungen bezeichnet, die Wasserstoff durch chemische Reaktion aufnehmen und wieder abgeben können. LOHCs können daher als Speichermedien für Wasserstoff verwendet werden.
Prinzipiell kann jede ungesättigte Verbindung (organische Moleküle mit C-C Doppel- oder Dreifachbindungen) bei Hydrierung Wasserstoff aufnehmen.
Die für die Wasserstofffreisetzung aus LOHC-Systemen erforderliche hohe Temperatur wurde in der Vergangenheit als Hauptnachteil angesehen, der die Gesamteffizienz des Speicherzyklus einschränkt. 2019 wurde ein alternativer Ansatz zur Umwandlung von LOHC-gebundenem Wasserstoff in Elektrizität vorgeschlagen. Der wasserstoffreiche Träger wird in einer thermoneutralen Transfer-Hydrierungs-Reaktion entladen. Der Wasserstoff wird dabei auf Aceton übertragen. Das Produkt (2-Propanol) der Transferhydrierung wird dann in einer Brennstoffzelle (direkte Isopropanol-Brennstoffzelle; DIPAFC) umgewandelt. Ein solches Konzept ist sehr attraktiv für die On-Board-Erzeugung elektrischer Energie in mobilen Anwendungen.[1]
Prinzip LOHC-basierter Wasserstoffspeicherung
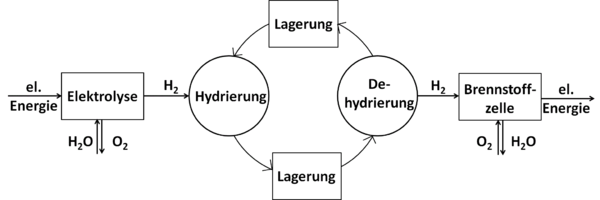
Zur Aufnahme von Wasserstoff reagiert die dehydrierte Form des LOHCs (eine ungesättigte, meist aromatische Verbindung) in einer Hydrierungsreaktion mit dem Wasserstoff. Die Hydrierung ist eine exotherme Reaktion und wird bei erhöhten Drücken (ca. 30–50 bar) und Temperaturen von ca. 150–200 °C in Gegenwart eines Katalysators durchgeführt. Dabei wird die korrespondierende gesättigte Verbindung gebildet, die bei Umgebungsbedingungen gelagert beziehungsweise transportiert werden kann. Wird der Wasserstoff wieder benötigt, wird die nun hydrierte, wasserstoffreiche Form des LOHCs dehydriert, wobei der Wasserstoff wieder aus dem LOHC freigesetzt wird. Diese Reaktion ist endotherm und erfolgt bei erhöhten Temperaturen (250–320 °C) wieder in Gegenwart eines Katalysators. Vor der Nutzung des Wasserstoffs muss dieser gegebenenfalls noch von LOHC-Dampf gereinigt werden. Zur Steigerung der Effizienz sollte die im heißen, aus der Freisetzungseinheit austretenden, Stoffstrom enthaltene Wärme auf den kalten, in die Freisetzungseinheit eintretenden, Stoffstrom aus wasserstoffreichem LOHC übertragen werden, um den Energiebedarf für dessen Vorwärmung vor der Reaktion gering zu halten.
Insbesondere die bei der Wasserstoffaufnahme freiwerdende Wärme der Hydrierungsreaktion lässt sich prinzipiell zu Heizungszwecken oder als Prozesswärme nutzen.[2]
Anforderungen an LOHC-Materialien
Die wichtigsten Anforderungen an einen LOHC sind:
- Flüssiger Aggregatzustand im gesamten relevanten Temperaturbereich
- Temperatur- und Zyklenstabilität
- Umkehrbarkeit der Wasserstoffaufnahme
Daneben ist je nach Einsatzgebiet die Umweltverträglichkeit zu prüfen. In geschlossenen Systemen mit entsprechenden Sicherungsmaßnahmen spielt zum Beispiel die Giftigkeit eine untergeordnete Rolle.
Um eine einfache Handhabung (Pumpbarkeit u. a.) zu gewährleisten, ist der flüssige Aggregatzustand wichtig. Dabei ist zu beachten, dass ein LOHC im Laufe des Prozesses in verschiedenen Formen vorliegt: der dehydrierten (wasserstoffarmen) Form, der hydrierten (wasserstoffreichen) Form und gegebenenfalls noch verschiedenen Zwischenstufen. Die Schmelztemperatur sollte dabei deutlich unter Raumtemperatur für alle Formen liegen. Dies ist beispielsweise ein Problem bei N-Ethylcarbazol, das in der dehydrierten Form einen Schmelzpunkt von ca. 70 °C aufweist. Daneben muss darauf geachtet werden, dass ein Übergang in die Dampfphase möglichst verhindert wird. Ein Siedepunkt unterhalb der Temperatur bei der Dehydrierreaktion, der höchsten Temperatur im Prozess, ist dabei nicht ausreichend, da durch die Anwesenheit des Wasserstoffs der Partialdruck des LOHCs in der Gasphase reduziert wird und daher nennenswerte Verdampfung schon unterhalb der Siedetemperatur möglich ist. LOHC-Materialien sollten daher stets Stoffe mit möglichst niedrigem Dampfdruck sein.
Da ein LOHC recycliert, d. h. immer wieder neu mit Wasserstoff be- und entladen wird, sollte möglichst wenig Zersetzung auftreten. Dabei ist neben den hohen Temperaturen im Prozess auch die Anwesenheit katalytisch-aktiven Materials während der Hydrierung und Dehydrierung zu beachten.
Entscheidend für die Anwendbarkeit als LOHC ist die Umkehrbarkeit der Wasserstoffaufnahme bei technisch sinnvollen Bedingungen. Prinzipiell ist jede ungesättigte Verbindung in der Lage, durch Hydrierung Wasserstoff aufzunehmen. Da die Abgabe thermodynamisch jedoch ungünstig ist, sind lediglich aromatische Verbindungen als LOHCs geeignet.
Bestimmung des Hydriergrads
Bei der Hydrierungs- oder Dehydrierungsreaktion kommt es nicht zwangsläufig zu einem vollständigen Umsatz des dehydrierten bzw. hydrierten LOHCs. Es kann daher eine teilhydrierte Mischung entstehen, die sich aus vollständig hydrierten, teilweise hydrierten und vollständig dehydrierten Molekülen zusammensetzt. Für die praktische Anwendung ist die Kenntnis des jeweiligen Hydriergrads wichtig. Dieser kann als eine Art „Ladezustand“ oder Energieinhalt des LOHCs verstanden werden. Deshalb werden Möglichkeiten zur Bestimmung des Hydriergrads benötigt. Da eine komplexe Laboranalytik (beispielsweise mittels Gaschromatographie oder NMR) in der technischen Praxis nicht in Frage kommt werden Korrelationen mit anderen, leichter zu messenden Größen verwendet. Insbesondere der Brechungsindex und die Dichte eignen sich hierfür.[3]
Beispiele für LOHC-Materialien
Toluol/Methylcyclohexan
Bereits in den 1980er Jahren gab es Versuche mit Toluol, das durch Hydrierung zu Methylcyclohexan umgewandelt wird.[4] Die Grundidee dieser Variante kam 1975 aus den USA und wurde 1979 am Paul-Scherrer-Institut in der Schweiz zusammen mit der ETH Zürich weiterentwickelt. Bereits damals wurde der Prototyp eines LKWs gebaut, der mit Hilfe von Wasserstoff aus der Dehydrierung von Methylcyclohexan angetrieben wurde.[5][6] Der gesamte Kreislauf wird als Methylcyclohexan-Toluol-H2-System (MTH) bezeichnet.[7]
N-Ethylcarbazol

In der aktuellen Forschung wird gegenwärtig unter anderem N-Ethylcarbazol untersucht, das Mitte der 2000er-Jahre von der US-Firma Air Products als Wasserstoffspeicher vorgeschlagen und patentiert wurde.[8] Durch das Vorhandensein des Stickstoffatoms lässt sich Dodecahydro-N-Ethylcarbazol bei deutlich niedrigeren Temperaturen dehydrieren als beispielsweise Methylcyclohexan. Eine relativ effiziente Energiespeicherung wird dadurch ermöglicht. In hydriertem N-Ethylcarbazol können bis zu 5,8 Gew-% Wasserstoff gespeichert werden, was einem formalen Energiegehalt von 1,9 kWh/kg entspricht. Die Dehydrierung erfolgt bei Temperaturen von ca. 200 bis 230 °C.[9] Eine Herausforderung stellt der relativ hohe Schmelzpunkt der dehydrierten Form von ca. 70 °C dar.
Dibenzyltoluol
Um die hohe Schmelztemperatur von N-Ethylcarbazol und den hohen Dampfdruck von Toluol zu umgehen, kann Dibenzyltoluol verwendet werden. Dieser Stoff wird gegenwärtig bereits als Wärmeträgeröl eingesetzt. Zur Dehydrierung sind Temperaturen von ca. 300 °C nötig. Allerdings ist Dibenzyltoluol anderen Trägersubstanzen in vielen physiko-chemischen Eigenschaften überlegen.[10][11]
Benzyltoluol
Benzyltoluol ist chemisch eng mit Dibenzyltoluol verwandt und die chemischen Charakteristika sind daher sehr ähnlich. 2021 gab das Forschungszentrum Jülich bekannt, im Rahmen des Kopernikus-Projekts P2X von nun an Benzyltoluol, anstatt Dibenzyltoluol zu nutzen. Dieses besitzt bei niedrigen Temperaturen eine geringere Viskosität, was die Handhabung in der Praxis erleichtert.[12] Eine entsprechende Brennstoffzelle wird von Schaeffler und dem Helmholtz-Institut Erlangen-Nürnberg für Erneuerbare Energien entwickelt.[13]
Weitere potentielle LOHCs
Naphthalin
Das System Naphthalin/Decalin wird ebenfalls in der Fachliteratur als Trägermaterial diskutiert.[14] Nachteilig ist hierbei allerdings, dass genau wie bei N-Ethylcarbazol, die wasserstoffarme Form bei Raumtemperatur ein Feststoff ist.
Azaborine
Um die für die Wasserstofffreisetzung benötigte Temperatur weiter zu senken, kann in die Ringstruktur zusätzlich zu einem Stickstoffatom, wie bei N-Ethylcarbazol, auch noch ein Bor-Atom eingebaut werden. Solche Azaborine lassen sich prinzipiell bei sehr niedrigen Temperaturen dehydrieren. Allerdings sind hier noch viele Fragen bezüglich Stabilität und Reversibilität ungeklärt.[15]
Energiedichte
1 m3 Dibenzyltoluol kann bis zu 57 kg Wasserstoff speichern, das entspricht ca. 1,9 kWh/l. Da zur Entnahme durch Dehydrierung aber 11 kWh/kg gespeichertem Wasserstoff benötigt werden, sinkt die Nettoenergiedichte um ca. ein Drittel auf 1,3 kWh/l. Das entspricht nur grob einem Zehntel von Diesel.
Im Einsatz kann sich die effektive Energiedichte nochmal dadurch reduzieren, dass bei der Dehydrierung nicht immer zwingend ein vollständiger Umsatz der Reaktion erreicht werden kann oder muss. Weiterhin muss mit Blick auf die volumenbezogene Energiedichte bedacht werden, dass es je mindestens eines Tanks für die hydrierte und die dehydrierte Form bedarf. Daraus folgt prinzipiell nochmals eine Halbierung der Energiedichte. Durch komplexe konstruktive Maßnahmen könnte die Raumnutzung aber verbessert werden. So kann beispielsweise eine Vielzahl kleiner Tanks, von denen immer nur einer leer ist, oder ein Tank mit verschiebbarer Trennwand im Inneren verwendet werden.
Umsetzung
Hydrogenious LOHC Technologies
Am 29. Januar 2016 wurde die weltweit erste kommerzielle LOHC-Anlage zur Speicherung von Wasserstoff in Dibenzyltoluol eingeweiht. Sie wurde durch die Hydrogenious LOHC Technologies GmbH entwickelt und erstellt. Mit Hilfe von Solarstrom aus einer 98 kWp-Photovoltaikanlage wird mittels PEM-Elektrolyse Wasserstoff erzeugt. Dieser wird in Dibenzyltoluol gespeichert.[16] Hydrogenious LOHC Technologies hat für das Speicherverfahren im Jahre 2016 den Innovationspreis der deutschen Wirtschaft gewonnen.
Hydrogenius LOHC Technologies ist eine Ausgründung der Friedrich-Alexander-Universität Erlangen-Nünberg mit Firmensitz in Erlangen-Bruck. Im November 2017 lieferte die Firma die ersten LOHC-Systeme für kommerzielle Anwendungen in die USA und hat sich inzwischen zum Weltmarktführer in der LOHC-Technologie entwickelt. Damit können kommerzielle Wasserstofftankstellen mit über 1.000 kg gespeichertem Wasserstoff vor Ort in dicht besiedelten Gebieten oder an Standorten mit begrenztem Platzbedarf realisiert werden. Das dabei verwendete Trägermaterial Dibenzyltoluol ist schwer entflammbar, aber auch als wassergefährdend und gesundheitsschädlich eingestuft, darf jedoch in unbegrenzter Menge gespeichert und transportiert werden.[17]
Anlage im industriellen Maßstab
Unterstützt vom Land Nordrhein-Westfalen entsteht seit März 2021 im Chempark Dormagen die weltweit größte Anlage für die Einspeicherung von grünem Wasserstoff in LOHC. Die Inbetriebnahme der Anlage im industriellen Maßstab ist für 2023 vorgesehen und sie wird von Hydrogenious LOHC Technologies geliefert. Mit der geplanten Anlagenkapazität können etwa 1.800 Tonnen Wasserstoff im Jahr in das Trägermedium Benzyltoluol eingespeichert werden. Damit steigt die Einspeicherleistung gegenüber den bisherigen Anlagengrößen um etwa das Zwanzigfache. Die Projektleitung und den Anlagenbetrieb übernimmt die LOHC Industrial Solutions NRW GmbH, eine in Krefeld ansässige Tochter von Hydrogenious LOHC Technologies. Covestro Deutschland AG – seit Mitte 2019 Gesellschafter von Hydrogenious LOHC Technologies – stellt die Standortfläche und zukünftig den grünen Wasserstoff zur Verfügung.
Das Forschungszentrum Jülich mit seinem Institut für Energie- und Klimaforschung ist wissenschaftlicher Projektpartner. Laut Peter Wasserscheid, Direktor am Institut für Energie und Klimaforschung des Forschungszentrums Jülich und Direktor des Helmholtz-Instituts Erlangen-Nürnberg für Erneuerbare Energien (HI ERN), der die LOHC-Technologie maßgeblich mitentwickelt hat, konzentriert sich die Begleitforschung auf drei Aspekte: Das Katalysatorverhalten im Realbetrieb, mögliche Einflüsse der LOHC- bzw. Wasserstoffqualität auf den Einspeicherprozess, die Weiterentwicklung industriell nutzbarer Qualitätssicherungsverfahren für das LOHC-System.[18]
Andere deutsche Aktivitäten
Forschung zum Thema LOHC findet aktuell unter anderem an der Friedrich-Alexander-Universität Erlangen-Nürnberg, am Helmholtz-Institut Erlangen-Nürnberg für Erneuerbare Energien und am Energie Campus Nürnberg statt.[19][20]
Neben Hydrogenious LOHC Technologies arbeitet in Deutschland auch das 2010 von Michael Stusch gegründete Münchner Start-up H2-Industries SE an der Weiterentwicklung der LOHC-Speichermethode. Entwicklung und Produktion von H2-Industries sind in Teterow bei Rostock in Mecklenburg-Vorpommern.[21] Eine Anwendung der LOHC-Stromspeichertechnik von H2-Industries ist der emissionsfreie Betrieb von Binnenschiffen.[21]
Einzelnachweise
- ↑ G. Sievi, D. Geburtig, T. Skeledzic, A. Bösmann, P. Preuster, O. Brummel, ... & J. Libuda (2019). Towards an efficient liquid organic hydrogen carrier fuel cell concept. In: Energy & Environmental Science, 12(7), 2305-2314.
- ↑ D. Teichmann, K. Stark, K. Müller, G. Zöttl, P. Wasserscheid, W. Arlt: Energy storage in residential and commercial buildings via Liquid Organic Hydrogen Carriers (LOHC). Energy & Environmental Science, 2012, 5, 5, 9044–9054, doi: 10.1039/C2EE22070A.
- ↑ K. Müller, R. Aslam, A. Fischer, K. Stark, P. Wasserscheid, W. Arlt, "Experimental assessment of the degree of hydrogen loading for the dibenzyl toluene based LOHC system", International Journal of Hydrogen Energy, 2016, 41, 47, 22097–22103, doi: 10.1016/j.ijhydene.2016.09.196.
- ↑ M. Taube, P. Taube, "A liquid organic carrier of hydrogen as a fuel for automobiles", In: Hydrogen energy progress; Proceedings of the Third World Hydrogen Energy Conference, Tokyo, Japan, June 23-26, 1980. Volume 2. (A81-42851 20-44) Oxford and New York, Pergamon Press, 1981, S. 1077–1085.
- ↑ M. Taube, D. Rippin, D.L. Cresswell, W. Knecht, N. Gruenenfelder, "A system of hydrogen-powered vehicles with liquid organic hydrides", International Journal of Hydrogen Energy, 1983, 8, 3, 213-225, doi: 10.1016/0360-3199(83)90067-8.
- ↑ M. Taube, D. Rippin, W. Knecht, D. Hakimifard, B. Milisavljevic, N. Gruenenfelder, "A prototype truck powered by hydrogen from organic liquid hydrides", International Journal of Hydrogen Energy, 1985, 10, 9, 595-599, doi: 10.1016/0360-3199(85)90035-7.
- ↑ Übersichtsbeitrag Energiespeicherung als Element einer sicheren Energieversorgung. In: Chemie Ingenieur Technik. 87, 2015, S. 17, doi:10.1002/cite.201400183, dort S. 49. - Joint GCC-JAPAN Environment Symposia in 2013.
- ↑ G.P. Pez, A.R. Scott, A.C. Cooper, H. Cheng, F.C. Wilhelm, A.H. Abdourazak, "Hydrogen Storage by Reversible Hydrogenation of pi-conjugated substrates", Patent US 7351395, angemeldet am 4. November 2005, erteilt am 1. April 2008.
- ↑ B. Müller, K. Müller, D. Teichmann, W. Arlt, "Energiespeicherung mittels Methan und energietragenden Stoffen – ein thermodynamischer Vergleich", Chemie Ingenieur Technik, 2011, 83, No. 11, 1–13, doi: 10.1002/cite.201100113.
- ↑ N. Brückner, K. Obesser, A. Bösmann, D. Teichmann, W. Arlt, J. Dungs, P. Wasserscheid, Evaluation of Industrially Applied Heat-Transfer Fluids as Liquid Organic Hydrogen Carrier Systems, In: ChemSusChem, 2014, 7, 229–235, doi: 10.1002/cssc.201300426.
- ↑ C. Krieger, K. Müller, W. Arlt: Energetische Analyse von LOHC-Systemen als thermochemische Wärmespeicher. In: Chemie Ingenieur Technik. 86, 2014, S. 1441, doi:10.1002/cite.201450058.
- ↑ Kopernikus-Projekte: P2X: Wechsel des LOHC. Abgerufen am 24. Januar 2022.
- ↑ Energiewende: Schaeffler entwickelt LOHC-Brennstoffzelle - Golem.de. In: golem.de. 2. Februar 2022, abgerufen am 3. Februar 2022.
- ↑ S. Hodoshima, S.Takaiwa, A. Shono, K. Satoh, Y. Saito, "Hydrogen storage by decalin/naphthalene pair and hydrogen supply to fuel cells by use of superheated liquid-film-type catalysis", Applied Catalysis A: General, 2005, 283, 1-2, 235–242, doi: 10.1016/j.apcata.2005.01.010.
- ↑ K. Müller, K. Stark, B. Müller, W. Arlt, "Amine borane based hydrogen carriers: An evaluation", Energy & Fuels, 2012, 26, 6, 3691–3696, doi: 10.1021/ef300516m.
- ↑ Von der Forschung zum Produkt – Produktvorstellung der Hydrogenious Technologies GmbH, 1. Februar 2016
- ↑ https://emcel.com/de/lohc-wasserstoffspeicher
- ↑ https://www.hydrogenious.net/index.php/de/2021/03/03/kick-off-fuer-bau-und-betrieb-der-weltweit-groessten-anlage-zur-einspeicherung-von-gruenem-wasserstoff-in-liquid-organic-hydrogen-carrier-in-dormagen
- ↑ Wasserstoffspeicher. Energie Campus Nürnberg, abgerufen am 25. April 2019.
- ↑ Aus dem Labor auf die Schiene - Forscher des HI-ERN planen Wasserstoffzüge mit LOHC-Technologie. In: Pressemitteilung. Forschungszentrum Jülich, 19. April 2018, abgerufen am 25. April 2019.
- ↑ a b Martin Jendrischik: H2-Industries und PortLiner bauen Binnenschiffe mit LOHC-Speicher. In: cleantech.de. 2. Mai 2020, abgerufen am 23. September 2020.
Auf dieser Seite verwendete Medien
Reaktionsgleichung N-Carbazol / Perhydro-N-Carbazol
Autor/Urheber: K. Müller, Lizenz: CC BY-SA 3.0
Schema einer Energiespeicherung mittels chemischer Speicherung von Wasserstoff auf einem organischen Wasserstoffträger (LOHC)

