Dihydrofolatreduktase
| Dihydrofolat-Reduktase | ||
|---|---|---|
 | ||
Vorhandene Strukturdaten: s. UniProt | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 186 Aminosäuren | |
| Bezeichner | ||
| Gen-Name | DHFR | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 1.5.1.3, Oxidoreduktase | |
| Reaktionsart | Reduktion | |
| Substrat | 7,8-Dihydrofolat + NADPH + H+ | |
| Produkte | 5,6,7,8-Tetrahydrofolat + NADP+ | |
| Vorkommen | ||
| Homologie-Familie | DHFR | |
| Übergeordnetes Taxon | Lebewesen | |
Dihydrofolatreduktase (DHFR), auch Dihydrofolsäure-Reduktase, heißen Enzyme, die Folsäure zu Dihydrofolsäure (DHF) und DHF zu Tetrahydrofolsäure (THF) hydrieren. Diese Reaktionen aktivieren das Vitamin Folsäure und sind unentbehrlich für die Nukleotid-Biosynthese in allen Lebewesen. Beim Menschen kommt DHFR in allen Gewebetypen vor. Mutationen am DHFR-Gen können Dihydrofolat-Reduktase-Mangel, und dieser eine megaloblastäre Anämie verursachen.[1]
Die DHFR in Protozoen und manchen Pflanzen ist ein Doppelenzym, das zusätzlich die Funktion der Thymidylatsynthase hat; aufgrund dieser strukturellen Eigenheit ist die protozoische DHFR Target bei der Entwicklung von Antibiotika, z. B. gegen den Malariaerreger Plasmodium falciparum oder Kryptosporidien.[2][3][4]
Katalysierte Reaktionen
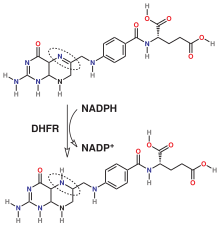
7,8-Dihydrofolsäure wird mit NADPH als Elektronendonor zu Tetrahydrofolsäure reduziert (s. Abb.). Außerdem kann Folsäure zu DHF reduziert werden; diese Reaktion läuft jedoch langsamer ab.[5][6]
Weitere Funktionen
Die Anwesenheit von DHFR in Endothelzellen ist ausschlaggebend für die Funktion von Tetrahydrobiopterin in der NO-Synthase.[7]
Regulation und Hemmung
DHFR ist ein ausgiebig untersuchtes Enzym, das als Target für die Chemotherapie und bei anderen Krankheiten gilt. Das Enzym kann durch Folsäure-Antagonisten wie Methotrexat, Aminopterin oder Trimethoprim kompetitiv gehemmt werden. Die Hemmung bewirkt einen Mangel an Tetrahydrofolsäure, wodurch die Thymin-Synthese (Thymidylat-Synthase benötigt THF) sowie die Purinsynthese (Aufbau des Puringrundkörpers) verhindert wird, woraufhin die Zelle abstirbt.[8]
Siehe auch
Weblinks
- reactome.org: Folate is reduced to dihydrofolate (DHF)
- reactome.org: DHF is reduced to tetrahydrofolate (THF)
- Proteopedia: Dihydrofolate reductase (engl.)
Einzelnachweise
- ↑ UniProt P00374
- ↑ Prosite-Eintrag
- ↑ Ochong E, Bell DJ, Johnson DJ, et al: Plasmodium falciparum strains harboring dihydrofolate reductase with the I164L mutation are absent in Malawi and Zambia even under antifolate drug pressure. In: Antimicrob. Agents Chemother. 52. Jahrgang, Nr. 11, November 2008, S. 3883–3888, doi:10.1128/AAC.00431-08, PMID 18725445.
- ↑ Bolstad DB, Bolstad ES, Frey KM, Wright DL, Anderson AC: Structure-based approach to the development of potent and selective inhibitors of dihydrofolate reductase from cryptosporidium. In: J. Med. Chem. 51. Jahrgang, Nr. 21, November 2008, S. 6839–52, doi:10.1021/jm8009124, PMID 18834108.
- ↑ EC 1.5.1.3
- ↑ Steven W Bailey, June E Ayling: The extremely slow and variable activity of dihydrofolate reductase in human liver and its implications for high folic acid intake. In: Proceedings of the National Academy of Sciences. 106. Jahrgang, Nr. 36, 2009, S. 15424–15429 (pnas.org).
- ↑ Chalupsky K, Cai H: Endothelial dihydrofolate reductase: critical for nitric oxide bioavailability and role in angiotensin II uncoupling of endothelial nitric oxide synthase. In: Proc. Natl. Acad. Sci. U.S.A. 102. Jahrgang, Nr. 25, Juni 2005, S. 9056–61, doi:10.1073/pnas.0409594102, PMID 15941833, PMC 1157015 (freier Volltext).
- ↑ Abali EE, Skacel NE, Celikkaya H, Hsieh YC: Regulation of human dihydrofolate reductase activity and expression. In: Vitam. Horm. 79. Jahrgang, 2008, S. 267–292, doi:10.1016/S0083-6729(08)00409-3, PMID 18804698.
Auf dieser Seite verwendete Medien
Ribbon diagram of human dihydrofolate reductase in complex with folate (blue).
Created using Accelrys DS Visualizer Pro 1.6 and the GIMP.
Schematic of the reaction catalyzed by dihydrofolate reductase (DHFR)

