Coomassie-Brillant-Blau
Coomassie-Brillantblau, häufig nur als Coomassie bezeichnet, sind Triphenylmethanfarbstoffe aus der Gruppe der Säurefarbstoffe, die in der Biochemie zum Anfärben von Proteinen verwendet werden.[1] Sie lagern sich an die basischen Seitenketten der Aminosäuren an und führen zu einer sequenzunspezifischen Proteinfärbung. Ursprünglich wurden diese Farbstoffe in der Textilindustrie genutzt.
| Coomassie-Brillantblau | ||||
| Name | Coomassie-Brillantblau R-250 | Coomassie-Brillantblau G-250 | ||
| Andere Namen | C.I. Acid Blue 83 Brillantblau R C.I. 42660 Xylenbrillantcyanin | C.I. Acid Blue 90 Brillantblau G C.I. 42655 | ||
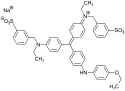
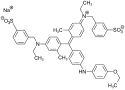
| Strukturformel |  |  | ||
| CAS-Nummer | 6104-59-2 | 6104-58-1 | ||
| PubChem | 61365 | 6324599 | ||
| Summenformel | C45H44N3NaO7S2 | C47H48N3NaO7S2 | ||
| Molare Masse | 825,97 g·mol−1 | 854,02 g·mol−1 | ||
| Aggregatzustand | fest | |||
| GHS- Kennzeichnung [2][3] |
|
| ||
| H- und P-Sätze | keine H-Sätze | keine H-Sätze | ||
| keine EUH-Sätze | keine EUH-Sätze | |||
| keine P-Sätze | keine P-Sätze | |||
Anwendungen

Typischerweise wird C.I. Acid Blue 83 (Coomassie-Brillantblau R-250) z. B. zum Einfärben von aufgetrennten Proteinen in einem Polyacrylamid-Gel benutzt. Es wird außerdem in der 2D-Gelelektrophorese zur Sichtbarmachung der getrennten Proteinpunkte verwendet.
C.I. Acid Blue 90 (Coomassie-Brillantblau G-250) dient auch der Quantifizierung des Proteingehaltes wässriger Lösungen nach der Methode von Bradford.
Neben Methylenblau wurde und wird Coomassie-Brillantblau auch zum dauerhaften Einfärben von nicht zum menschlichen Verzehr geeignetem Fleisch und Schlachtabfällen verwendet.
Die Nachweisgrenze für C.I. Acid Blue 83 liegt bei ungefähr 0,1 µg Protein pro Bande in einem Gel, für C.I. Acid Blue 90 bei etwa 0,5 µg. Mit C.I. Acid Blue 90 lassen sich Proteine jedoch deutlich schneller anfärben. Besondere Formulationen als kolloidale Lösungen verbessern die Nachweisgrenze von C.I. Acid Blue 90 auf ca. 5 ng Protein pro Bande.[4]
C.I. Acid Blue 90 wird auch bei Augenoperationen eingesetzt. Aufgrund der reduzierten Toxizität im Vergleich zu bisher verwendeten Farbstoffen (Indocyaningrün oder Trypanblau) werden Triphenylmethanfarbstoffe wie C.I. Acid Blue 90, Patentblau V oder C.I. Acid Violet 17 für das Anfärben von natürlich vorhandenen oder krankhaft veränderten Strukturen (Gliose) im Auge eingesetzt. Mit Hilfe dieser Farbstoffe lassen sich vor allem die transparenten Strukturen der Netzhaut, Hornhaut oder der Linsenkapsel gezielt anfärben und bei Bedarf chirurgisch entfernen. Für die Technik des Anfärbens von Gewebe an der Netzhaut hat sich der Fachbegriff der Chromovitrektomie etabliert.[5][6][7][8][9]
Name
Der Name des ursprünglich als Wollfarbstoff entwickelten Coomassie-Brillant-Blau stammt von der afrikanischen Stadt Kumasi in Ghana. Er wurde zur Erinnerung an die britische Besetzung der damaligen Aschanti-Hauptstadt Coomassie – heute Kumasi – im Jahr 1896 gewählt. Coomassie war ursprünglich eine registrierte Marke der Imperial Chemical Industries.
Der Zusatz „R“ im Namen Coomassie Brillant Blau R-250 ist eine Abkürzung der englischen bezeichnung „reddish“, zu deutsch etwa „rötlich“. Der Zusatz „G“ im Namen Coomassie Brillant Blau G-250 steht als Abkürzung für „greenish“, zu deutsch also für grünlich. Die Zahl 250 im Namen bezieht sich auf die Farbstärke, mit der der ursprüngliche Hersteller, Imperial Chemical Industries, das Färbevermögen quantitativ beschrieb.
Siehe auch
- Acid Violet 17
Weblinks
Einzelnachweise
- ↑ Eintrag zu Coomassie® Brilliant Blue. In: Römpp Online. Georg Thieme Verlag, abgerufen am 11. Juli 2019.
- ↑ Datenblatt Coomassie-Brillant-Blau bei Merck, abgerufen am 25. Mai 2021.
- ↑ Datenblatt Coomassie-Brillant-Blau bei Merck, abgerufen am 25. Mai 2021.
- ↑ D. Kang et al. (2002): Highly Sensitive and Fast Protein Detection with Coomassie Brilliant Blue in Sodium Dodecyl Sulfate-Polyacrylamide Gel Electrophoresis. In: Bull. Korean Chem. Soc. Bd. 23, Nr. 11, S. 1511–1512. doi:10.5012/bkcs.2002.23.11.1511.
- ↑ S. Balaiya, V. S. Brar, R. K. Murthy, K. V. Chalam: Comparative in vitro safety analysis of dyes for chromovitrectomy: indocyanine green, brilliant blue green, bromophenol blue, and infracyanine green. In: Retina 31(6):1128-36 (2011). PMID 21394068.
- ↑ E. B. Rodrigues, M. Maia, C. H. Meyer, E. M. Penha, E. Dib, M. E. Farah: Vital dyes for chromovitrectomy. In: Curr Opin Ophthalmol. 18(3):179-87 (2007). PMID 17435423.
- ↑ A. Iriyama, K. Kadonosono, Y. Tamaki, Y. Yanagi: Effect of Brilliant Blue G on the retinal ganglion cells of rats. In: Retina 32(3):613-6 (2012). PMID 22392093.
- ↑ Y. S. Chang, S. Y. Tseng, S. H. Tseng, Y. T. Chen, J. H. Hsiao: Comparison of dyes for cataract surgery. Part 1: cytotoxicity to corneal endothelial cells in a rabbit model. In: Journal of Cataract and Refractive Surgery. 31(4):792-8 (2005). PMID 15899458.
- ↑ S. Thaler, J. Hofmann, K. U. Bartz-Schmidt, F. Schuettauf, C. Haritoglou, E. Yoeruek: Methyl blue and aniline blue versus patent blue and trypan blue as vital dyes in cataract surgery: capsule staining properties and cytotoxicity to human cultured corneal endothelial cells. In: Journal of Cataract and Refractive Surgery. 37(6):1147-53 (2011). PMID 21596258.
Auf dieser Seite verwendete Medien
Autor/Urheber: Dasha, Lizenz: CC BY 2.0
Solution of Coomassie, which turns blue if protein is present. The chuky stuff is DNA. Taken with the superzoom feature.
chemical structure of C.I. Acid Blue 83, Na-salt
Autor/Urheber: Yikrazuul, Lizenz: CC BY-SA 3.0
Coomassie gefärbtes Gel. Für Einzelheiten siehe eins drüber und viel Spaß.
chemical structure of C.I. Acid Blue 90, Na-salt