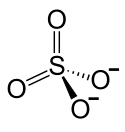
Cobalt(II)-sulfat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
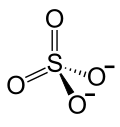 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Cobalt(II)-sulfat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel |
| |||||||||||||||
| Kurzbeschreibung | karminrote Kristalle (Heptahydrat)[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | ||||||||||||||||
| Aggregatzustand | fest[1] | |||||||||||||||
| Dichte | ||||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | gut in Wasser (383 g·l−1 bei 25 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Zulassungsverfahren unter REACH | besonders besorgniserregend: krebserzeugend, fortpflanzungsgefährdend (CMR)[4] | |||||||||||||||
| MAK | aufgehoben, da karzinogen[1] | |||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Das Cobalt(II)-sulfat ist im wasserfreien Zustand ein violettstichig-rotes („pink“), hygroskopisches Salz der Schwefelsäure. Das giftige, krebserzeugende Pulver nimmt an feuchter Luft Hydratwasser auf und bildet das karminrote Cobalt(II)-sulfat-Heptahydrat. Abhängig von der Temperatur treten auch das Hexahydrat und das Monohydrat auf.
Vorkommen
Cobalt(II)-sulfat tritt selten in Form von einigen Kristallhydrat-Mineralien (Co[SO4]·xH2O) entlang der Oxidationszonen von primären Cobaltmineralien (wie Skutterudit oder Cobaltit) auf. Dies sind: Bieberit (Heptahydrat), Moorhouseit (Hexahydrat), Aplowit (Tetrahydrat) und Cobaltkieserit (Monohydrat).
Das Recycling aus Lithium-Ionen-Akkumulatoren wird erforscht.[7] Dies gewinnt deshalb an Bedeutung, da derartige Akkus in der Elektromobilität eine zunehmende Rolle spielen und Cobalt als Rohstoff darin eine herausragende Rolle spielt.
Gewinnung und Darstellung
Cobalt(II)-sulfat entsteht bei Einwirkung von Schwefelsäure auf elementares Cobalt oder auf Cobaltoxide wie Cobalt(II)-oxid.
Eigenschaften

Wasserfreies Cobalt(II)-sulfat ist polymorph und kristallisiert als orthorhombische A-Form oder monokline B-Form.[8] Das Hepta- und Monohydrat bilden monokline Kristallstrukturen.[2] Das Heptahydrat spaltet bei 41,5 °C Kristallwasser ab und bildet das ebenfalls rote Hexahydrat. Dieses wiederum setzt sich durch Abspaltung von Kristallwasser bei 71 °C zum pinkfarbenen Monohydrat um.
Verwendung
Cobalt(II)-sulfat wird zur Herstellung von Pigmenten, Glasuren, in der Porzellanmalerei, zur Tonung von Papieren (Fotografie), in Bädern für Cobalt-Electroplating und zur Spurenelementsupplementierung in der Aquaristik und anderem verwendet.
Zudem wurde das Salz in den 1960er-Jahren Bier beigemischt, um die Stabilität des Schaumes zu erhöhen.[9] Als Folge kam es in Kanada und den USA zu einer Reihe von Fällen einer Cobalt-induzierten Kardiomyopathie (Cobalt-Kardiomyopathie). In Quebec wurden 49, in Omaha 64 Patienten registriert. Die Symptome umfassten unter anderem Magenschmerzen, Gewichtsverlust, Übelkeit, Atemnot und Husten. Die Letalitätsrate betrug etwa 40 Prozent. Autopsien ergaben schwere Schädigungen an Herzmuskel und Leber. Alle Patienten waren starke Biertrinker (1,5 bis 3 Liter pro Tag). Sie konsumierten bevorzugt Sorten von lokalen Brauereien, die etwa einen Monat zuvor angefangen hatten dem Bier Cobalt(II)-sulfat als Schaumstabilisator beizumischen.[9] Die Grenzwerte für Cobalt in Lebensmitteln waren nicht überschritten worden. Das Auftreten der Krankheitsfälle kam unmittelbar zum Stillstand, nachdem die Brauereien die Cobalt(II)-sulfat-Beimischungen einstellten.[10][11]
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu Cobalt(II)-sulfat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ a b SLAC:PHYSICAL CONSTANTS OF INORGANIC COMPOUNDS ( vom 5. Dezember 2020 im Internet Archive) (PDF; 391 kB)
- ↑ Eintrag zu Cobalt sulphate in der Datenbank ECHA CHEM der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 6. Dezember 2019.
- ↑ Datenblatt Cobalt(II)-sulfat bei Merck, abgerufen am 19. Januar 2011.
- ↑ G.J.A. Speijers, E.I. Krajnc, J.M. Berkvens, M.J. van Logten: Acute oral toxicity of inorganic cobalt compounds in rats. In: Food and Chemical Toxicology. Band 20, Nr. 3, Juni 1982, S. 311–314, doi:10.1016/S0278-6915(82)80298-6.
- ↑ Jingu Kang, Gamini Senanayake, Jeongsoo Sohn, Shun Myung Shin: Recovery of cobalt sulfate from spent lithium ion batteries by reductive leaching and solvent extraction with Cyanex 272. In: Hydrometallurgy. Band 100, Nummer 3–4, 2010, S. 168–171. DOI:10.1016/j.hydromet.2009.10.010.
- ↑ J. D. Dunitz, P. Pauling: Polymorphism in Anhydrous Cobalt Sulphate. In: Acta Crystallographica. Band 18, Nr. 4, 1965, S. 737–740, doi:10.1107/S0365110X65001688.
- ↑ a b Carlos Thomas: Spezielle Pathologie. Schattauer Verlag, 1996, ISBN 3-7945-2110-2, S. 179 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Expert Group on Vitamins and Minerals. 2002.
- ↑ Cardiology: When Beer Brought the Blues. In: New York Times Ausgabe vom 10. Januar 1967.
Auf dieser Seite verwendete Medien
Globales Harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS) Piktogramm für gesundheitsgefährdende Stoffe.
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances
Struktur des Co2+-Ions