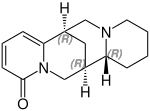Chinolizidin-Alkaloide
Chinolizidin-Alkaloide sind Naturstoffe, die eine Chinolizidin-Grundstruktur aufweisen, dazu gehören auch die Lupinen-Alkaloide.[1][2]
Vorkommen
Chinolizidin-Alkaloide kommen in der Pflanzenfamilie der Hülsenfrüchtler, insbesondere in den Schmetterlingsblütlern, vor. Während die Lupinen-Alkaloide ihrem Namen entsprechend in Lupinen vorkommen, wurde Tinctorin aus dem Färber-Ginster isoliert.[3][1]
Vertreter
Es sind mehr als 200 Chinolizidin-Alkaloide bekannt. Die Alkaloide lassen sich in 6 Strukturtypen einordnen:[2]
- dem Lupinin-Typ mit 34 bekannten Strukturen, u. a. Lupinin und seine Derivate
- dem Camoensin-Typ mit 6 bekannten Strukturen, u. a. Camoensidin
- dem Spartein-Typ mit 66 Strukturen, u. a. Spartein, Lupanin, Angustifolin
- dem α-Pyridon-Typ mit 25 Strukturen, u. a. Anagyrin und Cytisin
- dem Matrin-Typ mit 31 Strukturen, u. a. Matrin
- und dem Ormosanin-Typ mit 19 Strukturen, u. a. Ormosanin
Eigenschaften
Cytisin ist das toxische Hauptalkaloid des Goldregens. Es wirkt ähnlich wie Nicotin in geringer Dosis anregend bis halluzinogen, in höheren Dosen atemlähmend. Cytisin und Matrin sind Wirkstoffe der Sophora Bohnen in Mexico sowie der Kuh Seng und Shinkyogan-Drogen in China und Japan.[1]
Die Chinolizidin-Alkaloide dienen chemischen Abwehr der Pflanzen. Sie zeigen vielfältige Wirkungen auf Warmblüter und führen zu Vergiftungen von Weidevieh (Schafe und Rinder). Dafür verantwortlich sind insbesondere Cytisin und Anagyrin. Auswirkungen einer Vergiftung sind Erregung, Koordinationsstörungen, Atemnot, Krämpfe und schließlich Tod durch Atemlähmung. Anagyrin wirkt teratogen. Das einzige therapeutisch genutzte Chinolizidin-Alkaloid ist Spartein[2], welches antiarrhythmisch und wehenfördernd wirkt.[1]
Einzelnachweise
- ↑ a b c d Eberhard Breitmaier: Alkaloide. Springer Fachmedien, Wiesbaden 1997, ISBN 978-3-519-03542-8, S. 45 ff.
- ↑ a b c Eintrag zu Chinolizidin-Alkaloide. In: Römpp Online. Georg Thieme Verlag, abgerufen am 28. April 2020.
- ↑ D. Knöfel, H. Schütte: Chinolizidinalkaloide: Konstitution und Konfiguration von Tinctorin aus Genista tinctoria. In: Journal fur praktische Chemie. Band 312, Nr. 5, 1970, S. 887–888, doi:10.1002/prac.19703120521.
Weblinks
Auf dieser Seite verwendete Medien
Quinolizidine structural formula
Struktur des (6R,7S,9S,11S)-(-)-Sparteins
Strukturformel des (-)-Anagyrins
Strukturformel des (-)-Lupinins
Autor/Urheber: WH23, Lizenz: CC BY-SA 4.0
Strukturformel des (+)-Matrins
Struktur des (6S,7R,9R,11R)-(-)-Lupanins