Cephalosporine

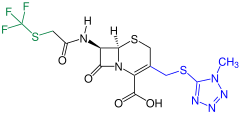
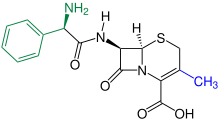
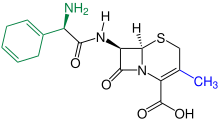
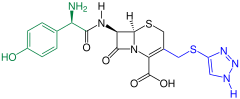
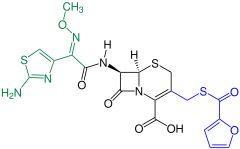
Cephalosporine (von kephale κέφαλη für „Kopf“ und sporos σπόρος für „Spore“) bilden eine Gruppe von Breitband-Antibiotika und gehören wie Penicillin zu den β-Lactam-Antibiotika. Sie wirken auf sich teilende Bakterien bakterizid, indem sie beim Neuaufbau der Zellwände die innere Quervernetzung der Mureinschicht verhindern.
Natürlicherweise kommen Cephalosporine im Schimmelpilz Acremonium chrysogenum (ehemals Cephalosporium acremonium) als Cephalosporin-C vor. Cephalosporin-C wurde 1945 erstmals von Giuseppe Brotzu an der Universität Cagliari entdeckt[1] und von Edward Abraham und Kollegen in Oxford näher untersucht. Die chemische Struktur, die Ähnlichkeiten mit der Struktur von Penicillin G aufweist, wurde 1953 aufgeklärt. Es ist wegen seiner schwachen pharmakologischen Wirkung ohne Bedeutung, dient bis heute aber als Grundsubstanz zur Herstellung von wirksameren halbsynthetischen Cephalosporinen. Die Biofermentation findet heute hauptsächlich in der Provinz Hubei in China statt.[2]
Einteilung und Wirkspektrum
Es existiert keine international verbindliche Einteilung der Cephalosporine. Eine Einteilung kann entsprechend dem Wirkspektrum nach Generationen oder Gruppen erfolgen sowie nach der Art der Aufnahme (parenteral oder peroral).[3]
Alle derzeit auf dem Markt erhältlichen Cephalosporine sind nicht wirksam gegen Enterokokken, da diese eine Primärresistenz aufweisen (die sogenannte „Enterokokkenlücke“).[4]
Einteilung nach Gruppen
Häufig erfolgt die Einteilung nach Generationen. Da die „Ablösung“ von älteren Cephalosporinen durch neuere Stoffe nicht in allen Fällen erfolgt ist, wird an dieser Stelle der Begriff Gruppe zur Einteilung benutzt. „Klassische“ oder Cephalosporine der ersten Gruppe zeichnen sich durch eine gute Wirksamkeit gegen Staphylokokken, auch gegen β-Lactamase-Bildner (siehe unten), aus. Ihre Wirksamkeit gegen gramnegative Erreger ist eingeschränkt. Neben den Cephalosporinen der ersten Generation gibt es eine Reihe von Abwandlungen, die als Cephalosporine der zweiten und dritten Gruppe bezeichnet werden. Der Vorteil der zweiten Gruppe ist eine bessere Resistenz gegen β-Lactamase, ein Enzym, mit dem sich einige Bakterien, insbesondere gramnegative Stäbchenbakterien, gegen β-Lactam-Antibiotika (siehe oben) schützen können. Die dritte Gruppe hat ein breiteres Wirkungsspektrum, erfasst also weitere Bakterien. Mindestens 18 Substanzen waren in den 1990er Jahren auf dem deutschen Markt zugelassen; nach einer Konsolidierungsphase enthält die Rote Liste jetzt noch neun Cephalosporine mit guter Verträglichkeit und Wirksamkeit. Cephalosporine der vierten Gruppe zeigen zudem eine Wirksamkeit gegen Pseudomonas aeruginosa. Im Gegensatz zu den anderen Cephalosporinen sind die der fünften Gruppe auch gegen MRSA wirksam.[3]
Parenterale und perorale Therapie
Cephalosporine können außerdem darin unterteilt werden, ob sie parenteral verabreicht werden oder zur peroralen Therapie geeignet sind. Zudem gibt es Cephalosporine, die lediglich für die Veterinärmedizin zugelassen sind (z. B. Cefalonium[5]).
Cephalosporine der 1. Gruppe (oder klassische Cephalosporine)
Diese Basiscephalosporine haben im Vergleich zu anderen die höchste Aktivität gegen Staphylokokken. Sie zeigen eine schwache Aktivität gegen gramnegative Bakterien und sind instabil gegenüber vielen β-Lactamasen von gramnegativen Bakterien.[3]
- Parenterale Therapie: Cefazolin, Cefacetril, Cefapirin, Ceftezol, Cefazaflur, Cefalotin, Cefaloridin
- Perorale Therapie: Cefadroxil, Cefalexin, Cefradin, Cefaloglycin (nicht mehr im Handel), Cefatrizin, Cefazedon, Cefroxadin
- Ausschließlich in der Veterinärmedizin: Cefalonium
- Cefazolin
- Cefacetril
- Cefapirin
- Ceftezol
- Cefazaflur
- Cefalotin
- Cefaloridin
- Cefadroxil
- Cefalexin
- Cefradin
- Cefaloglycin
- Cefatrizin
- Cefazedon
- Cefroxadin
- Cefalonium
Cephalosporine der 2. Gruppe
Diese Übergangscephalosporine sind im Vergleich zur Gruppe 1 ausreichend, aber schwächer wirksam gegen grampositive Bakterien. Sie zeigen aber eine verbesserte Wirkung im gramnegativen Bereich. Sie sind stabil gegenüber Penicillinasen aus Staphylokokken und begrenzt stabil gegenüber β-Lactamasen gramnegativer Bakterien.[3]
- Parenterale Therapie: Cefuroxim-Natrium, Cefotiam (nicht mehr im Handel)
- Perorale Therapie: Cefuroxim (als Cefuroximaxetil), Cefaclor, Loracarbef (nicht mehr im Handel)
- Cefuroxim
- Cefotiam
- Cefaclor
- Loracarbef
Cephalosporine der 3. Gruppe
Diese Breitspektrumcephalosporine sind schwächer wirksam gegen Staphylokokken, aber deutlich besser wirksam gegen gramnegative Bakterien als die Gruppen 1 und 2. Sie sind stabil gegenüber zahlreichen β-Lactamasen gramnegativer Bakterien.[3]
- Parenterale Therapie: Cefotaxim, Ceftriaxon, Ceftazidim, Ceftazidim kann auch inhalativ verwendet werden.[6] Ceftazidim ist zudem das einzige Cephalosporin dieser Generation, welches auch gegen Pseudomonaden wirksam ist.
- Perorale Therapie: Cefixim, Cefpodoxim (als Cefpodoximproxetil), Ceftibuten[7]
- Ausschließlich in der Veterinärmedizin: Cefovecin, Ceftiofur
- Cefotaxim
- Ceftriaxon
- Ceftazidim
- Cefixim
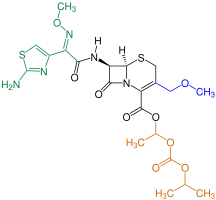
- Cefpodoximproxetil
- Ceftibuten
- Cefovecin
- Ceftiofur
Cephalosporine der 4. Gruppe
Diese Cephalosporine werden auch als Breitspektrumcephalosporine bezeichnet. Ceftolozan zeigt eine hohe Aktivität gegen Pseudomonas aeruginosa und erfasst durch Kombination mit Tazobactam auch ESBL-bildende Erreger.[3]
- Parenterale Therapie: Cefepim, Ceftolozan (mit Tazobactam)
- Cefepim
- Ceftolozan
Cephalosporine der 5. Gruppe
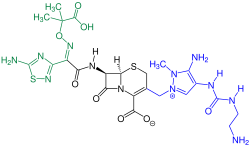
Auch diese Cephalosporine werden als Breitspektrumcephalosporine bezeichnet. Ceftarolinfosamil ist nicht gegen Pseudomonas aeruginosa wirksam. Beide zeigen eine Wirksamkeit gegen MRSA und andere grampositive sowie gramnegative Erreger.[3][8][9]
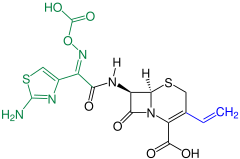
- Parenterale Therapie: Ceftobiprol, Ceftarolinfosamil
- Ceftobiprol
- Ceftarolinfosamil
Hemmkonzentration
Als minimale Hemmkonzentration (MHK) gegenüber Mikroorganismen wird die niedrigste Konzentration des Antibiotikums bezeichnet, bei der das Wachstum eines mikrobiellen Erregers über eine bestimmte Zeit gerade noch gehemmt ist.[10] Bei der mikrobiologischen Überprüfung neuer β-Laktam-Antibiotika erfolgt üblicherweise eine MHK-Untersuchung mit einer großen Anzahl meist frisch isolierter Bakterien gegenüber der neuen Substanz im Vergleich zu älteren Substanzen.[11]
| Allgemeine Struktur | Name | S. aureus | E. coli |
|---|---|---|---|
 | Cefalotin | 0,2–0,4 | 6,2 |
| Cephaloridin | 0,02 | 3,2–6,4 | |
| Cefapirin | 0,1–0,4 | 12 | |
| Cefamandol | 0,2–0,8 | 0,4–0,8 | |
| Cefuroxim | 0,8 | 0,8–6,2 | |
| Cefotaxim | 3,2 | 0,04–0,10 | |
| Cefoperazon | 1,6 | 0,04–0,40 |
Literatur
- Gunter Schmidt: Cephalosporine. In: Chemie in unserer Zeit. Band 10, Nr. 6, 1976, S. 189–195, doi:10.1002/ciuz.19760100605.
- Mutschler: Arzneimittelwirkung - Lehrbuch der Pharmakologie und Toxikologie. 8. Auflage. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2001, ISBN 3-8047-1763-2, S. 793–797.
- Klaus Aktories, Ulrich Förstermann, Franz Bernhard Hofmann, Klaus Starke: Allgemeine und spezielle Pharmakologie und Toxikologie. 12. Auflage. München 2017, ISBN 978-3-437-42525-7, 33.2.2.
Weblinks
Einzelnachweise
- ↑ A. Riva, B. Orrù, E. Fruciano:Giuseppe Brotzu and the Discovery of Cephalosporines ( vom 22. Februar 2014 im Internet Archive), 8th European Conference of Medical and Health Libraries, Köln 16. bis 21. September 2002.
- ↑ laut Unternehmensberater Morris Hosseini, zitiert von Tobias Lau: Bisher sind wir immer davongekommen, vielleicht auch diesmal, in: Apotheke ad hoc, 12. Februar 2020, abgerufen am 15. Februar 2020
- ↑ a b c d e f g Klaus Aktories, Ulrich Förstermann, Franz Bernhard Hofmann, Klaus Starke: Allgemeine und spezielle Pharmakologie und Toxikologie. 12. Auflage. München 2017, ISBN 978-3-437-42525-7, 33.2.2.
- ↑ Hahn H et al.: Medizinische Mikrobiologie und Infektiologie. 6. Auflage. Springer, Heidelberg 2009.
- ↑ Eintrag zu Cefalonium in der DrugBank der University of Alberta, abgerufen am 18. Juni 2019.
- ↑ Qin Lu, Nebulized Ceftazidime and Amikacin in Ventilator Associated Pneumonia, Am J Respir Crit Care Med 2011;184:106–115; PMID 21474643; doi:10.1164/rccm.201011-1894OC.
- ↑ H. Lüllmann, K. Moh, L. Hein, Taschenatlas Pharmakologie, 6. Auflage, Georg Thieme Verlag, Stuttgart 2008, S. 255.
- ↑ MSD (Hrsg.): Fachinformation ZERBAXA (Ceftolozane and Tazobactam).
- ↑ Fachinformation Zavicefta 2g/0,5g: Fachinformation Zavicefta 2g/0,5g. Hrsg.: Pfizer.
- ↑ Nils-Olaf Hübner, Katharina Sciermoch, Axel Kramer: Vergleich von Methoden zur Bestimmung der minimalen Hemmkonzentration und Schlussfolgerungen zur Weiterentwicklung der Methoden. In: GMS Krankenhaushygiene Interdisziplinär. Band 2, Nr. 2, 28. Dezember 2007, S. Doc34 (egms.de [abgerufen am 6. Dezember 2018]).
- ↑ B. Wiedemann: In-vitro-Beurteilungsparameter von Beta-Laktamring-Antibiotika. In: Infection. Band 6, Nr. 2, 1. März 1978, S. S203–S206, doi:10.1007/BF01638974.
- ↑ Gerhard G. Habermehl, Peter E. Hammann, Hans C. Krebs, W. Ternes: Naturstoffchemie: Eine Einführung. Springer, Berlin; 3., vollst. überarb. u. erw. Auflage 2008; ISBN 978-3-540-73732-2; S. 301.
Auf dieser Seite verwendete Medien
Autor/Urheber: Tamina212, Lizenz: CC BY-SA 4.0
Strukturformel von Ceftarolinfosamil
Autor/Urheber: Tamina212, Lizenz: CC BY-SA 4.0
Allgemeine Struktur klassischer Cephalosporine
Autor/Urheber: Tamina212, Lizenz: CC BY-SA 4.0
Strukturformel von Cepodoximproxetil
Autor/Urheber: Tamina212, Lizenz: CC BY-SA 4.0
Allgemeine Struktur klassischer Cephalosporine