Brown-Séquard-Syndrom
| Klassifikation nach ICD-10 | |
|---|---|
| G83.88 | Brown-Séquard-Syndrom |
| ICD-10 online (WHO-Version 2019) | |
Das Brown-Séquard-Syndrom (Abkürzung BSS) ist ein Symptomverbund aus der Gruppe der Rückenmarkssyndrome, der sich durch dissoziierte Sensibilitätsstörungen und einseitige Muskellähmungen auszeichnet. Ursächlich für das Auftreten der Symptome ist eine halbseitige Schädigung des Rückenmarks, meist infolge einer Quetschung oder anderweitigen Verletzung, selten auch Tumore im Wirbelkanal.
Einerseits kommt es beim BSS zu einer Lähmung der Willkürmuskulatur und einer Beeinträchtigung der Tiefen- und Feinsensibilität auf jener Körperhälfte, auf deren Seite die Läsion im Rückenmark liegt (ipsilateral). Andererseits ist auf der anderen Hälfte (kontralateral) die protopathische Sensibilität (Temperatur-, Druck- und Schmerzwahrnehmung) gestört. Diesem scheinbar diffusen Krankheitsbild liegt zu Grunde, dass das Rückenmark sowohl aus absteigenden motorischen als auch aus aufsteigenden sensiblen Nervenbahnen besteht, die in ihrem Verlauf teilweise auf die jeweils andere Seite des Marks wechseln, teilweise aber auch nicht. In einem weiteren Sinne spricht man von einem Brown-Séquard-Plus-Syndrom (Abkürzung BSPS), wann immer bei einer asymmetrischen Parese das Schmerzempfinden auf der weniger gelähmten Körperseite stärker vermindert ist.
Benannt ist es nach dem Neurologen Charles-Édouard Brown-Séquard, der es ab 1846 systematisch untersuchte. Obgleich das Krankheitsbild in seiner Reinform in der klinischen Praxis eine Seltenheit darstellt, lieferte die Erforschung seiner Pathogenese wesentliche Erkenntnisse zur Neuroanatomie und -physiologie. Noch heute wird die Pathophysiologie der im Brown-Séquard-Syndrom gebündelten Symptome im Tiermodell untersucht, um Phänomene neuronaler Plastizität und zentralen Schmerz besser verstehen zu können.
Pathologie
Anatomische Hintergründe

Efferenzen
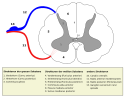
Efferente Nervenfasern leiten Signale vom Zentralnervensystem in die Körperperipherie, insbesondere in Form von Motoneuronen an die Muskulatur. Zwischen 70 und 90 Prozent jener Nerven, die als Teil der Pyramidenbahn für die Ausführung feinmotorischer und willkürlicher Bewegungen zuständig sind, kreuzen bereits vor dem Rückenmark im verlängerten Mark (Medulla oblongata) und steigen dann im Seitenstrang des Rückenmarks als Tractus corticospinalis lateralis (1a, s. Abbildung) ab. Die restlichen Fasern steigen auf der gleichen Seite (ipsilateral) im Vorderstrang als Tractus corticospinalis anterior (1b) ab und kreuzen entweder gar nicht oder erst auf Endigungshöhe. Ebenfalls ipsilateral steigen die für gröbere Bewegungsabläufe verantwortlichen Extrapyramidalbahnen (2a–d) gleichwohl wie vegetative Bahnen ab.[1]
Afferenzen
Afferenzen sind Nervenbahnen, die Signale von der Körperperipherie über das Rückenmark zum Gehirn leiten.
Die sensiblen Afferenzen für die Grobwahrnehmung (protopathische Sensibilität, grobe Druck-, Temperatur- und Schmerzempfindung) treten durch die Hinterwurzel in das Rückenmark ein und kreuzen noch im gleichen Segment auf die andere Seite (kontralateral). Von hier verlaufen sie als Tractus spinothalamicus, bestehend aus einem seitlichen (5a) und einem vorderen (5b) Trakt, zum Thalamus und von dort nach Umschaltung weiter zum sensiblen Gebiet der Großhirnrinde.[2]
Die Afferenzen zur Vermittlung der Tastschärfe (epikritische Sensibilität) und Tiefensensibilität steigen dagegen im Hinterstrang (Funiculus dorsalis oder beim Menschen auch Funiculus posterior, bestehend aus Fasciculus gracilis (3a) und Fasciculus cuneatus (3b)) von der Hinterwurzel ipsilateral zum Gehirn auf und kreuzen erst im Bereich der Medulla oblongata auf die andere Seite.[2]
Das vor allem für die Koordination komplexer Bewegungsabläufe zuständige Kleinhirn (Cerebellum) erhält über die Kleinhirnseitenstränge kontinuierlich Informationen über die Gesamtheit der Bewegungen. Zu diesen Strängen gehören die Tractus spinocerebellares posterior (4a) und anterior (4b), welche Informationen von den Mechanorezeptoren der unteren Gliedmaßen weiterleiten. Während die Axone des Tractus spinocerebellaris posterior ungekreuzt aufsteigen, kreuzen einige Axone des Tractus spinocerebellaris anterior durch die Commissura grisea anterior zunächst auf die Gegenseite, um von dort aus aufzusteigen und im Mittelhirn erneut zu kreuzen, bevor sie das Kleinhirn erreichen.[3] Der Tractus spinocerebellaris posterior leitet dabei überwiegend propriozeptive Impulse, also solche der Eigenwahrnehmung, der Tractus spinocerebellaris anterior sowohl proprio- als auch exterozeptive, also solche der Außenwahrnehmung, der Lokalisation und Qualität einer Tastempfindung.[2]
Folgen einer Halbseitenläsion
Bei halbseitiger Durchtrennung des Rückenmarkes werden sowohl kreuzende als auch nicht kreuzende Nervenstränge unterbrochen, wodurch es zu neurologischen Ausfällen auf beiden Seiten kommt. Die Unterbrechung motorischer Efferenzen bewirkt eine ipsilaterale Lähmung all jener Skelettmuskeln, die von Vorderhornzellen auf Läsionshöhe oder darunter versorgt werden. Diese Lähmung ist auf Höhe der Läsion selbst schlaff (segmental schlaffe Parese), da dort die Vorderhornzellen selbst mitgeschädigt sind, unterhalb dieser jedoch starr (durchgehende spastische Parese) mit gesteigerten Eigenreflexen und Pyramidenbahnzeichen infolge der Schädigung des Tractus corticospinalis lateralis.[4] Als Folge der Lähmung kommt es auch zur unilateralen Muskelatrophie.[5]
Da der Grobwahrnehmung vermittelnde Tractus spinothalamicus kreuzt, bevor er aufsteigt, treten Störungen des Schmerz- und Temperaturempfindens unterhalb der Läsion kontralateral auf. Im Gegensatz dazu kreuzen sowohl der Hinterstrang (Funiculus dorsalis bzw. posterior) als auch die Kleinhirnseitenstränge vor dem Aufsteigen nicht bzw. nur teilweise, sodass ipsilateral zur Läsion und ab dieser abwärts eine massive Störung der Tiefensensibilität und ein Verlust der Vibrationsempfindung auftreten. Zudem tritt eine kleine anästhetische Zone ipsilateral zur Läsion und knapp über dieser gelegen auf, was auf die Zerstörung der Hinterwurzeleintrittszone auf Läsionshöhe zurückgeführt wird.[6] Auf der lädierten Seite kann unterhalb der Läsion eine Hyperästhesie auftreten, bei der bereits eine leichte Berührung als Schmerz empfunden wird (Hyperalgesie). Sie wird auf das ipsilaterale Fortbestehen protopathischer Sensibilität bei gleichzeitigem Verlust der epikritischen Sensibilität zurückgeführt.[6] Die aufgrund der Unterbrechung von Kleinhirnseitensträngen zu erwartende Ataxie tritt klinisch nicht in Erscheinung, da sie durch die spastische Parese verdeckt wird.[4]
Darüber hinaus kommt es anfangs aufgrund der Schädigung zentraler Sympathikusbahnen, die im Seitenstrang absteigen, ipsilateral zur Erweiterung der Blutgefäße, wodurch sich die Haut anfangs rötet und überwärmt, später jedoch abkühlt und sich bläulich verfärbt. Stressbedingte Schweißproduktion im selben Areal ist vermindert oder erloschen.[7] Blase und Mastdarm bleiben bei einem reinen Brown-Séquard-Syndrom funktionstüchtig, da die hierfür verantwortlichen vegetativen Bahnen beidseitig absteigen.[4] Eine Läsion auf der Höhe des zervikothorakalen Übergangs (C7/Th1) führt zusätzlich zu einem ipsilateralen Horner-Syndrom.[8]
Klinik
Ätiologie
Es sind eine Vielzahl von Ursachen für ein Brown-Séquard-Syndrom möglich.[8][9] Zu den häufigeren gehören stumpfe oder penetrierende Verletzungen, epi- oder subdurale Hämatome der Rückenmarkshäute, Herniationen der Bandscheiben im Halsmarkbereich oder lokale Primärtumoren beziehungsweise Metastasen. In Einzelfällen kann sich auch eine Spinalkanalstenose als Brown-Séquard-Syndrom äußern.[10]
Die relative Häufigkeit Brown-Séquard-artiger Syndrome nach Stichverletzungen des Rückenmarks wird darauf zurückgeführt, dass die Quer- und Dornfortsätze der Wirbelsäule zusammen eine Mulde bilden, entlang derer ein Messer abgelenkt wird, sodass es nicht über den Dornfortsatz hinweg auf die andere Seite gelangt.[11] Während solche Verletzungen in gesellschaftlichen Situationen mit gesteigerter Gewaltbereitschaft gehäuft vorkommen können,[12] spielen in anderen Verkehrsunfälle als Ursache eine viel größere Rolle.[9]
Diagnostik
Leitsymptome des Brown-Séquard-Syndroms sind Lähmungen in der geschädigten Körperhälfte (ipsilaterale Hemiplegie) bei gleichzeitiger Schmerzunempfindlichkeit auf der gegenüberliegenden Seite (kontralaterale Hemianalgesie) in Form einer dissoziierten Sensibilitätsstörung.[13] In seiner reinen Form ist es sehr selten,[7][14] der Anteil an allen menschlichen Rückenmarkssyndromen wird auf 2–4 % geschätzt.[15] Oftmals treten unvollständige Formen auf, oder aufgrund der häufigen Mitschädigung der anderen Rückenmarkshälfte ist statt der erwarteten einseitigen eine beidseitige Lähmung (Paraparese) festzustellen.[7] In der wissenschaftlichen Literatur wird dem breiteren Spektrum an Symptomkomplexen, die in der klinischen Praxis auftreten, durch die erweiterte Definition eines Brown-Séquard-Plus-Syndroms (BSPS) Rechnung getragen. Ein solches besteht aus asymmetrischer Parese mit Hypalgesie auf der weniger paretischen Seite. Lähmung und Schmerzunempfindlichkeit müssen beim BSPS also jeweils weder vollständig sein noch ausschließlich eine Körperhälfte betreffen.[9]
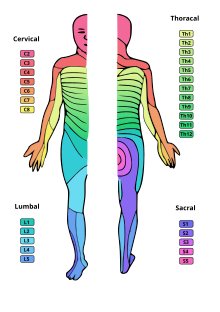
Diagnostisch steht eine neurologische Untersuchung mit entsprechender Prüfung der Motorik, des Temperatursinns sowie der Oberflächen- und Tiefensensibilität im Mittelpunkt. Zur lokalisatorischen Feststellung der Läsionshöhe orientiert man sich an der oberen Grenze des epikritischen Sensibilitätsausfalls („sensibler Spiegel“). Die Begrenzung des Ausfalls der protopathischen Sensibilität hingegen ist unscharf, da diese Bahnen über mehrere Segmente hinweg kreuzen. Die segmentale schlaffe Parese kann maskiert sein, da benachbarte Spinalnerven in ihrem Versorgungsgebiet einen gewissen Überschneidungsbereich aufweisen – entscheidend ist hier die Ausdehnung der Rückenmarksschädigung in kranio-kaudaler Richtung. Die wichtigsten bildgebenden Verfahren zur Feststellung von Ausmaß und Ursache der Läsion sind Röntgen, Computertomographie und Magnetresonanztomographie.[16]
| ipsilateral | kontralateral |
|---|---|
|
|
Therapie
Wenn der Läsion ein Tumor, der auf das Rückenmark drückt, zu Grunde liegt, kann das Rückenmark durch eine operative Entfernung des Tumors entlastet werden. Tritt die Symptomatik akut auf und lässt sich eine mechanische Rückenmarkskompression erkennen, so muss der Patient umgehend operiert werden. Obgleich eine Operation der Wirbelsäule im Falle traumatischer Rückenmarksverletzungen kaum eine Besserung der neurologischen Ausfälle mit sich bringt, erleichtert sie im weiteren Behandlungsverlauf die Remobilisation des Patienten und die Nachsorge im Allgemeinen, die Langzeitergebnisse sind besser und die Fähigkeit des Patienten, einen Rollstuhl zu benutzen, ebenfalls. An die ärztliche Versorgung schließt sich eine Physiotherapie an.[16]
Prognose
Bei adäquater Therapie erlangt ein Großteil der Patienten die Fähigkeit zurück, selbständig gehen zu können; der Anteil wird mit 75–90 % angegeben. Innerhalb der Gruppe unvollständiger Querschnittsyndrome kommt dem Brown-Séquard-Syndrom damit eine vergleichsweise gute Prognose zu.[17][18] Unbeschadet dessen werden beim Vergleich von reinem BSS mit dem BSPS im wissenschaftlichen Schrifttum unterschiedliche Ansichten vertreten. Koehler und Endtz gingen 1986 davon aus, dass Patienten mit reinem BSS eine bessere Prognose beschieden sein dürfte als solchen, bei denen es zu beidseitigen Lähmungen kommt, und sahen dies im Rahmen einer systematischen Übersichtsarbeit von Fallstudien zumindest im Hinblick auf solche Fälle bestätigt, denen eine nicht tumorbedingte Kompression oder nichtkompressive Läsion zu Grunde lag (N = 34).[8] Demgegenüber kam eine Studie von Roth et al. 1991 (N = 38) zu dem Ergebnis, dass Patienten mit BSPS eine statistisch signifikant kürzere Rehabilitationsdauer hatten, häufiger selbständig gehen konnten und im Mittel auf dem modifizierten Barthel-Index (MBI) höhere Gesamtwerte sowie höhere Werte auf den Subskalen für Mobilität und Selbstfürsorge erreichten. Im Hinblick auf Komplikationshäufigkeit, Blasenfunktion, Verbleib nach Entlassung und folgendem Erwerbsstatus waren dagegen keine Unterschiede zwischen BSS und BSPS ersichtlich. Als wichtigster Faktor zur Vorhersage funktionaler Rehabilitation erwies sich das Verhältnis zwischen der Schwäche von oberer und unterer Extremität. Patienten mit Halbseitenläsion auf Halshöhe, deren untere Extremität in geringerem Maße geschwächt war als die obere, wiesen eine höhere Wahrscheinlichkeit auf, bei Entlassung selbständig gehen zu können, sowie bessere MBI-Werte insgesamt und auf der Mobilitätssubskala.[9] Das Phänomen, dass Beinkontrolle und Gehfähigkeit nach zervikaler Rückenmarksschädigung oft besser regenerieren als Arm- und Handfunktion, ist klinisch wohlbekannt,[19] aber pathophysiologisch noch nicht verstanden.[20]
In einem Review von Fällen unterschiedlicher Rückenmarksverletzungen (N = 175) stellten McKinley et al. 2007 fest, dass das Ausmaß der Behinderung bei den meisten Patienten mit diagnostiziertem BSS bzw. BSPS (N = 30) bereits vor Behandlungsbeginn – gemessen in der ASIA Impairment Scale[21] – vergleichsweise gering war. Bei zervikalem BS(P)S erschienen die funktionellen Verbesserungen, die durch Rehabilitationsmaßnahmen erreicht werden konnten, besser im Vergleich zum zentralen Rückenmarkssyndrom.[18] In dem Zusammenhang wiesen Pouw et al. 2010 im Rahmen einer prospektiven Studie darauf hin, dass sich bei tetraplegischen Patienten (N = 148) die meisten Werte auf neurologischen und funktionellen Skalen zwölf Monate nach Therapiebeginn bei BSPS (N = 30) nicht signifikant von solchen mit anderen Formen unvollständiger Tetraplegie unterschieden, wenn dabei die jeweilige Verletzungsschwere berücksichtigt wird.[22]
Geschichte und Stand der Forschung
Im frühen 19. Jahrhundert waren die Mediziner Charles Bell in Großbritannien und François Magendie in Frankreich unabhängig voneinander zu der Erkenntnis gelangt, dass die vorderen und hinteren Wurzeln der Spinalnerven unterschiedliche Funktionen vermitteln („Bell-Magendie-Gesetz“).[23] Als klinischen Beleg für diese Gesetzmäßigkeit präsentierte der britische Militärchirurg Robert Dundas im Jahr 1825 der Fachöffentlichkeit den Fall eines Steinmetz im British Hospital im brasilianischen Bahia, welcher nach einem Sturz von einem sechs Meter hohen Gerüst von der Schulter an abwärts auf der linken Körperseite zu keiner willkürlichen Bewegung mehr imstande war, während auf der rechten zwar sein Empfinden ausgelöscht war, seine Muskeln dort dagegen tadellos funktionierten.[24] Dieser Fallbericht gilt heute als erste Dokumentation eines Brown-Séquard-Syndroms,[8] wenngleich auch schon behauptet worden ist, der italienische Arzt Bernardino Ramazzini habe bereits 1700 ein solches Syndrom beschrieben.[25]
Auf dieser Grundlage etablierte sich die allgemeine Ansicht, wonach motorische und sensorische Nervenbahnen in getrennten, wohldefinierten Bereichen durch das Zentralnervensystem verlaufen: motorische im Vorder-, sensorische im Hinterhorn der grauen Substanz. Vor allem der französische Physiologe François Achille Longet – ein Schüler Magendies – vertrat eine strikte räumliche Trennung dieser beiden Funktionen. Gegen diese vermeintliche Klarheit wandte der britisch-französische Mediziner Charles-Édouard Brown-Séquard in seiner Dissertation[26] 1846 die zahlreichen ungeklärten Widersprüche mit Ergebnissen anderer Forscher ein und führte systematische Vivisektionen an verschiedenen Spezies durch, um sie aufzulösen. Im Laufe der folgenden Jahre gelang es ihm anhand systematischer Tierversuche und klinischer Untersuchung von Patienten mit einseitigen Rückenmarksverletzungen zu zeigen, dass die sensorischen Nervenbahnen zum einen keineswegs einheitlich verlaufen, sondern sich dabei je nach Sinnesmodalität unterscheiden, und sie zum anderen zu wesentlichen Teilen tatsächlich nicht innerhalb des Hinterhorns aufsteigen, teilweise sogar auf die andere Seite des Rückenmarks kreuzen – im Gegensatz zu motorischen Bahnen.[23]
Zunächst trafen diese Schlussfolgerungen auf einigen Widerstand. Auf Brown-Séquards Bitte hin bildete die Société de Biologie in Paris einen Ausschuss, der seine Forschungsarbeit begutachtete, einige Schlüsselexperimente wiederholte, und schließlich seine Ergebnisse umfassend bestätigte. Über die Umwälzung der bis dahin gültigen Vorstellungen erklärte der Ausschussvorsitzende Paul Broca 1855 vor der Société:
« [C]ette doctrine si séduisante et si applaudie n’est qu’une déception de plus ajoutée à tant d’autres qui l’ont précédée, et dont les débris jonchent le sol de l’histoire. Les belles expériences de M. Brown-Séquard viennent de renverser pour toujours cet édifice si bien cimenté, dont Charles Bell avait jeté les fondements et dont M. Longet avait scellé la dernière pierre. Tant il est vrai que les apparances sont souvent trompeuses, et que les plus belles choses ont souvent le pire destin ! […] A aucune époque peut-être la physiologie du système nerveux n’a été bouleversée par une révolution plus radicale et plus rapide. »
„Diese so verführerische wie bejubelte Doktrin erweist sich als nur eine weitere Enttäuschung unter vielen anderen, die ihr vorangegangen sind und deren Trümmer auf dem Boden der Geschichte verstreut liegen. Die schönen Experimente des Hrn. Brown-Séquard haben dieses so fest zementierte Gebäude soeben niedergerissen, dessen Fundament Charles Bell gelegt hatte und das von Hrn. Longet versiegelt worden war. So erweist sich als wahr, dass der Schein oftmals trügt und den schönsten Dingen oft das schlimmste Schicksal beschieden ist! […] Vielleicht in keinem Zeitalter ist die Physiologie des Nervensystems von einer radikaleren und schnelleren Revolution umgestürzt worden.“
Umfangreiche Forschungen des Physiologen Moritz Schiff – eines weiteren ehemaligen Magendie-Schülers – ergänzten genauere Erkenntnisse zum Verlauf der Nervenbahnen einzelner Sinnesmodalitäten, wobei im Einzelnen noch Fragen offen blieben, insbesondere die Ursache für die gelegentlich beobachtete ipsilaterale Hyperästhesie.[23]
Nachdem seine Revision des bis dahin gültigen Bildes allgemein akzeptiert worden war, kam Brown-Séquard in späteren Jahren selbst aufgrund weitergehender Studien zu dem Ergebnis, dass auch dieses neue Bild unzulänglich ist. Als im Jahre 1892 der junge Physiologe Frederick Walker Mott[28] der Royal Society in London von experimentellen Befunden an Affen berichtete, die der inzwischen etablierten Theorie widersprachen, war Brown-Séquard voll des Lobes für Motts Arbeit. Noch in seinem letzten Lebensjahr entwarf er 1894[29] – Charles Scott Sherringtons Konzept reziproker Hemmung vorgreifend[8] – Grundzüge eines differenzierten Modells der Neurophysiologie, das ein dynamisches Zusammenspiel exzitatorischer und inhibitorischer Signale postulierte. Mit diesen Vorstellungen jedoch war er seiner Zeit erneut voraus; erst 1979 wurden sie vom Neurologen Derek Denny-Brown aufgegriffen, welcher systematisch an Makaken untersuchte, wie sich die sensorische Symptomatik verändert, wenn das Rückenmark weiter kopfwärts (kranial) ein weiteres Mal halbseitig lädiert wird. Denny-Brown kombinierte, dass der kontralaterale Sensibilitätsverlust nach einseitiger Durchtrennung des Tractus spinothalamicus lateralis auf der Unterbrechung einer inhibitorischen Wirkung beruht und unter lokaler Gabe von Strychnin zeitweise rückgängig gemacht werden kann. Vollständige Durchtrennung des Vorderstrangs auf Läsionsseite führt insoweit zu einer Symptomumkehr, als dass kontralateral Empfindsamkeit in schlecht modulierter Form wieder zurückkehrt, sich nun aber ein ipsilateraler Sensibilitätsverlust bemerkbar macht, der auf Überfunktion des intakten kontralateralen Vorderstrangs zurückgeführt wird.[30] Der deutsche Neurologe Klaus-Joachim Zülch wies auf den Konflikt zwischen den „sensationellen“ Schlussfolgerungen Denny-Browns und der Lokalisationslehre des Neurochirurgen Otfrid Foerster – seines Doktorvaters – hin.[31] Der britische Neurowissenschaftler und Schmerzmediziner Patrick David Wall betonte 1988[32] die Bedeutung des von Brown-Séquard in seinen späteren Schaffensjahren entwickelten Konzepts eines neuronalen Gleichgewichts für die Möglichkeit der Behandlung sensorischer Störungen nach zentralnervösen Schädigungen.[23]
In jüngeren tierexperimentellen Studien werden nach Hemiläsion des Rückenmarks nicht nur Verhaltensbeobachtungen und post mortem histologische Untersuchungen, sondern auch in vivo elektrophysiologische Methoden angewandt, wodurch sich die zentralnervösen Signalwege genauer nachvollziehen lassen.[33][34][35] Dabei haben sich weitere Hinweise dafür ergeben, dass die Entwicklung ipsilateraler Hyperästhesie ein Ausdruck neuronaler Plastizität als Reaktion auf ein gestörtes neuronales Gleichgewicht sein könnte.[34] Ein genaueres Verständnis der dem Brown-Séquard-Syndrom zugrundeliegenden Pathophysiologie könnte weiteren Aufschluss über die Entstehung und Behandlung zentraler Schmerzen geben.[30][33]
Literatur
Frühe Forschungsarbeiten
- Robert Dundas: Case of Concussion of the Spine, tending to confirm the Opinion, that the Nerves of Sensation and of Motion are Distinct. In: Edinburgh Medical and Surgical Journal, 1825, Band 23, Nr. 83, S. 304–307, PMID 30329672.
- Charles-Édouard Brown: Recherches et expériences sur la physiologie de la moelle épinière. Dissertation, Paris 1846. Online auf Google Books.
- Charles-Édouard Brown-Séquard: De la transmission des impressions sensitives par la moelle épinière. In: Comptes rendus des séances de la Société de Biologie et de ses filiales. Jahrgang 1849 (erschienen 1850), S. 192–194. Online archiviert auf Gallica.
- Charles-Édouard Brown-Séquard: De la transmission croisée des impressions sensitives par la moelle épinière. In: Comptes rendus des séances de la Société de Biologie et de ses filiales, Jahrgang 1850 (erschienen 1851), Band 2, S. 33–34. Online archiviert auf Gallica.
- Paul Broca: Rapport sur les expériences de M. Brown-Séquard, relatives aux propriétés et aux fonctions de la moelle épinière. In: Comptes rendus des séances de la Société de Biologie et de ses filiales, Jahrgang 1855 (erschienen 1856), S. 23–50. Online archiviert auf Gallica.
- Charles-Édouard Brown-Séquard: Course of Lectures on the Physiology and Pathology of the Central Nervous System: Delivered at the Royal College of Surgeons of England in May, 1858. Collins, Philadelphia 1860. Ebook auf Google Play.
- Charles-Édouard Brown-Séquard: Lectures on the physiology and pathology of the central nervous system and on the treatment of organic nervous affections. Lecture I: On spinal hemiplegia. In: The Lancet, 1868, Band 2, erschienen in vier Teilen:
- Nr. 2358, S. 593–596, doi:10.1016/S0140-6736(02)72108-9, online auf ScienceDirect,
- Nr. 2360, S. 659–662, doi:10.1016/S0140-6736(02)75931-X, online auf ScienceDirect,
- Nr. 2363, S. 755–757, doi:10.1016/S0140-6736(02)50188-4, online auf ScienceDirect,
- Nr. 2365, S. 821–823, doi:10.1016/S0140-6736(02)52465-X, online auf ScienceDirect.
- Charles-Édouard Brown-Séquard: Remarques à propos des recherches du Dr F. W. Mott sur les effets de la section d’une moitié latérale de la moelle épinière. In: Archives de physiologie normale et pathologique, 1894, Band 5, Nr. 6, S. 195–198. Online archiviert auf Gallica.
Aktuelle Forschungsarbeiten
- Charles H. Hubscher, Richard D. Johnson: Differential effects of chronic spinal hemisection on somatic and visceral inputs to caudal brainstem. In: Brain Research, 2002, Band 947, Nr. 2, S. 234–242, doi:10.1016/S0006-8993(02)02930-X.
- M. Wirz, B. Zörner, R. Rupp, V. Dietz: Outcome after incomplete spinal cord injury: central cord versus Brown-Sequard syndrome. In: Spinal Cord, 2010, Band 48, Nr. 5, S. 407–414, doi:10.1038/sc.2009.149.
- A. Vedantam, M. B. Jirjis, B. D. Schmit, M. D. Budde, J. L. Ulmer, M. C. Wang, S. N. Kurpad: Diffusion tensor imaging and tractography in Brown-Sequard syndrome. In: Spinal Cord, 2012, Band 50, Nr. 12, S. 928–930, doi:10.1038/sc.2012.94.
- Angel Gil-Agudo, Soraya Pérez-Nombela, Enrique Pérez-Rizo, Antonio del Ama-Espinosa, Beatriz Crespo-Ruiz, José L. Pons: Comparative biomechanical analysis of gait in patients with central cord and Brown-Séquard syndrome. In: Disability and Rehabilitation, 2013, Band 35, Nr. 22, S. 1869–1876, doi:10.3109/09638288.2013.766268.
- Björn Zörner, Lukas C. Bachmann, Linard Filli, Sandra Kapitza, Miriam Gullo, Marc Bolliger, Michelle L. Starkey, Martina Röthlisberger, Roman R. Gonzenbach, Martin E. Schwab: Chasing central nervous system plasticity: the brainstem's contribution to locomotor recovery in rats with spinal cord injury. In: Brain, 2014, Band 137, Nr. 6, S. 1716–1732, doi:10.1093/brain/awu078.
Übersichtsarbeiten und Lehrbücher
- Peter J. Koehler, Lambertus J. Endtz: The Brown-Séquard Syndrome: True or False? In: Archives of Neurology, 1986, Band 43, Nr. 9, S. 921–924, doi:10.1001/archneur.1986.00520090051015.
- Michael J. Aminoff: Brown-Séquard and his syndrome. In: Journal of the History of the Neurosciences, 1996, Band 5, Nr. 1, S. 14–20, doi:10.1080/09647049609525646.
- E. J. Roth, T. Park, T. Pang, G. M. Yarkony, M. Y. Lee: Traumatic cervical Brown-Sequard and Brown-Sequard-plus syndromes: the spectrum of presentations and outcomes. In: Paraplegia, 1991, Band 29, S. 582–589, doi:10.1038/sc.1991.86.
- Marco Mumenthaler, Claudio Bassetti, Christof Daetwyler: Neurologische Differenzialdiagnostik. Georg Thieme Verlag, Stuttgart 2005 (5. Auflage), ISBN 9783135924052, S. 16–17.
Einzelnachweise
- ↑ Werner Kahle, Michael Frotscher: Taschenatlas der Anatomie, Band 3: Nervensystem und Sinnesorgane. Georg Thieme Verlag, Stuttgart 2002 (8. Auflage), ISBN 3134922088, S. 56 u. 309.
- ↑ a b c Werner Kahle, Michael Frotscher: Taschenatlas der Anatomie, Band 3: Nervensystem und Sinnesorgane. Georg Thieme Verlag, Stuttgart 2002 (8. Auflage), ISBN 3134922088, S. 56.
- ↑ Stefan Huggenberger, Natasha Moser, Hannsjörg Schröder, Bruno Cozzi, Alberto Granato, Adalberto Merighi: Neuroanatomie des Menschen. Springer, Berlin 2019, ISBN 978-3-662-56461-5 (Ebook), S. 41.
- ↑ a b c Bettina Ende-Henningsen: Spinale Syndrome. In: Peter Berlit (Hrsg.): Klinische Neurologie. Springer Reference Medizin. Springer, Berlin/Heidelberg 2020, ISBN 978-3-662-60676-6 (Ebook), S. 85–86.
- ↑ J. Larry Jameson, Dennis Kasper, Stephen Hauser, Dan Longo, Anthony Fauci, Joseph Loscalzo: Harrison’s Principles of Internal Medicine. 21. Auflage, McGraw-Hill, New York 2022, Band 2, ISBN 9781-2642-6848-1, S. 3446.
- ↑ a b Werner Kahle, Michael Frotscher: Taschenatlas der Anatomie, Band 3: Nervensystem und Sinnesorgane. Georg Thieme Verlag, Stuttgart 2002 (8. Auflage), ISBN 3134922088, S. 68.
- ↑ a b c Marco Mumenthaler, Claudio Bassetti, Christof Daetwyler: Neurologische Differenzialdiagnostik. Georg Thieme Verlag, Stuttgart 2005 (5. Auflage), ISBN 9783135924052, S. 16.
- ↑ a b c d e Peter J. Koehler, Lambertus J. Endtz: The Brown-Séquard Syndrome: True or False? In: Archives of Neurology, 1986, Band 43, Nr. 9, S. 921–924, doi:10.1001/archneur.1986.00520090051015.
- ↑ a b c d E. J. Roth, T. Park, T. Pang, G. M. Yarkony, M. Y. Lee: Traumatic cervical Brown-Sequard and Brown-Sequard-plus syndromes: the spectrum of presentations and outcomes. In: Paraplegia, 1991, Band 29, S. 582–589, doi:10.1038/sc.1991.86.
- ↑ Sepehr Sani, Tibor Boco, Harel Deutsch: Cervical stenosis presenting with acute Brown-Sequard syndrome: case report. In: Spine, 2005, Band 30, Nr. 16, E481-3, PMID 16103843, doi:10.1097/01.brs.0000174284.08440.1e.
- ↑ W. J. Peacock, R. D. Shrosbree, A. G. Key: A review of 450 stabwounds of the spinal cord. In: South African Medical Journal, 1977, Band 51, Nr. 26, S. 961–964, PMID 888030. Online archiviert auf der Website des SAMJ.
- ↑ Robert Lipschitz, Joseph Block: Stab wounds of the spinal cord. In: The Lancet, 1962, Band 28, Nr. 2 (7248), S. 169–172, doi:10.1016/s0140-6736(62)90054-5.
- ↑ Karl F. Masuhr, Marianne Neumann: Duale Reihe – Neurologie. Hippokrates Verlag, Stuttgart 1998 (4. Auflage), ISBN 3-7773-1334-3, S. 123.
- ↑ Niklas von Spreckelsen, Roland H. Goldbrunner, Boris Krischek, Christoph Kolja Boese: Querschnittslähmung. In: Gregor Stein, Peer Eysel, Max Joseph Scheyerer (Hrsg.): Expertise Orthopädie und Unfallchirurgie Wirbelsäule. Georg Thieme Verlag, Stuttgart 2019, ISBN 9783132403765, S. 404.
- ↑ Keith C. Hayes, Jane T. C. Hsieh, Dalton L. Wolfe, Patrick J. Potter, Gail A. Delaney: Classifying Incomplete Spinal Cord Injury Syndromes: Algorithms Based on the International Standards for Neurological and Functional Classification of Spinal Cord Injury Patients. In: Archives of Physical Medicine and Rehabilitation, 2000, Band 81, S. 644–652, doi:10.1016/s0003-9993(00)90049-2.
- ↑ a b Helmut Rössler, Wolfgang Rüther: Orthopädie und Unfallchirurgie. Elsevier, 19. Auflage, München 2007, ISBN 978-3-437-44445-6, S. 183.
- ↑ Dennis A. Velez, David W. Newell: Spine Injuries. In: Anne J. Moore, David W. Newell (Hrsg.): Neurosurgery: Principles and Practice. Springer, London/Berlin/Heidelberg 2005, ISBN 1-85233-522-X, S. 382.
- ↑ a b William McKinley, Katia Santos, Michelle Meade, Karen Brooke: Incidence and Outcomes of Spinal Cord Injury Clinical Syndromes. In: The Journal of Spinal Cord Medicine, 2007, Band 30, Nr. 3, S. 215–224, doi:10.1080/10790268.2007.11753929.
- ↑ Allan D. O. Levi, Charles H. Tator, Richard P. Bunge: Clinical Syndromes Associated with Disproportionate Weakness of the Upper versus the Lower Extremities after Cervical Spinal Cord Injury. In: Neurosurgery, 1996, Band 38, Nr. 1, S. 179–185, doi:10.1097/00006123-199601000-00039.
- ↑ Linard Filli, Björn Zörner, Oliver Weinmann, Martin E. Schwab: Motor deficits and recovery in rats with unilateral spinal cord hemisection mimic the Brown-Sequard syndrome. In: Brain, 2011, Band 134, Nr. 8, S. 2261–2273, doi:10.1093/brain/awr167.
- ↑ vgl. ICF Case Studies: American Spinal Injury Association (ASIA) Impairment Scale.
- ↑ M. H. Pouw, H. van de Meent, J. J. van Middendorp, S. Hirschfeld, R. Thietje, A. van Kampen, EM-SCI study Group & A. J. F. Hosman: Relevance of the diagnosis traumatic cervical Brown-Séquard-plus syndrome: an analysis based on the neurological and functional recovery in a prospective cohort of 148 patients. In: Spinal Cord, 2010, Band 48, S. 614–618, doi:10.1038/sc.2009.189.
- ↑ a b c d Michael J. Aminoff: Brown-Séquard and his syndrome. In: Journal of the History of the Neurosciences, 1996, Band 5, Nr. 1, S. 14–20, doi:10.1080/09647049609525646.
- ↑ Robert Dundas: Case of Concussion of the Spine, tending to confirm the Opinion, that the Nerves of Sensation and of Motion are Distinct. In: Edinburgh Medical and Surgical Journal, 1825, Band 23, Nr. 83, S. 304–307, PMID 30329672.
- ↑ F. Clifford Rose: History of British Neurology. Imperial College Press, London 2012, ISBN 978-1-84816-668-4, S. 153.
- ↑ Charles-Édouard Brown: Recherches et expériences sur la physiologie de la moelle épinière. Dissertation, Paris 1846, S. 20–30. Online auf Google Books.
- ↑ Paul Broca: Rapport sur les expériences de M. Brown-Séquard, relatives aux propriétés et aux fonctions de la moelle épinière. In: Comptes rendus des séances de la Société de Biologie et de ses filiales, Jg. 1855 (ersch. 1856), S. 20 / 50 f. Online archiviert auf Gallica.
- ↑ Frederick W. Mott: Results of Hemisection of the Spinal Cord in Monkeys. In: Philosophical Transactions of the Royal Society of London, B, 1892, Band 183, S. 1–59, doi:10.1098/rstb.1892.0001. Online archiviert auf JStor.
- ↑ Charles-Édouard Brown-Séquard: Remarques à propos des recherches du Dr F. W. Mott sur les effets de la section d’une moitié latérale de la moelle épinière. In: Archives de physiologie normale et pathologique, 1894, Band 5, Nr. 6, S. 195–198. Online archiviert auf Gallica.
- ↑ a b Derek Denny-Brown: The enigma of crossed sensory loss with cord hemisection. In: J. J. Bonica, J. C. Liebeskind, D. G. Albe-Fessard (Hrsg.): Advances in Pain Research and Therapy. Volume 3. Raven Press, New York 1979, ISBN 9780890042700, S. 889–895.
- ↑ Klaus-Joachim Zülch: Cerebral Localization („Lokalisationslehre“): A Critical Appraisal. In: Neurosurgical Review, 1979, Band 2, S. 177–186, doi:10.1007/BF01650648.
- ↑ Patrick David Wall: The design of experimental studies in the future development of restorative neurology of altered sensation and pain. In: M. R. Dimitrijevic, P. D. Wall, U. Lindblom (Hrsg.): Recent Achievements in Restorative Neurology. Volume 3. Karger, Basel 1990, ISBN 978-3-8055-5036-9, S. 197–205.
- ↑ a b Marc D. Christensen, Claire E. Hulsebosch: Chronic Central Pain after Spinal Cord Injury. In: Journal of Neurotrauma, 1997, Band 14, Nr. 8, S. 517–537, doi:10.1089/neu.1997.14.517.
- ↑ a b Charles H. Hubscher, Richard D. Johnson: Differential effects of chronic spinal hemisection on somatic and visceral inputs to caudal brainstem. In: Brain Research, 2002, Band 947, Nr. 2, S. 234–242, doi:10.1016/S0006-8993(02)02930-X.
- ↑ M. M. Rank, J. R. Flynn, C. R. Battistuzzo, M. P. Galea, R. Callister, R. J. Callister: Functional changes in deep dorsal horn interneurons following spinal cord injury are enhanced with different durations of exercise training. In: The Journal of Physiology, 2015, Band 593, Nr. 1, S. 331–345, doi:10.1113/jphysiol.2014.282640.
Auf dieser Seite verwendete Medien
Autor/Urheber: User:Polarlys, Lizenz: CC BY-SA 3.0
Bahnen des Rückenmarks (Querschnitt)
Autor/Urheber: User:Polarlys, Lizenz: CC BY 2.5
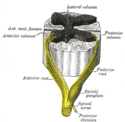
Rückenmark – Querschnitt
A diagram showing human dermatomes, i.e., skin regions with respect to the routing of their afferent nerves through the spinal cord.
Thoracic vertebra as seen from top.
Formation of spinal nerve from roots of spinal cord