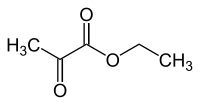
Brenztraubensäureethylester
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Brenztraubensäureethylester | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C5H8O3 | |||||||||||||||||||||
| Kurzbeschreibung | farblose Flüssigkeit mit stechendem Geruch[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 116,12 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand | flüssig[2] | |||||||||||||||||||||
| Dichte | 1,05 g·cm−3[2] | |||||||||||||||||||||
| Schmelzpunkt | −58 °C[2] | |||||||||||||||||||||
| Siedepunkt | 144–146 °C[2] | |||||||||||||||||||||
| Löslichkeit | wenig in Wasser (10 g·l−1 bei 20 °C)[2] | |||||||||||||||||||||
| Brechungsindex | 1,4056[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||||||||
Brenztraubensäureethylester ist eine chemische Verbindung aus der Gruppe der Pyruvate. Der α-Ketoester wirkt zytoprotektiv[4] und als Inhibitor der CO2-Sensoren der Gelbfiebermücke.[5]
Gewinnung und Darstellung
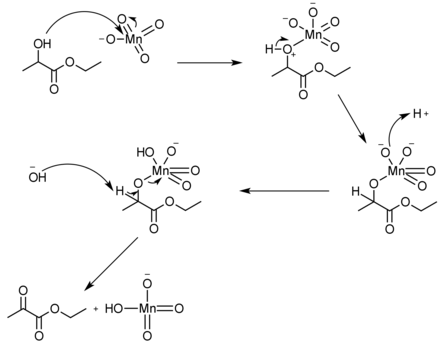
Brenztraubensäureethylester wird durch Oxidation von Milchsäureethylester mit Kaliumpermanganat gewonnen.
Einzelnachweise
- ↑ Eintrag zu ETHYL PYRUVATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 17. März 2020.
- ↑ a b c d e f g h Eintrag zu Ethylpyruvat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ a b c Datenblatt 4-Ethylpyruvat bei Merck, abgerufen am 17. Dezember 2013.
- ↑ X. Su, H. Wang, L. Zhu, J. Zhao, H. Pan, X. Ji: Ethyl pyruvate ameliorates intracerebral hemorrhage-induced brain injury through anti-cell death and anti-inflammatory mechanisms. In: Neuroscience. Band 245, 2013, S. 99–108, doi:10.1016/j.neuroscience.2013.04.032.
- ↑ Genevieve M. Tauxe, Dyan MacWilliam, Sean Michael Boyle, Tom Guda, Anandasankar Ray: Targeting a Dual Detector of Skin and CO2 to Modify Mosquito Host Seeking. In: Cell. Band 155, Nr. 6, 2013, S. 1365–1379, doi:10.1016/j.cell.2013.11.013, PMID 24315103.
Auf dieser Seite verwendete Medien
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for flammable substances
Ethylpyruvat; Brenztraubensäureethylester; 2-Oxopropionsäureethylester
(c) Tsmith60, CC BY-SA 3.0
Synthesis of ethyl pyruvate, starting with ethyl lactate and oxidizing it with potassium permanganate to form ethyl pyruvate. This picture shows the mechanism of this transformation.