Boc-Schutzgruppe
tert-Butyloxycarbonyl (Boc) ist eine Schutzgruppe. Innerhalb organischer Synthesestrategien verhindert sie die Umsetzung von freien Aminen. Haupteinsatzgebiet ist dabei der Aufbau von Peptiden im Rahmen der klassischen Festphasen-Peptid-Synthese nach Merrifield.
Verwendung
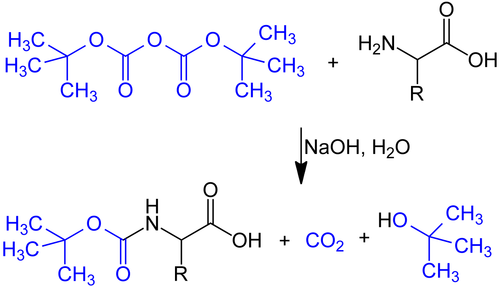
Die Boc-Gruppe lässt sich zum Schützen eines Amins einfach in ein Molekül einführen, indem das Amin basenkatalysiert mit Di-tert-butyldicarbonat umgesetzt wird:
Die Schutzgruppe ist unter vielen chemischen Reaktionsbedingungen stabil, wird aber leicht durch Säuren angegriffen. So wird häufig HCl in Methanol oder Trifluoressigsäure zum Entschützen verwendet. Wird die Boc-Gruppe neben der Fmoc-Gruppe [(9-Fluorenylmethyl)oxycarbonyl-] in einer Synthese eingesetzt, ergibt sich die Möglichkeit der orthogonalen Schutzgruppenstrategie: zwei unterschiedliche Amino-Funktionen eines Moleküls können gezielt nacheinander freigesetzt und zur Reaktion gebracht werden.
Literatur
- Alfred Pingoud, Claus Urbanke: Arbeitsmethoden der Biochemie. De Gruyter, Berlin, New York 1997, ISBN 3-11-016513-9, S. 180 (eingeschränkte Vorschau in der Google-Buchsuche).
Auf dieser Seite verwendete Medien
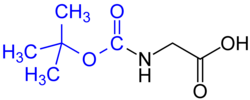
N-tert-Butoxycarbonyl_geschütztes_Glycin_Strukturformel
Autor/Urheber: Jü, Lizenz: CC BY-SA 4.0
Schutz der Aminofunftion einer Aminosäure durch BOC-Anhydrid