4-Nitrobiphenyl
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | 4-Nitrobiphenyl | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C12H9NO2 | |||||||||||||||||||||
| Kurzbeschreibung | Weiße bis gelbliche Kristallnadeln, süßlicher Geruch[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 199,21 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand | fest | |||||||||||||||||||||
| Dichte | 1,328 g·cm−3[1] | |||||||||||||||||||||
| Schmelzpunkt | 114–115 °C[1] | |||||||||||||||||||||
| Siedepunkt | 340 °C[1] | |||||||||||||||||||||
| Löslichkeit | praktisch unlöslich in Wasser[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
4-Nitrobiphenyl ist eine aromatische Nitroverbindung mit einer Biphenyl-Grundstruktur.
Darstellung
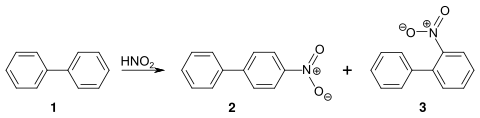
Die Herstellung von 4-Nitrobiphenyl 2 wurde erstmals 1874 von Gustav Schultz beschrieben.[3] Die Verbindung erhält man durch Nitrierung von Biphenyl 1, wobei Hans Hübner zeigen konnte, dass als Nebenprodukt 2-Nitrobiphenyl 3 entsteht:[4]
Alternativ ist 4-Nitrobiphenyl über eine Palladium-katalysierte Negishi-Reaktion zugänglich. Zunächst wird Brombenzol 1 mit Lithium in Diethylether zu Phenyllithium 2 umgesetzt. Umsetzung von Phenyllithium mit einer Lösung von Zinkchlorid in THF ergibt Phenylzinkchlorid 3. Dieses wird mit 4-Nitroiodbenzol 4 und einem Pd-Katalysator, hergestellt durch Reaktion von Bis(triphenylphosphin)palladiumchlorid Pd(PPh3)2Cl2 mit Diisobutylaluminiumhydrid, zu 4-Nitrobiphenyl 5 umgesetzt:[5]
Verwendung
Durch Reduktion der Nitroverbindung erhält man 4-Aminobiphenyl, das als Zwischenprodukt bei der Synthese von Farbstoffen oder Kautschuk-Antioxidantien verwendet wurde.[6][7]
Eigenschaften
Im Tierversuch wurde unter anderem 4-Aminobiphenyl als Metabolit des 4-Nitrobiphenyl nachgewiesen. Ebenso wurde in vitro in Gegenwart von Rattenleberenzymen eine schnelle Reduktion von 4-Nitrobiphenyl zum 4-Aminobiphenyl festgestellt. 4-Aminobiphenyl wirkt beim Menschen nachweislich kanzerogen, so dass eine kanzerogene Wirkung von 4-Nitrobiphenyl auch beim Menschen vermutet wird.[1] 4-Nitrobiphenyl ist in der REACH-Verordnung (EG) Nr. 1907/2006 Anhang XVII gelistet und darf demzufolge weder als Stoff noch in Gemischen in Konzentrationen von > 0,1 Gew.-% in Verkehr gebracht oder verwendet werden.[8]
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu 4-Nitrobiphenyl in der GESTIS-Stoffdatenbank des IFA, abgerufen am 31. Oktober 2019. (JavaScript erforderlich)
- ↑ Eintrag zu 4-nitrobiphenyl im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 31. Oktober 2019. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Gustav Schultz: Ueber Diphenyl. In: Justus Liebigs Annalen der Chemie. Band 174, Nr. 2, 1874, S. 201, doi:10.1002/jlac.18741740206.
- ↑ H. Hübner: Mittheilungen aus dem Göttinger Universitäts-Laboratorium. In: Berichte der deutschen chemischen Gesellschaft. Band 8, Nr. 1, Januar 1875, S. 870, doi:10.1002/cber.187500801286.
- ↑ Ivica Cepanec: Synthesis of Biaryls. Elsevier, Amsterdam, San Diego, Oxford, London 2004, ISBN 0-08-044412-1, S. 127 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Deutsche Gesetzliche Unfallversicherung (Hrsg.): Aromatische Amine. Eine Arbeitshilfe in Berufskrankheiten-Feststellungsverfahren. 4. Auflage. Berlin 2018, ISBN 978-3-86423-225-1, S. 74 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ 4-Aminobiphenyl. (PDF) In: IARC Monographs on the Identification of Carcinogenic Hazards to Humans. International Agency for Research on Cancer, abgerufen am 1. November 2019 (englisch).
- ↑ Anhang XVII der REACH-Verordnung. Bundesanstalt für Arbeitsschutz und Arbeitsmedizin, abgerufen am 1. November 2019 (Stand: 7. Januar 2019).
Auf dieser Seite verwendete Medien
synthesis of 4-Nitrobiphenyl by a Pd-catalyzed reaction of Phenyl zinc chloride with 4-Nitroiodobenzene (Negishi-Reaction)
Synthesis of 4-Nitrophenyl by nitration of biphenyl
Globales Harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS) Piktogramm für gesundheitsgefährdende Stoffe.
chemical structure of 4-Nitrobiphenyl
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances