3β-Hydroxysteroid-Dehydrogenase
| 3β-Hydroxysteroid-Dehydrogenase | ||
|---|---|---|
| Masse/Länge Primärstruktur | 371 / 372 / 369 Aminosäuren | |
| Sekundär- bis Quartärstruktur | single-pass Membranprotein (ER, Mit.) | |
| Isoformen | NP_000853, NP_000189, NP_079469 | |
| Bezeichner | ||
| Gen-Name(n) | HSD3B1, HSD3B2, HSD3B7 | |
| Externe IDs | ||
| Enzymklassifikationen | ||
| EC, Kategorie | 1.1.1.145, Oxidoreduktase | |
| Reaktionsart | Dehydrierung | |
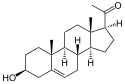
| Substrat | Pregnenolon + NAD+ | |
| Produkte | Pregn-5-en-3,20-dion + NADH/H+ | |
| EC, Kategorie | 5.3.3.1, Isomerase | |
| Reaktionsart | Umlagerung | |
| Substrat | Pregn-5-en-3,20-dion | |
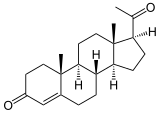
| Produkte | Progesteron | |
| Vorkommen | ||
| Übergeordnetes Taxon | mehrzellige Tiere, Protozoen[1] | |
3β-Hydroxysteroid-Dehydrogenasen (3β-HSD) sind Enzyme, die in Steroiden die 3β-Hydroxygruppe zum Keton oxidieren und gleichzeitig die Umlagerung der Doppelbindung von der 5- in die 4-Position katalysieren. Diese Reaktion wird in Wirbeltieren bei der Biosynthese von Progesteron aus Pregnenolon benötigt, genauso wie bei der Umwandlung von Dehydroepiandrosteron zu Androstendion oder von 17α-Hydroxypregnenolon zu 17α-Hydroxyprogesteron.
3β-HSD sind Transmembranproteine und lokalisieren zum endoplasmatischen Retikulum und zu den Mitochondrien. Beim Menschen sind drei paraloge Isoformen bekannt, die in unterschiedlichen Gewebetypen exprimiert werden: 3β-HSD I hauptsächlich in den Brustdrüsen, der Plazenta und der Haut; 3β-HSD II vor allem in Nebennieren, Hoden und Eierstöcken. Mutationen im HSD3B2-Gen sind verantwortlich für ein adrenogenitales Syndrom Typ 2 (CAH durch 3-beta-Hydroxysteroid-Dehydrogenase-Mangel).[3][2] Das dritte menschliche Enzym dieser Proteinfamilie ist 3β-HSD Typ 7, ein Enzym der Gallensäurebildung aus Cholesterin.[4]
Katalysierte Reaktionen
Pregnenolon wird zu Progesteron umgesetzt. Es findet nacheinander eine Dehydrierung zum Keton und eine Umlagerung der Doppelbindung statt. Eine weitere Reaktion ist die Umsetzung von DHEA zu Androstendion.[5]
Strukturverweis
Strukturmodell von HSD3B1: siehe vierter Weblink; aus [6]
Weblinks
- Jassal / reactome: DHA isomerizes to 4-Androstene3,17-dione
- Jassal / reactome: Pregn-5-ene-3,20-dione isomerizes to progesterone
- Jassal / reactome: Pregnenolone is dehydrogenated to form pregn-5-ene-3,20-dione
- Strukturverweis
Einzelnachweise
- ↑ Homologe bei inParanoid
- ↑ a b Welzel M, Wüstemann N, Sîmić-Schleicher G, et al.: Carboxyl-Terminal Mutations in 3β-Hydroxysteroid Dehydrogenase Type II Cause Severe Salt-Wasting Congenital Adrenal Hyperplasia. In: J. Clin. Endocrin. Metabol.. 93, September, S. 1418–1425.
- ↑ UniProt P26439, UniProt P14060
- ↑ Simard J, Ricketts M-L, Gingras S et al.: Molecular Biology of the 3β-Hydroxysteroid Dehydrogenase/Δ5-Δ4 Isomerase Gene Family. In: Endocrine Rev.. 26, 2005, S. 525–582. doi:10.1210/er.2002-0050. PMID 15632317.
- ↑ Pletnev VZ, Thomas JL, Rhaney FL, et al.: Rational proteomics V: structure-based mutagenesis has revealed key residues responsible for substrate recognition and catalysis by the dehydrogenase and isomerase activities in human 3beta-hydroxysteroid dehydrogenase/isomerase type 1. In: J. Steroid Biochem. Mol. Biol.. 101, Nr. 1, September 2006, S. 50–60. doi:10.1016/j.jsbmb.2006.06.004. PMID 16889958. PMC 1971842 (freier Volltext).
- ↑ Thomas JL, et al.: Structure/Function Relationships Responsible for Coenzyme Specificity and the Isomerase Activity of Human Type 1 3β-Hydroxysteroid Dehydrogenase/Isomerase. In: J.Biol.Chem.. 278, 2003, S. 35483–35490. PMID 12832414.
Auf dieser Seite verwendete Medien
Struktur von Pregnenolon
Struktur von Progesteron